Hạt Nhân Nguyên Tử Của Các Nguyên Tố đồng Vị Luôn Có Cùng số lượng proton, nhưng khác nhau về số lượng neutron. Để hiểu rõ hơn về khái niệm này và ứng dụng của nó trong lĩnh vực xe tải, hãy cùng Xe Tải Mỹ Đình khám phá chi tiết trong bài viết dưới đây. Chúng tôi sẽ cung cấp cho bạn cái nhìn sâu sắc về cấu tạo nguyên tử, đồng vị, và cách tính phần trăm đồng vị, từ đó giúp bạn hiểu rõ hơn về các vật liệu chế tạo xe tải.
1. Những Khái Niệm Tiền Đề Quan Trọng
Để hiểu rõ hơn về cách tính phần trăm đồng vị, chúng ta cần nắm vững một số khái niệm cơ bản về nguyên tử, nguyên tử khối, và nguyên tử khối trung bình.
1.1. Nguyên Tử Là Gì?
Nguyên tử là đơn vị cơ bản cấu tạo nên vật chất. Nó bao gồm một hạt nhân ở trung tâm, chứa các proton mang điện tích dương và neutron không mang điện tích, được bao quanh bởi các electron mang điện tích âm.
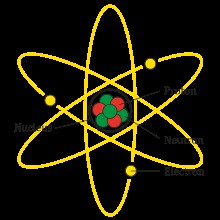 Mô hình cấu tạo nguyên tử, thể hiện các thành phần proton, neutron, và electron
Mô hình cấu tạo nguyên tử, thể hiện các thành phần proton, neutron, và electron
Số lượng proton trong hạt nhân xác định nguyên tố hóa học, trong khi số lượng neutron có thể khác nhau, tạo ra các đồng vị của nguyên tố đó. Theo Wikipedia, nguyên tử là thành phần cơ bản của mọi vật chất, và các tính chất của nó quyết định tính chất của vật chất đó.
1.2. Nguyên Tử Khối Là Gì?
Nguyên tử khối là khối lượng của một nguyên tử, thường được đo bằng đơn vị khối lượng nguyên tử (đvC). Nó được xác định chủ yếu bởi số lượng proton và neutron trong hạt nhân, vì electron có khối lượng rất nhỏ so với hai loại hạt này.
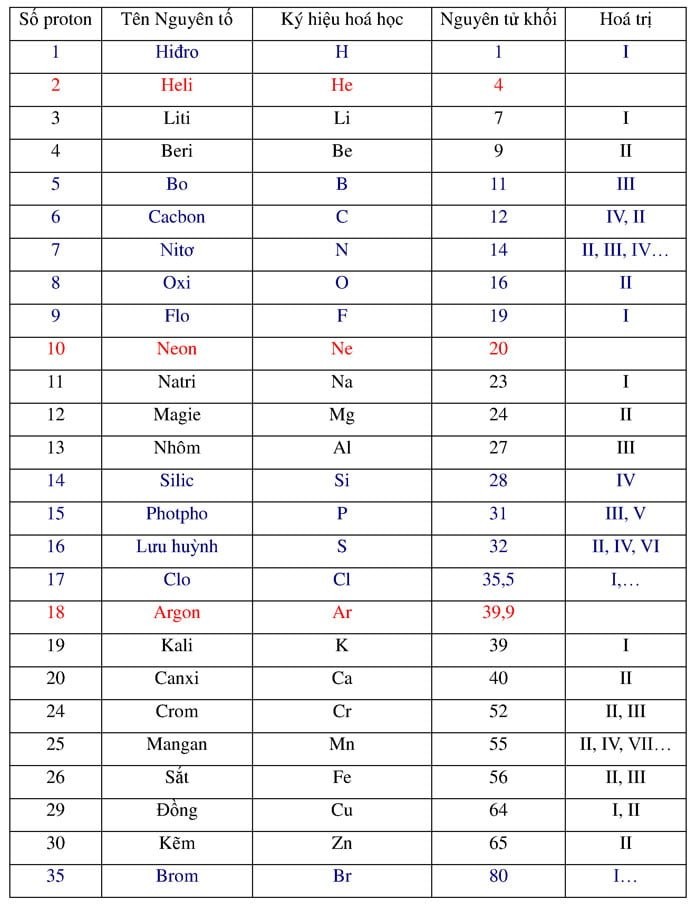 Bảng nguyên tử khối của các nguyên tố hóa học thường gặp
Bảng nguyên tử khối của các nguyên tố hóa học thường gặp
Ví dụ, nguyên tử khối của đồng (Cu) là khoảng 64 đvC, còn nguyên tử khối của sắt (Fe) là khoảng 56 đvC.
1.3. Nguyên Tử Khối Trung Bình Là Gì?
Nguyên tử khối trung bình là giá trị trung bình của nguyên tử khối của tất cả các đồng vị của một nguyên tố, được tính dựa trên tỷ lệ phần trăm của mỗi đồng vị trong tự nhiên. Công thức tính nguyên tử khối trung bình như sau:
A = (x₁.X₁ + x₂.X₂ + … + xₙ.Xₙ) / 100
Trong đó:
- A là nguyên tử khối trung bình của nguyên tố.
- X₁, X₂, …, Xₙ là nguyên tử khối của các đồng vị.
- x₁, x₂, …, xₙ là tỷ lệ phần trăm của các đồng vị tương ứng.
Ví dụ, nếu một nguyên tố A có hai đồng vị X và Y với tỷ lệ phần trăm lần lượt là x và y, thì nguyên tử khối trung bình của A sẽ là: A = (x%.X + y%.Y).
2. Đồng Vị Là Gì?
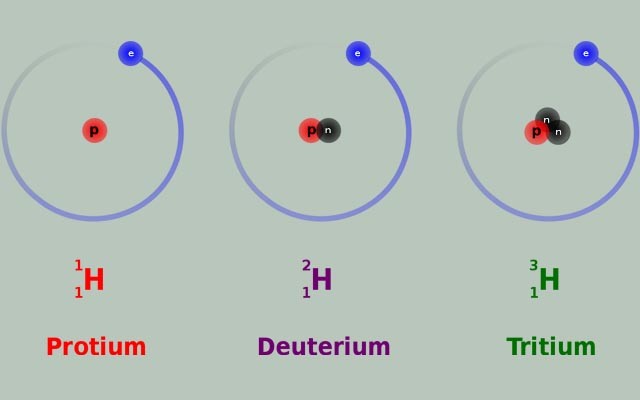
Đồng vị là các dạng khác nhau của cùng một nguyên tố hóa học, có cùng số lượng proton nhưng khác nhau về số lượng neutron trong hạt nhân.
2.1. Định Nghĩa Về Đồng Vị
Đồng vị là các nguyên tử có cùng số hiệu nguyên tử (Z) nhưng khác nhau về số khối (A). Điều này có nghĩa là chúng có cùng số lượng proton nhưng khác nhau về số lượng neutron.
 Mô tả các đồng vị của một nguyên tố, có cùng số proton nhưng khác số neutron
Mô tả các đồng vị của một nguyên tố, có cùng số proton nhưng khác số neutron
Ví dụ, neon (Ne) có ba đồng vị: Neon-20 (10 proton, 10 neutron), Neon-21 (10 proton, 11 neutron), và Neon-22 (10 proton, 12 neutron).
2.1.1. Phân Loại Đồng Vị
Đồng vị có thể được phân loại thành hai loại chính:
- Đồng vị bền: Là các đồng vị không tự phân rã theo thời gian.
- Đồng vị phóng xạ: Là các đồng vị không ổn định và tự phân rã, phát ra các hạt và năng lượng.
 Phân biệt đồng vị bền và đồng vị phóng xạ
Phân biệt đồng vị bền và đồng vị phóng xạ
Đồng vị phóng xạ được sử dụng rộng rãi trong nhiều lĩnh vực, bao gồm y học, khảo cổ học, và công nghiệp.
2.1.2. Ứng Dụng Của Đồng Vị
Đồng vị có nhiều ứng dụng quan trọng trong đời sống và công nghiệp. Ví dụ, đồng vị carbon-14 được sử dụng để xác định niên đại của các vật thể cổ, trong khi đồng vị uranium-235 được sử dụng trong các nhà máy điện hạt nhân.
Trong lĩnh vực xe tải, đồng vị có thể được sử dụng để nghiên cứu độ bền và tuổi thọ của các vật liệu chế tạo xe, giúp cải thiện chất lượng và hiệu suất của xe.
2.2. Cách Tính Phần Trăm Đồng Vị
Để tính phần trăm đồng vị của một nguyên tố, chúng ta sử dụng công thức sau:
M = (x₁.M₁ + x₂.M₂ + … + xₙ.Mₙ) / 100
Trong đó:
- M là nguyên tử khối trung bình của nguyên tố.
- M₁, M₂, …, Mₙ là nguyên tử khối của các đồng vị.
- x₁, x₂, …, xₙ là tỷ lệ phần trăm của các đồng vị tương ứng.
Để xác định phần trăm của từng đồng vị, chúng ta có thể sử dụng phương pháp đại số. Ví dụ, nếu một nguyên tố có hai đồng vị, chúng ta có thể gọi phần trăm của đồng vị 1 là x, và phần trăm của đồng vị 2 là (1 – x). Sau đó, chúng ta có thể giải phương trình để tìm giá trị của x.
2.3. Ví Dụ Minh Họa
Ví dụ 1: Đồng (Cu) có hai đồng vị là ⁶³Cu và ⁶⁵Cu. Biết rằng đồng có nguyên tử khối trung bình là 63,54. Tính thành phần phần trăm số nguyên tử của mỗi đồng vị.
Giải:
Gọi thành phần phần trăm của đồng vị ⁶³Cu là x (%), suy ra phần trăm của đồng vị ⁶⁵Cu là (100 – x) (%).
Ta có: 63,54 = (63.x + 65.(100-x))/100
=> -2x = -1,46
=> x = 73%
Vậy %⁶³Cu = 73%; và %⁶⁵Cu = 27%.
3. Bài Tập Vận Dụng
Để củng cố kiến thức về cách tính phần trăm đồng vị, chúng ta hãy cùng nhau giải một số bài tập sau:
Câu 1: Trong tự nhiên, nguyên tố cacbon tồn tại ở hai đồng vị bền: ¹²C chiếm 98,89% và ¹³C chiếm 1,11%. Từ các dữ liệu trên, hãy xác định nguyên tử khối trung bình của cacbon.
Giải:
Nguyên tử khối trung bình của cacbon là:
M = (12 98,89 + 13 1,11) / 100 = 12,0111
Vậy nguyên tử khối trung bình của cacbon là 12,0111.
Câu 2: Clo có hai đồng vị là ³⁵Cl và ³⁷Cl trong tự nhiên. Biết rằng nguyên tố clo có nguyên tử khối trung bình là 35,5. Hãy tính phần trăm về khối lượng của ³⁷Cl chứa trong hợp chất HClO₄ (với hiđro là đồng vị ¹H, oxi là đồng vị ¹⁶O).
Giải:
Gọi phần trăm đồng vị ³⁵Cl là x (%), thì suy ra phần trăm đồng vị ³⁷Cl là 100 – x (%).
Ta có nguyên tử khối trung bình của clo là:
35,5 = (35.x + 37.(100 – x)) / 100
Giải phương trình trên ta được x = 75 (%)
%³⁵Cl là 75% và %³⁷Cl là 25%
Phần trăm khối lượng của ³⁷Cl trong HClO₄ là:
(37 25) / (100 MHClO4) = (37 25) / (100 (1 + 35,5 + 16 * 4)) = 9,2%
Câu 3: Giả sử một nguyên tố A có 2 đồng vị với tỷ lệ số nguyên tử là 27:23. Biết rằng hạt nhân của nguyên tử A này chứa 35 proton và đồng vị thứ nhất có 44 hạt neutron trong nhân và có ít hơn đồng vị thứ hai 2 hạt neutron. Hãy tính nguyên tử khối trung bình của A.
Giải:
Đồng vị thứ nhất có nguyên tử khối là:
35 + 44 = 79
=> Nguyên tử khối của đồng vị thứ 2 bằng 81
=> MA= (79 27 + 81 23) / (27 + 23) = 79,23
Như vậy nguyên tử khối của A bằng 79,23
Câu 4: Nguyên tố oxi trong tự nhiên có thể tồn tại 3 dạng đồng vị lần lượt là:
⁸O¹⁶ (99,757%); ⁸O¹⁷ (0,039%); ⁸O¹⁸ (0,204%)
a) Hãy xác định khối lượng nguyên tử trung bình của oxi
b) Có thể tạo thành tối đa bao nhiêu loại phân tử oxi O₂
Giải:
a) Ta có:
M =(16 99,757% + 17 0,039% + 18 * 0,204%) = 16,004
Như vậy nguyên tử khối trung bình của oxi xấp xỉ 16
b) Phân tử oxi được cấu thành từ 2 nguyên tử oxi và vì oxi có 3 loại đồng vị nên số loại phân tử oxi là 3 * 3 = 9 (loại)
Câu 5:
Các nghiên cứu cho thấy nguyên tố Bo có khối lượng nguyên tử trung bình là 10,81. Biết rằng trong tự nhiên Bo có 2 loại đồng vị là ¹⁰B và ¹¹B. Tính phần trăm khối lượng của đồng vị ¹¹B trong hợp chất axit HBO₃ (M = 61,81).
Giải:
Đặt phần trăm đồng vị ¹⁰B là x (%), như vậy có thể suy ra phần trăm đồng vị ¹¹B là 1 – x (%)
Ta có:
10x + 11(1 – x) = 10,81
=> -x = -0,19
=> x = 0,19 = 19%
Như vậy % ¹⁰B là 19% và % ¹¹B là 81%
Phần trăm khối lượng đồng vị ¹¹B trong HBO₃ là:
(11 81%) / MHBO3 100% = (11 81%) / 61,81 100% = 14,41%
Câu 6: Một nguyên tố X trong tự nhiên có hai đồng vị ¹⁷X³⁵ và ¹⁷X³⁷ có thành phần phần trăm lần lượt 75,77% và 24,23%. Và một nguyên tố Y khác có 2 đồng vị là ¹Y¹¹ và ¹Y¹² thành phần của các đồng vị lần lượt 99,2% và 0,8% số nguyên tử Y.
a) Theo lý thuyết có tối đa bao nhiêu loại phân tử XY?
b) Tính phân tử khối trung bình của phân tử XY
Giải:
a) Nguyên tố X có 2 loại đồng vị và nguyên tố Y có 2 loại đồng vị như vậy số loại phân tử XY mà chúng ta có thể có là 2 * 2 = 4 (loại)
¹⁷X³⁵¹Y¹¹; ¹⁷X³⁷¹Y¹¹; ¹⁷X³⁵¹Y¹²; ¹⁷X³⁷¹Y¹²
b) Nguyên tử khối trung bình của X:
(35 75,77% + 37 24,23%) = 35,485
Nguyên tử khối trung bình của Y:
(1 99,2% + 2 0,8%) = 1,008
Vậy phân tử khối trung bình của phân tử XY:
35,485 + 1,008 = 36,493
Câu 7: Nguyên tố Bạc (Ag) trong tự nhiên có 2 đồng vị là ⁴⁷Ag¹⁰⁹ (chiếm 44% về số lượng nguyên tử) và một đồng vị khác. Biết rằng nguyên tử khối trung bình của Ag là 107,88. Hãy tính số khối của đồng vị thứ hai.
Giải:
Đặt số khối của đồng vị thứ 2 là x
Phần trăm số nguyên tử của đồng vị thứ 2 là 100% – 44% = 56%
Ta có, khối lượng nguyên tử trung bình là:
A = (44% 109 + 56% x) = 107,08
=> x = 107
Vậy đồng vị thứ hai của bạc là ⁴⁷Ag¹⁰⁷
Câu 8: Giả sử có hợp chất XY₂ được cấu thành bởi 2 nguyên tố X và Y. Y có 2 đồng vị là Y⁷⁹ và Y⁸¹ trong đó đồng vị Y⁷⁹ chiếm 55% . Biết rằng trong hợp chất XY₂ thì X chiếm 28,44% khối lượng của phân tử. Xác định khối lượng nguyên tử trung bình của X và Y?
Giải:
Phần trăm số nguyên tử của đồng vị Y⁸¹ là 100% – 55% = 45%
Như vậy suy ra, nguyên tử khối trung bình của Y là:
My= (55%79+45%81)=79,9
Theo đầu bài ta có X chiếm 28,44% khối lượng phân tử XY₂ suy ra:
%MX= X/(X + 2Y) * 100% = 28,44%
=> X/(X + 279,9) 100% = 28,44%
=> X=63,73
Câu 9: Cho hợp chất AB₂ được hình thành bởi hai nguyên tố A và B. Trong đó, nguyên tố B có hai đồng vị là ⁷⁹B, chiếm 55% và còn lại là đồng vị ⁸¹B. Biết rằng trong phân tử AB₂, nguyên tố A có thành phần phần trăm khối lượng là 28,51%. Hãy tính nguyên tử khối trung bình của các nguyên tố A và B.
Giải:
Từ đầu bài chúng ta có:
Phần trăm số nguyên tử của ⁸¹B là 100%−55% = 45%
Nguyên tử khối trung bình của nguyên tố B là:
MB= (55%79 + 45%81) = 79,9
Ta có %MA= MA/(MA + 2MB).100% = 28,51%
=> MA = 0,2851(MA + 2.79,9)
=> MA = 63,73
Câu 10: Giả sử rằng một nguyên tố X gồm hai đồng vị là XA và XB. Đồng vị XA có tổng số hạt là 18. Đồng vị XB có tổng số hạt là 20. Biết rằng thành phần phần trăm các đồng vị của nguyên tố X là bằng nhau và các loại hạt trong XA cũng bằng nhau. Hãy xác định nguyên tử khối trung bình của nguyên tố X.
Giải:
Theo đầu bài ta có các loại hạt trong X1 bằng nhau
=> pXA = eXA = nXA = 18/3 = 6
Vì XA và XB là hai đồng vị nên có số proton bằng nhau
=> pXA = pXB = 6 = eXB
Ta có tổng số hạt trong đồng vị XB là 20
=> pXB + eXB + nXB = 20
=> nXB = 20 – 6 – 6 = 8
Vậy số khối của XA là 12 và XB là 14
Nguyên tử khối trung bình của nguyên tố X là:
X=(1250% + 1450%) =13
4. Ứng Dụng Kiến Thức Về Đồng Vị Trong Ngành Xe Tải
Kiến thức về đồng vị không chỉ hữu ích trong lĩnh vực hóa học mà còn có ứng dụng quan trọng trong ngành công nghiệp xe tải. Cụ thể, nó giúp chúng ta hiểu rõ hơn về thành phần và tính chất của các vật liệu chế tạo xe.
4.1. Nghiên Cứu Độ Bền Vật Liệu
Các nhà khoa học có thể sử dụng đồng vị phóng xạ để theo dõi sự mài mòn và ăn mòn của các bộ phận xe tải. Bằng cách thêm một lượng nhỏ đồng vị phóng xạ vào vật liệu, họ có thể đo lượng vật liệu bị mất đi theo thời gian, từ đó đánh giá độ bền của vật liệu.
4.2. Kiểm Tra Chất Lượng Sản Phẩm
Đồng vị cũng có thể được sử dụng để kiểm tra chất lượng của các bộ phận xe tải. Ví dụ, bằng cách chiếu xạ một bộ phận bằng neutron, các nhà sản xuất có thể phát hiện các khuyết tật bên trong mà không cần phải phá hủy bộ phận đó.
4.3. Phát Triển Vật Liệu Mới
Hiểu rõ về cấu trúc và tính chất của các đồng vị giúp các nhà khoa học phát triển các vật liệu mới với độ bền và hiệu suất cao hơn. Điều này có thể dẫn đến việc tạo ra các loại xe tải nhẹ hơn, tiết kiệm nhiên liệu hơn và có tuổi thọ cao hơn.
5. Tại Sao Nên Tìm Hiểu Về Xe Tải Tại XETAIMYDINH.EDU.VN?
Nếu bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình, Hà Nội, thì Xe Tải Mỹ Đình là địa chỉ không thể bỏ qua. Chúng tôi cung cấp:
- Thông tin chi tiết và cập nhật về các loại xe tải có sẵn.
- So sánh giá cả và thông số kỹ thuật giữa các dòng xe.
- Tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách của bạn.
- Giải đáp các thắc mắc liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải.
- Thông tin về các dịch vụ sửa chữa xe tải uy tín trong khu vực.
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
Hotline: 0247 309 9988.
Trang web: XETAIMYDINH.EDU.VN.
6. Lời Kêu Gọi Hành Động (CTA)
Bạn đang gặp khó khăn trong việc lựa chọn chiếc xe tải phù hợp? Bạn lo lắng về chi phí vận hành và bảo trì xe? Hãy truy cập ngay XETAIMYDINH.EDU.VN để được tư vấn và giải đáp mọi thắc mắc về xe tải ở Mỹ Đình. Chúng tôi cam kết mang đến cho bạn những thông tin chính xác và hữu ích nhất, giúp bạn đưa ra quyết định đúng đắn nhất.
7. FAQ – Các Câu Hỏi Thường Gặp
1. Hạt nhân nguyên tử của các nguyên tố đồng vị luôn có cùng yếu tố nào?
Hạt nhân nguyên tử của các nguyên tố đồng vị luôn có cùng số lượng proton.
2. Đồng vị là gì?
Đồng vị là các dạng khác nhau của cùng một nguyên tố hóa học, có cùng số lượng proton nhưng khác nhau về số lượng neutron.
3. Nguyên tử khối trung bình là gì?
Nguyên tử khối trung bình là giá trị trung bình của nguyên tử khối của tất cả các đồng vị của một nguyên tố, được tính dựa trên tỷ lệ phần trăm của mỗi đồng vị trong tự nhiên.
4. Làm thế nào để tính phần trăm đồng vị của một nguyên tố?
Để tính phần trăm đồng vị, bạn sử dụng công thức: M = (x₁.M₁ + x₂.M₂ + … + xₙ.Mₙ) / 100, trong đó M là nguyên tử khối trung bình, M₁, M₂, …, Mₙ là nguyên tử khối của các đồng vị, và x₁, x₂, …, xₙ là tỷ lệ phần trăm của các đồng vị.
5. Đồng vị phóng xạ là gì?
Đồng vị phóng xạ là các đồng vị không ổn định và tự phân rã, phát ra các hạt và năng lượng.
6. Ứng dụng của đồng vị trong ngành xe tải là gì?
Đồng vị được sử dụng để nghiên cứu độ bền vật liệu, kiểm tra chất lượng sản phẩm và phát triển vật liệu mới cho xe tải.
7. Tại sao nên tìm hiểu về xe tải tại XETAIMYDINH.EDU.VN?
Vì XETAIMYDINH.EDU.VN cung cấp thông tin chi tiết, cập nhật, tư vấn chuyên nghiệp và dịch vụ sửa chữa xe tải uy tín.
8. Địa chỉ và hotline của Xe Tải Mỹ Đình là gì?
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội. Hotline: 0247 309 9988.
9. Làm thế nào để liên hệ với Xe Tải Mỹ Đình để được tư vấn?
Bạn có thể truy cập trang web XETAIMYDINH.EDU.VN hoặc gọi hotline 0247 309 9988 để được tư vấn.
10. Xe Tải Mỹ Đình có cung cấp dịch vụ sửa chữa xe tải không?
Có, Xe Tải Mỹ Đình cung cấp thông tin về các dịch vụ sửa chữa xe tải uy tín trong khu vực.