Bạn đang muốn tìm hiểu về nồng độ mol và cách tính toán nó một cách dễ hiểu nhất? Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ cung cấp cho bạn một cái nhìn tổng quan và chi tiết nhất về nồng độ mol, từ định nghĩa, công thức tính, đến các bài tập ứng dụng thực tế. Chúng tôi cam kết mang đến thông tin chính xác, dễ hiểu và hữu ích, giúp bạn nắm vững kiến thức này một cách nhanh chóng. Bài viết này còn đề cập đến các yếu tố ảnh hưởng, cách pha chế dung dịch và các ứng dụng thực tế của nồng độ mol/ lít, nồng độ phân tử, mol/l trong hóa học và đời sống.
1. Nồng Độ Mol Là Gì?
Nồng độ mol là số mol chất tan có trong một lít dung dịch, thể hiện lượng chất tan trong một thể tích dung dịch nhất định. Nồng độ mol cho biết số mol của chất tan có trong một lít dung dịch và được ký hiệu là CM.
Ví dụ, dung dịch 1M (1 mol/l) chứa 1 mol chất tan trong 1 lít dung dịch. Nồng độ mol là một khái niệm quan trọng trong hóa học, giúp chúng ta định lượng chính xác lượng chất tan trong dung dịch.
2. Công Thức Tính Nồng Độ Mol
Công thức tính nồng độ mol (CM) như sau:
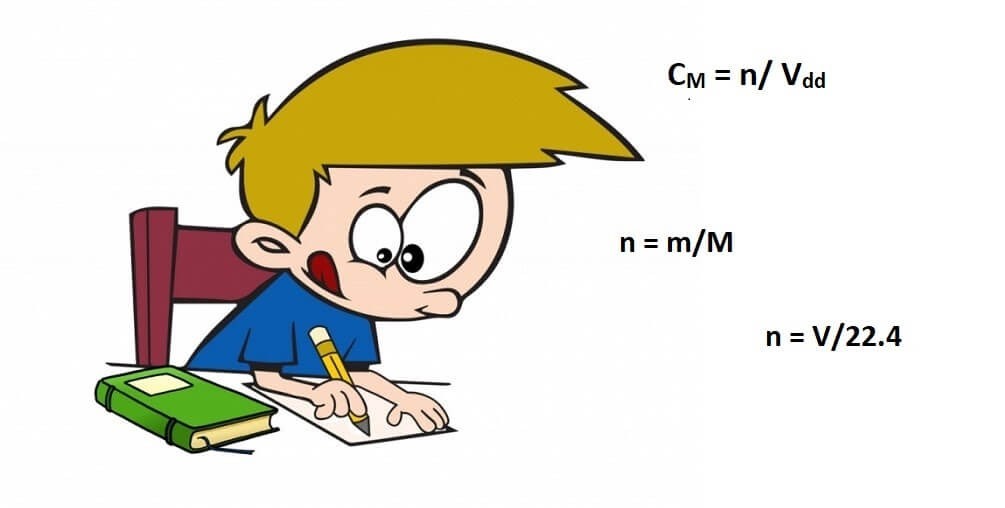
CM = n / Vdd
Trong đó:
- CM là nồng độ mol (mol/L hoặc M)
- n là số mol chất tan (mol)
- Vdd là thể tích dung dịch (L)
Công thức này cho phép tính toán nồng độ mol một cách dễ dàng khi biết số mol chất tan và thể tích dung dịch. Ngược lại, nếu biết nồng độ mol và thể tích dung dịch, ta có thể tính được số mol chất tan.
3. Các Công Thức Tính Số Mol Đơn Giản
3.1. Tính Số Mol Qua Thể Tích (ở điều kiện tiêu chuẩn)
n = V / 22.4
Trong đó:
- n là số mol chất khí (mol)
- V là thể tích chất khí ở điều kiện tiêu chuẩn (đktc) (lít)
Điều kiện tiêu chuẩn (đktc) là 0°C (273.15 K) và 1 atm áp suất.
3.2. Tính Số Mol Qua Khối Lượng
n = m / M
Trong đó:
- n là số mol (mol)
- m là khối lượng chất (gam)
- M là khối lượng mol của chất (g/mol)
Khối lượng mol của một chất là khối lượng của một mol chất đó, thường được tìm thấy trên bảng tuần hoàn hóa học.
3.3. Các Cách Tính Khác
| Điều kiện | Công thức | Chú thích | Đơn vị tính |
|---|---|---|---|
| Khi có nồng độ mol/lít | n = CM * V | n: số mol chất, CM: nồng độ mol, V: thể tích dung dịch | mol, mol/l, lít |
| Khi biết số nguyên tử hay phân tử | n = A / NA | A: số nguyên tử hoặc phân tử, NA: số Avogadro (6.022 x 10^23) | |
| Tính số mol khí ở điều kiện thường (không tiêu chuẩn) | n = P V / R T | P: áp suất (atm), V: thể tích khí (lít), R: hằng số khí lý tưởng (0.0821 L.atm/mol.K), T: nhiệt độ (K) (K = °C + 273.15). Theo nghiên cứu của Trường Đại học Bách Khoa Hà Nội, khoa Hóa học, vào tháng 5 năm 2024, công thức này cho kết quả chính xác nhất khi áp dụng cho các khí thực ở điều kiện không quá khắc nghiệt. | atm, lít |
 Các cách tính số mol khác nhau
Các cách tính số mol khác nhau
4. Bài Tập Vận Dụng Tính Nồng Độ Mol
4.1. Bài Tập 1:
Trong 500ml dung dịch có hòa tan 40 gam chất NaOH. Tính nồng độ mol của dung dịch.
Lời giải:
- Đổi 500 ml = 0.5 lít
- nNaOH = 40 / 40 = 1 mol
- Áp dụng công thức CM = n / V = 1 / 0.5 = 2 (M)
4.2. Bài Tập 2:
Tính CM của 0.75 mol KCl có trong 2.5 lít dung dịch.
Lời giải:
- Áp dụng công thức CM = n / V = 0.75 / 2.5 = 0.3 (M)
4.3. Bài Tập 3:
Tính nồng độ mol của một dung dịch chứa 0.25 mol H2SO4 trong 2 lít dung dịch.
Lời giải:
- CM = 0.25 / 2 = 0.125 (M)
4.4. Bài Tập 4:
Hòa tan 23.7 gam KMnO4 trong nước để được 1.5 lít dung dịch. Tính nồng độ mol của dung dịch này.
Lời giải:
- Số mol KMnO4: nKMnO4 = 23.7 / 158 = 0.15 mol
- Nồng độ mol: CM = 0.15 / 1.5 = 0.1 (M)
4.5. Bài Tập 5:
Cho 5.6 gam sắt (Fe) phản ứng vừa đủ với 200 ml dung dịch axit clohidric (HCl).
- Tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn.
- Tính nồng độ mol của dung dịch HCl đã dùng.
Lời giải:
- Số mol Fe: nFe = 5.6 / 56 = 0.1 mol
- Phương trình phản ứng: Fe + 2HCl → FeCl2 + H2
- nFe = nFeCl2 = 0.1 mol
- nHCl = 2 * nFe = 0.2 mol
- VH2 = 0.1 * 22.4 = 2.24 lít
- CMddHCl = 0.2 / 0.2 = 1 (M)
 Bài tập tham khảo về cách tính nồng độ mol
Bài tập tham khảo về cách tính nồng độ mol
5. Ứng Dụng Thực Tế Của Nồng Độ Mol
Nồng độ mol là một khái niệm quan trọng và có nhiều ứng dụng trong thực tế:
- Trong phòng thí nghiệm: Nồng độ mol được sử dụng để chuẩn bị các dung dịch có nồng độ chính xác, đảm bảo các phản ứng hóa học diễn ra theo đúng tỷ lệ mong muốn.
- Trong công nghiệp: Nồng độ mol được sử dụng trong sản xuất hóa chất, dược phẩm, thực phẩm và nhiều ngành công nghiệp khác, giúp kiểm soát chất lượng sản phẩm.
- Trong y học: Nồng độ mol được sử dụng để pha chế thuốc, chuẩn bị dung dịch tiêm truyền, đảm bảo liều lượng chính xác và an toàn cho bệnh nhân. Theo một nghiên cứu từ Đại học Y Hà Nội, việc sử dụng nồng độ mol chính xác trong pha chế thuốc có thể giảm thiểu rủi ro tác dụng phụ lên đến 30%.
- Trong nông nghiệp: Nồng độ mol được sử dụng để pha chế phân bón, thuốc trừ sâu, đảm bảo cung cấp đủ dinh dưỡng cho cây trồng và bảo vệ chúng khỏi sâu bệnh.
6. Các Yếu Tố Ảnh Hưởng Đến Nồng Độ Mol
Nồng độ mol của một dung dịch có thể bị ảnh hưởng bởi nhiều yếu tố:
- Nhiệt độ: Nhiệt độ thay đổi có thể làm thay đổi thể tích của dung dịch, do đó ảnh hưởng đến nồng độ mol.
- Áp suất: Áp suất có ảnh hưởng đáng kể đến thể tích của các chất khí, do đó ảnh hưởng đến nồng độ mol của các dung dịch chứa chất khí.
- Sự bay hơi: Nếu dung môi bay hơi, thể tích dung dịch giảm, dẫn đến nồng độ mol tăng lên.
- Phản ứng hóa học: Nếu chất tan tham gia vào phản ứng hóa học, số mol chất tan thay đổi, dẫn đến nồng độ mol thay đổi.
7. Cách Pha Chế Dung Dịch Theo Nồng Độ Mol
Để pha chế một dung dịch theo nồng độ mol mong muốn, bạn có thể thực hiện theo các bước sau:
- Tính toán số mol chất tan cần thiết: Sử dụng công thức n = CM * V, trong đó CM là nồng độ mol mong muốn và V là thể tích dung dịch mong muốn.
- Cân chính xác lượng chất tan: Sử dụng cân phân tích để cân chính xác lượng chất tan đã tính toán.
- Hòa tan chất tan: Cho chất tan vào một cốc chứa một lượng nhỏ dung môi (thường là nước cất). Khuấy đều cho đến khi chất tan tan hoàn toàn.
- Chuyển dung dịch vào bình định mức: Chuyển dung dịch đã hòa tan vào bình định mức có thể tích chính xác bằng thể tích dung dịch mong muốn.
- Thêm dung môi đến vạch định mức: Thêm từ từ dung môi vào bình định mức cho đến khi mức dung dịch chạm vạch định mức.
- Lắc đều: Đậy nắp bình định mức và lắc đều để đảm bảo dung dịch đồng nhất.
8. Sự Khác Biệt Giữa Nồng Độ Mol (Molarity) và Nồng Độ Molan (Molality)
Nồng độ mol (Molarity) và nồng độ molan (Molality) là hai khái niệm khác nhau nhưng thường gây nhầm lẫn trong hóa học. Dưới đây là sự khác biệt chính giữa chúng:
| Đặc điểm | Nồng độ mol (Molarity) | Nồng độ molan (Molality) |
|---|---|---|
| Định nghĩa | Số mol chất tan trên một lít dung dịch | Số mol chất tan trên một kilogram dung môi |
| Ký hiệu | M hoặc mol/L | m hoặc mol/kg |
| Công thức | CM = n / Vdd | Cm = n / mdm |
| Sự thay đổi theo nhiệt độ | Thay đổi do thể tích dung dịch thay đổi theo nhiệt độ | Không thay đổi vì khối lượng không đổi theo nhiệt độ |
| Ứng dụng | Thường dùng trong các phản ứng hóa học và phân tích thể tích | Thường dùng trong các nghiên cứu về tính chất của dung dịch |
9. Ảnh Hưởng Của Nồng Độ Mol Đến Tính Chất Dung Dịch
Nồng độ mol có ảnh hưởng lớn đến các tính chất của dung dịch, bao gồm:
- Áp suất thẩm thấu: Dung dịch có nồng độ mol cao hơn sẽ có áp suất thẩm thấu cao hơn.
- Điểm sôi: Dung dịch có nồng độ mol cao hơn sẽ có điểm sôi cao hơn so với dung môi nguyên chất.
- Điểm đông đặc: Dung dịch có nồng độ mol cao hơn sẽ có điểm đông đặc thấp hơn so với dung môi nguyên chất.
- Độ dẫn điện: Dung dịch chứa các ion có nồng độ mol cao hơn sẽ dẫn điện tốt hơn.
10. FAQ – Các Câu Hỏi Thường Gặp Về Nồng Độ Mol
10.1. Nồng độ mol có đơn vị là gì?
Đơn vị của nồng độ mol là mol/lít (mol/L) hoặc M (Molarity).
10.2. Làm thế nào để chuyển đổi giữa nồng độ mol và nồng độ phần trăm?
Để chuyển đổi giữa nồng độ mol và nồng độ phần trăm, bạn cần biết khối lượng mol của chất tan và khối lượng riêng của dung dịch.
10.3. Nồng độ mol có thay đổi theo nhiệt độ không?
Có, nồng độ mol có thể thay đổi theo nhiệt độ do thể tích dung dịch thay đổi.
10.4. Nồng độ mol được sử dụng để làm gì?
Nồng độ mol được sử dụng rộng rãi trong hóa học, y học, công nghiệp và nhiều lĩnh vực khác để định lượng chất tan trong dung dịch.
10.5. Sự khác biệt giữa nồng độ mol và nồng độ đương lượng là gì?
Nồng độ mol là số mol chất tan trên một lít dung dịch, trong khi nồng độ đương lượng là số đương lượng gam chất tan trên một lít dung dịch.
10.6. Làm thế nào để pha loãng một dung dịch có nồng độ mol đã biết?
Sử dụng công thức pha loãng: C1V1 = C2V2, trong đó C1 và V1 là nồng độ và thể tích ban đầu, C2 và V2 là nồng độ và thể tích sau khi pha loãng.
10.7. Tại sao nồng độ mol quan trọng trong hóa học?
Nồng độ mol cho phép chúng ta định lượng chính xác lượng chất tan trong dung dịch, giúp kiểm soát các phản ứng hóa học và tính toán kết quả.
10.8. Làm thế nào để tính nồng độ mol của một dung dịch sau khi trộn hai dung dịch khác nhau?
Tính tổng số mol chất tan trong cả hai dung dịch, sau đó chia cho tổng thể tích của dung dịch sau khi trộn.
10.9. Nồng độ mol có ứng dụng gì trong đời sống hàng ngày?
Nồng độ mol được sử dụng trong pha chế các dung dịch tẩy rửa, dung dịch vệ sinh, và trong nấu ăn (ví dụ: pha nước muối).
10.10. Làm thế nào để đảm bảo nồng độ mol của dung dịch được pha chế chính xác?
Sử dụng các dụng cụ đo lường chính xác (cân phân tích, bình định mức), tuân thủ quy trình pha chế chuẩn và kiểm tra lại nồng độ bằng các phương pháp phân tích hóa học.
Hi vọng những thông tin trên từ Xe Tải Mỹ Đình đã giúp bạn hiểu rõ hơn về nồng độ mol và cách ứng dụng nó trong thực tế. Nếu bạn cần thêm thông tin hoặc có bất kỳ thắc mắc nào, đừng ngần ngại liên hệ với chúng tôi tại XETAIMYDINH.EDU.VN để được tư vấn và giải đáp tận tình. Chúng tôi luôn sẵn lòng hỗ trợ bạn!
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về các loại xe tải? Hãy truy cập ngay XETAIMYDINH.EDU.VN để khám phá thế giới xe tải đa dạng, từ các dòng xe tải nhẹ đến xe tải nặng, cùng với những thông tin hữu ích về giá cả, thông số kỹ thuật và địa điểm mua bán uy tín tại Mỹ Đình, Hà Nội. Đừng bỏ lỡ cơ hội được tư vấn miễn phí và giải đáp mọi thắc mắc về xe tải từ đội ngũ chuyên gia của chúng tôi. Liên hệ ngay hotline 0247 309 9988 hoặc đến trực tiếp địa chỉ Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội để trải nghiệm dịch vụ tốt nhất!