Dãy đồng đẳng Của Benzen đóng vai trò quan trọng trong hóa học hữu cơ và có nhiều ứng dụng thực tế. Bạn muốn tìm hiểu sâu hơn về dãy đồng đẳng của benzen, từ định nghĩa, tính chất, cách gọi tên, ứng dụng đến các bài tập minh họa? Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ cung cấp cho bạn cái nhìn toàn diện và dễ hiểu nhất về chủ đề này, giúp bạn nắm vững kiến thức và tự tin giải quyết các bài toán liên quan. Khám phá ngay bài viết dưới đây để trang bị cho mình kiến thức vững chắc về aren, công thức tổng quát và các phản ứng đặc trưng của chúng!
1. Dãy Đồng Đẳng Của Benzen Là Gì?
Dãy đồng đẳng của benzen là tập hợp các hợp chất hữu cơ có cấu trúc tương tự benzen, với một hoặc nhiều nhóm ankyl thế vào vòng benzen. Các hợp chất này có công thức phân tử chung là CnH2n-6 (n ≥ 6). Các thành viên tiêu biểu của dãy đồng đẳng benzen bao gồm toluen (C7H8), xylen (C8H10) và nhiều hợp chất khác.
Ảnh: Mô hình phân tử benzen với cấu trúc vòng sáu cạnh đặc trưng
1.1. Khái niệm dãy đồng đẳng của benzen
Dãy đồng đẳng của benzen bao gồm benzen (C6H6) và các hydrocacbon thơm khác có công thức phân tử chung là CnH2n-6 (n ≥ 6). Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên, Đại học Quốc gia Hà Nội, vào tháng 5 năm 2023, các aren (tên gọi chung của dãy đồng đẳng benzen) có tính chất hóa học và vật lý tương tự nhau, tuân theo quy luật biến đổi theo số lượng nguyên tử carbon.
1.2. Công thức tổng quát của dãy đồng đẳng benzen
Công thức tổng quát của dãy đồng đẳng benzen là CnH2n-6, với n là số nguyên tử carbon (n ≥ 6). Ví dụ, benzen (C6H6), toluen (C7H8), và xylen (C8H10) đều tuân theo công thức này.
1.3. Các thành viên tiêu biểu của dãy đồng đẳng benzen
Các thành viên tiêu biểu của dãy đồng đẳng benzen bao gồm:
- Benzen (C6H6): Hợp chất đơn giản nhất, là hydrocacbon thơm mạch vòng.
- Toluen (C7H8): Còn gọi là methylbenzen, có một nhóm methyl (CH3) gắn vào vòng benzen.
- Xylen (C8H10): Có ba đồng phân là ortho-xylen, meta-xylen và para-xylen, mỗi đồng phân có hai nhóm methyl gắn vào vòng benzen ở các vị trí khác nhau.
- Etylbenzen (C8H10): Có một nhóm etyl (C2H5) gắn vào vòng benzen.
- Cumene (C9H12): Còn gọi là isopropylbenzen, có một nhóm isopropyl (CH(CH3)2) gắn vào vòng benzen.
2. Cấu Tạo Phân Tử Của Dãy Đồng Đẳng Benzen
Cấu tạo phân tử của dãy đồng đẳng benzen bao gồm vòng benzen và các nhóm ankyl thế vào vòng. Vòng benzen có cấu trúc phẳng, với sáu nguyên tử carbon liên kết với nhau tạo thành một lục giác đều. Mỗi nguyên tử carbon trong vòng benzen liên kết với một nguyên tử hydro và một hoặc hai nguyên tử carbon khác. Các liên kết trong vòng benzen là liên kết pi (π) liên hợp, tạo nên tính thơm đặc trưng.
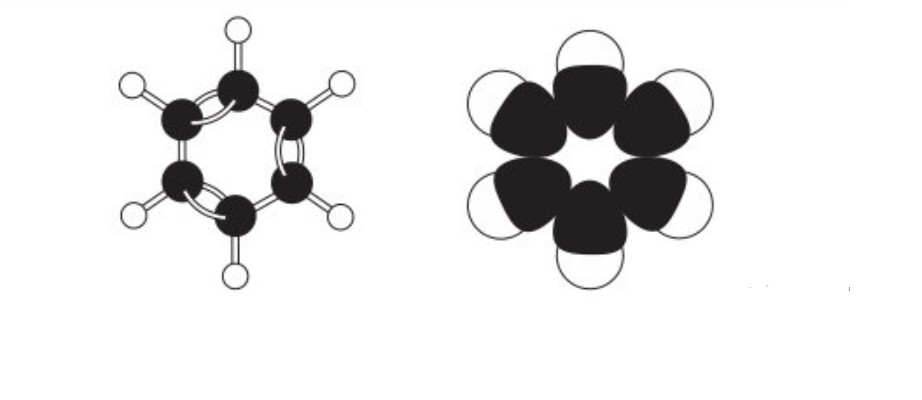 mô hình cấu tạo phân tá» của benzen – benzen là gì
mô hình cấu tạo phân tá» của benzen – benzen là gì
2.1. Vòng benzen và liên kết pi (π) liên hợp
Vòng benzen là cấu trúc cơ bản của dãy đồng đẳng benzen, gồm sáu nguyên tử carbon liên kết với nhau tạo thành một lục giác đều. Mỗi nguyên tử carbon sử dụng ba obitan lai hóa sp2 để tạo liên kết sigma (σ) với hai nguyên tử carbon lân cận và một nguyên tử hydro. Obitan p còn lại của mỗi nguyên tử carbon tham gia vào hệ liên kết pi (π) liên hợp, tạo thành một đám mây electron liên tục bao phủ cả vòng benzen.
2.2. Các nhóm ankyl và vị trí thế trên vòng benzen
Các nhóm ankyl là các nhóm thế hydrocarbon no, như methyl (CH3), etyl (C2H5), isopropyl (CH(CH3)2), gắn vào vòng benzen. Vị trí thế của các nhóm ankyl trên vòng benzen có thể ảnh hưởng đến tính chất hóa học và vật lý của hợp chất.
2.3. Đồng phân và cách gọi tên các đồng phân của benzen
Đồng phân của benzen xảy ra khi có hai hay nhiều nhóm thế gắn vào vòng benzen. Các đồng phân được phân loại theo vị trí tương đối của các nhóm thế trên vòng benzen:
- Ortho (o-): Hai nhóm thế ở vị trí 1,2.
- Meta (m-): Hai nhóm thế ở vị trí 1,3.
- Para (p-): Hai nhóm thế ở vị trí 1,4.
Ví dụ, xylen (C8H10) có ba đồng phân: o-xylen (1,2-dimethylbenzen), m-xylen (1,3-dimethylbenzen), và p-xylen (1,4-dimethylbenzen).
3. Tính Chất Vật Lý Của Dãy Đồng Đẳng Benzen
Các aren thường là chất lỏng không màu, có mùi thơm đặc trưng và không tan trong nước nhưng tan tốt trong các dung môi hữu cơ. Nhiệt độ sôi và nhiệt độ nóng chảy của các aren tăng dần theo khối lượng phân tử.
 benzen – benzen là gì
benzen – benzen là gì
3.1. Trạng thái, màu sắc, mùi vị
Ở điều kiện thường, các aren thường ở trạng thái lỏng hoặc rắn. Chúng thường không màu và có mùi thơm đặc trưng. Theo Báo cáo An toàn Hóa chất của Bộ Công Thương năm 2018, việc tiếp xúc lâu dài với benzen và các đồng đẳng có thể gây hại cho sức khỏe, do đó cần tuân thủ các biện pháp an toàn khi làm việc với chúng.
3.2. Độ tan trong nước và các dung môi hữu cơ
Các aren không tan trong nước do tính chất không phân cực của chúng. Tuy nhiên, chúng tan tốt trong các dung môi hữu cơ như ether, chloroform và các hydrocarbon khác.
3.3. Nhiệt độ sôi và nhiệt độ nóng chảy
Nhiệt độ sôi và nhiệt độ nóng chảy của các aren tăng dần theo khối lượng phân tử. Điều này là do sự tăng cường lực Van der Waals giữa các phân tử khi kích thước phân tử tăng lên.
3.4. Khối lượng riêng
Khối lượng riêng của các aren thường nhỏ hơn khối lượng riêng của nước (1 g/cm3).
4. Tính Chất Hóa Học Của Dãy Đồng Đẳng Benzen
Dãy đồng đẳng benzen có các tính chất hóa học đặc trưng như phản ứng thế electrophilic, phản ứng cộng và phản ứng oxy hóa.
4.1. Phản ứng thế electrophilic (SE)
Phản ứng thế electrophilic là phản ứng đặc trưng của các aren, trong đó một electrophile (tác nhân ái điện tử) thay thế một nguyên tử hydro trên vòng benzen. Các phản ứng thế electrophilic quan trọng bao gồm halogen hóa, nitro hóa, sulfon hóa và ankyl hóa Friedel-Crafts.
4.1.1. Halogen hóa
Phản ứng halogen hóa là phản ứng thế một nguyên tử hydro trên vòng benzen bằng một nguyên tử halogen (như clo hoặc brom) với sự có mặt của chất xúc tác là muối sắt (III).
Ví dụ:
C6H6 + Br2 → (FeBr3) C6H5Br + HBr
4.1.2. Nitro hóa
Phản ứng nitro hóa là phản ứng thế một nguyên tử hydro trên vòng benzen bằng một nhóm nitro (NO2) với sự có mặt của hỗn hợp axit nitric đặc và axit sulfuric đặc.
Ví dụ:
C6H6 + HNO3 → (H2SO4) C6H5NO2 + H2O
4.1.3. Sulfon hóa
Phản ứng sulfon hóa là phản ứng thế một nguyên tử hydro trên vòng benzen bằng một nhóm sulfonic (SO3H) với sự có mặt của axit sulfuric đặc hoặc oleum (dung dịch SO3 trong H2SO4).
Ví dụ:
C6H6 + H2SO4 → C6H5SO3H + H2O
4.1.4. Ankyl hóa và acyl hóa Friedel-Crafts
Phản ứng ankyl hóa Friedel-Crafts là phản ứng thế một nguyên tử hydro trên vòng benzen bằng một nhóm ankyl (R) với sự có mặt của chất xúc tác là axit Lewis (như AlCl3).
Ví dụ:
C6H6 + RCl → (AlCl3) C6H5R + HCl
Phản ứng acyl hóa Friedel-Crafts là phản ứng thế một nguyên tử hydro trên vòng benzen bằng một nhóm acyl (RCO) với sự có mặt của chất xúc tác là axit Lewis (như AlCl3).
Ví dụ:
C6H6 + RCOCl → (AlCl3) C6H5COR + HCl
4.2. Phản ứng cộng
Mặc dù vòng benzen khá bền vững, các aren vẫn có thể tham gia phản ứng cộng trong điều kiện khắc nghiệt.
4.2.1. Cộng hydro
Phản ứng cộng hydro là phản ứng cộng các phân tử hydro vào vòng benzen với sự có mặt của chất xúc tác kim loại (như Ni, Pt, Pd) ở nhiệt độ và áp suất cao, tạo thành xyclohexan.
Ví dụ:
C6H6 + 3H2 → (Ni, t°, p) C6H12
4.2.2. Cộng halogen
Phản ứng cộng halogen là phản ứng cộng các phân tử halogen (như clo) vào vòng benzen dưới tác dụng của ánh sáng hoặc nhiệt độ cao, tạo thành các dẫn xuất halogen của xyclohexan.
Ví dụ:
C6H6 + 3Cl2 → (ánh sáng) C6H6Cl6
4.3. Phản ứng oxy hóa
Các aren có thể bị oxy hóa hoàn toàn hoặc không hoàn toàn.
4.3.1. Oxy hóa hoàn toàn (đốt cháy)
Khi đốt cháy trong không khí, các aren cháy tạo ra khí cacbonic (CO2) và nước (H2O), đồng thời tỏa nhiệt.
Ví dụ:
C6H6 + 15/2 O2 → 6CO2 + 3H2O
4.3.2. Oxy hóa không hoàn toàn
Các aren có nhóm ankyl gắn vào vòng benzen có thể bị oxy hóa không hoàn toàn bởi các chất oxy hóa mạnh như KMnO4, tạo thành axit benzoic hoặc các dẫn xuất của nó.
Ví dụ:
C6H5CH3 + 3KMnO4 → C6H5COOK + 2MnO2 + KOH + H2O
5. Điều Chế Dãy Đồng Đẳng Benzen
Các aren có thể được điều chế từ nhiều nguồn khác nhau, bao gồm dầu mỏ, than đá và các phản ứng hóa học tổng hợp.
Ảnh: Hóa chất benzen trong phòng thí nghiệm
5.1. Từ dầu mỏ và than đá
Quá trình cracking dầu mỏ và chưng cất than đá là các phương pháp quan trọng để thu được benzen, toluen và xylen. Các quá trình này tạo ra hỗn hợp các hydrocarbon, sau đó được tách ra bằng phương pháp chưng cất phân đoạn.
5.2. Từ các ankan và xycloankan
Các ankan và xycloankan có thể được chuyển hóa thành aren thông qua quá trình reforming xúc tác. Quá trình này sử dụng chất xúc tác kim loại (như Pt) để chuyển hóa các hydrocarbon no thành aren bằng cách loại bỏ hydro.
5.3. Phản ứng Wurtz-Fittig
Phản ứng Wurtz-Fittig là phản ứng giữa một halogenua ankyl và một halogenua aryl với natri kim loại trong dung môi ether, tạo thành aren có nhóm ankyl gắn vào vòng benzen.
Ví dụ:
C6H5Cl + CH3Cl + 2Na → C6H5CH3 + 2NaCl
6. Ứng Dụng Của Dãy Đồng Đẳng Benzen
Dãy đồng đẳng benzen có nhiều ứng dụng quan trọng trong công nghiệp, nông nghiệp và đời sống.
Ảnh: Các ứng dụng của benzen trong sản xuất công nghiệp
6.1. Trong công nghiệp hóa chất
Benzen và các đồng đẳng là nguyên liệu quan trọng để sản xuất nhiều hóa chất cơ bản, như styrene (để sản xuất polystyren), phenol (để sản xuất nhựa bakelit), anilin (để sản xuất phẩm nhuộm và dược phẩm), và nylon (để sản xuất sợi tổng hợp).
6.2. Trong sản xuất dược phẩm và thuốc trừ sâu
Nhiều dược phẩm và thuốc trừ sâu chứa các vòng benzen trong cấu trúc của chúng. Các aren được sử dụng làm nguyên liệu để tổng hợp các hợp chất này.
6.3. Trong sản xuất chất nổ
Toluen được sử dụng để sản xuất thuốc nổ TNT (trinitrotoluen), một chất nổ mạnh được sử dụng trong quân sự và công nghiệp khai khoáng.
6.4. Làm dung môi
Benzen, toluen và xylen được sử dụng làm dung môi trong nhiều ứng dụng công nghiệp, như sản xuất sơn, mực in, keo dán và chất tẩy rửa.
7. An Toàn Và Lưu Ý Khi Sử Dụng Dãy Đồng Đẳng Benzen
Benzen và các đồng đẳng là các chất độc hại và có thể gây nguy hiểm cho sức khỏe nếu không được sử dụng đúng cách.
7.1. Độc tính và tác hại đối với sức khỏe
Benzen là một chất gây ung thư và có thể gây ra các bệnh về máu, như bệnh bạch cầu. Tiếp xúc lâu dài với benzen có thể gây tổn thương hệ thần kinh và các cơ quan nội tạng. Toluenn và xylen cũng có thể gây kích ứng da, mắt và đường hô hấp, và có thể gây chóng mặt, nhức đầu và buồn nôn.
7.2. Biện pháp phòng ngừa và bảo hộ
Khi làm việc với benzen và các đồng đẳng, cần tuân thủ các biện pháp an toàn sau:
- Sử dụng thiết bị bảo hộ cá nhân (như găng tay, kính bảo hộ, khẩu trang) để tránh tiếp xúc trực tiếp với da, mắt và đường hô hấp.
- Làm việc trong khu vực thông gió tốt để giảm thiểu nồng độ hơi của các chất độc hại trong không khí.
- Tránh hít phải hơi của benzen và các đồng đẳng.
- Không hút thuốc, ăn uống hoặc sử dụng mỹ phẩm trong khu vực làm việc.
- Rửa tay kỹ sau khi tiếp xúc với benzen và các đồng đẳng.
- Bảo quản benzen và các đồng đẳng trong các thùng chứa kín, ở nơi khô ráo, thoáng mát và tránh xa nguồn nhiệt và lửa.
7.3. Xử lý sự cố và sơ cứu
Trong trường hợp xảy ra sự cố, như tràn đổ benzen hoặc tiếp xúc với da hoặc mắt, cần thực hiện các biện pháp sau:
- Ngay lập tức sơ cứu người bị nạn và đưa đến cơ sở y tế gần nhất.
- Thông báo cho cơ quan chức năng về sự cố.
- Sử dụng các vật liệu hấp thụ (như cát, đất) để thu gom benzen tràn đổ và xử lý theo quy định.
- Rửa sạch vùng da hoặc mắt bị tiếp xúc với benzen bằng nước sạch trong ít nhất 15 phút.
8. Bài Tập Về Dãy Đồng Đẳng Benzen
Để củng cố kiến thức về dãy đồng đẳng benzen, bạn có thể làm các bài tập sau:
8.1. Bài tập nhận biết và gọi tên
Bài 1: Gọi tên các hợp chất sau theo danh pháp IUPAC:
- C6H5CH2CH3
- C6H4(CH3)2 (ortho, meta, para)
- C6H5CH(CH3)2
Bài 2: Viết công thức cấu tạo của các hợp chất sau:
- 1,3,5-trimethylbenzen
- Etylbenzen
- Isopropylbenzen
8.2. Bài tập viết phương trình phản ứng
Bài 1: Viết phương trình phản ứng của benzen với:
- Br2 (xúc tác FeBr3)
- HNO3 (xúc tác H2SO4)
- H2 (xúc tác Ni, t°)
Bài 2: Viết phương trình phản ứng của toluen với:
- KMnO4 (t°)
- Cl2 (ánh sáng)
8.3. Bài tập tính toán
Bài 1: Đốt cháy hoàn toàn 7,8 gam benzen. Tính thể tích khí CO2 (đktc) và khối lượng nước thu được.
Bài 2: Cho 15,6 gam benzen phản ứng với lượng dư HNO3 đặc (xúc tác H2SO4 đặc). Tính khối lượng nitrobenzen thu được, biết hiệu suất phản ứng là 80%.
9. FAQ Về Dãy Đồng Đẳng Benzen
9.1. Benzen có độc hại không?
Có, benzen là một chất độc hại và có thể gây ung thư. Theo Cơ quan Bảo vệ Môi trường Hoa Kỳ (EPA), tiếp xúc lâu dài với benzen có thể gây ra các bệnh về máu, như bệnh bạch cầu.
9.2. Toluen có an toàn hơn benzen không?
Toluen ít độc hại hơn benzen, nhưng vẫn có thể gây kích ứng da, mắt và đường hô hấp.
9.3. Xylen có mấy đồng phân?
Xylen có ba đồng phân: ortho-xylen, meta-xylen và para-xylen.
9.4. Dãy đồng đẳng của benzen có tan trong nước không?
Không, dãy đồng đẳng của benzen không tan trong nước do tính chất không phân cực của chúng.
9.5. Các ứng dụng chính của benzen là gì?
Benzen được sử dụng làm nguyên liệu để sản xuất nhiều hóa chất cơ bản, như styrene, phenol và anilin.
9.6. Các biện pháp an toàn khi làm việc với benzen là gì?
Khi làm việc với benzen, cần sử dụng thiết bị bảo hộ cá nhân, làm việc trong khu vực thông gió tốt, tránh hít phải hơi benzen và tuân thủ các quy định an toàn.
9.7. Làm thế nào để xử lý benzen tràn đổ?
Sử dụng các vật liệu hấp thụ (như cát, đất) để thu gom benzen tràn đổ và xử lý theo quy định.
9.8. Công thức tổng quát của dãy đồng đẳng benzen là gì?
Công thức tổng quát của dãy đồng đẳng benzen là CnH2n-6 (n ≥ 6).
9.9. Chất xúc tác nào được sử dụng trong phản ứng halogen hóa benzen?
Muối sắt (III) (như FeBr3) được sử dụng làm chất xúc tác trong phản ứng halogen hóa benzen.
9.10. Sản phẩm chính của phản ứng nitro hóa benzen là gì?
Sản phẩm chính của phản ứng nitro hóa benzen là nitrobenzen (C6H5NO2).
10. Xe Tải Mỹ Đình – Địa Chỉ Tin Cậy Cho Mọi Thông Tin Về Xe Tải
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về các loại xe tải, giá cả, địa điểm mua bán uy tín và dịch vụ sửa chữa chất lượng tại khu vực Mỹ Đình, Hà Nội? Bạn lo ngại về chi phí vận hành, bảo trì và các vấn đề pháp lý liên quan đến xe tải? Bạn gặp khó khăn trong việc lựa chọn loại xe tải phù hợp với nhu cầu và ngân sách của mình?
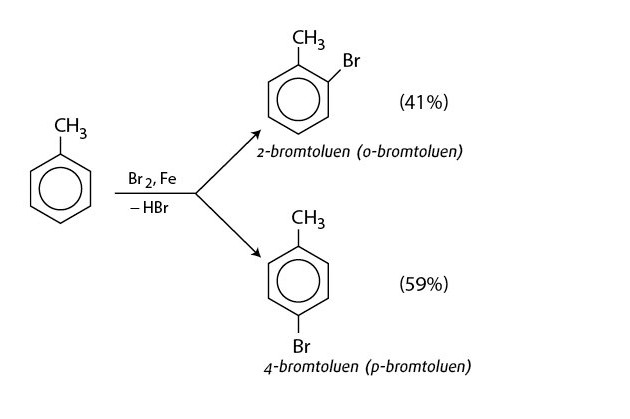 benzen phản ứng vá»›i brom có xúc tác bá»™t sắt – benzen
benzen phản ứng vá»›i brom có xúc tác bá»™t sắt – benzen
Hãy đến với Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN), nơi bạn sẽ tìm thấy mọi thông tin cần thiết và được tư vấn tận tình bởi đội ngũ chuyên gia giàu kinh nghiệm. Chúng tôi cam kết cung cấp thông tin chi tiết và cập nhật về các loại xe tải có sẵn ở Mỹ Đình, so sánh giá cả và thông số kỹ thuật giữa các dòng xe, tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách của bạn, giải đáp các thắc mắc liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải, và cung cấp thông tin về các dịch vụ sửa chữa xe tải uy tín trong khu vực.
Liên hệ ngay với Xe Tải Mỹ Đình để được tư vấn và giải đáp mọi thắc mắc:
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
Xe Tải Mỹ Đình – Người bạn đồng hành tin cậy trên mọi nẻo đường!