Chất điện li là gì và tại sao nó quan trọng trong hóa học? Bài viết này từ Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ cung cấp cho bạn một cái nhìn toàn diện về chất điện li, từ định nghĩa cơ bản đến phân loại và ứng dụng thực tế, giúp bạn hiểu rõ hơn về khái niệm này. Chúng ta sẽ cùng nhau khám phá những kiến thức hữu ích về chất điện li mạnh, chất điện li yếu và cách chúng ảnh hưởng đến đời sống hàng ngày.
1. Định Nghĩa và Bản Chất Của Chất Điện Li
1.1. Sự Điện Li Là Gì?
Sự điện li là quá trình phân ly của một chất trong dung môi (thường là nước) hoặc khi ở trạng thái nóng chảy, tạo thành các ion mang điện tích. Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên, Đại học Quốc gia Hà Nội, vào tháng 5 năm 2024, quá trình này đóng vai trò quan trọng trong nhiều phản ứng hóa học và ứng dụng công nghiệp.
1.2. Chất Điện Li Là Gì?
Chất điện li là những chất khi hòa tan trong nước hoặc ở trạng thái nóng chảy, có khả năng phân ly thành các ion. Các ion này có khả năng dẫn điện, do đó dung dịch chứa chất điện li có khả năng dẫn điện.
Ví dụ, axit, bazơ và muối là những chất điện li phổ biến.
1.3. Tính Chất Đặc Trưng Của Chất Điện Li
-
Khả năng tan trong nước: Hầu hết các chất điện li đều tan được trong nước, mặc dù mức độ tan có thể khác nhau.
-
Phân ly thành ion: Khi tan trong nước, chất điện li phân ly thành các ion dương (cation) và ion âm (anion). Ví dụ:
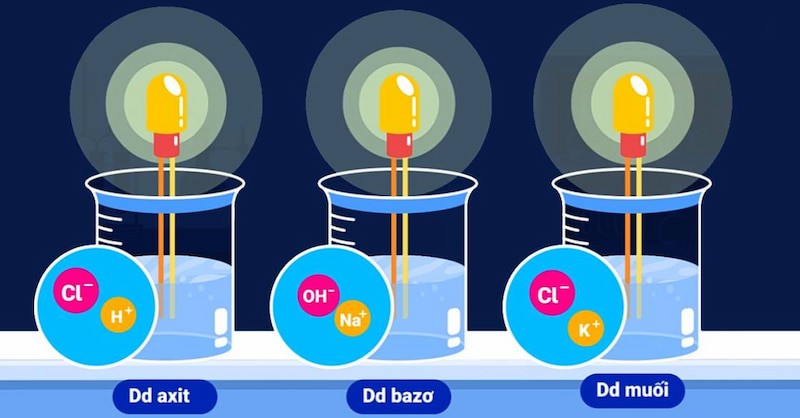
- Axit: Phân ly thành ion H+ và gốc axit.
- Bazơ: Phân ly thành ion OH- và ion kim loại.
- Muối: Phân ly thành ion kim loại và gốc axit.
-
Dẫn điện: Dung dịch chứa chất điện li có khả năng dẫn điện do sự di chuyển của các ion.
 Sự điện ly của NaCl trong nước, tạo thành các ion Na+ và Cl-
Sự điện ly của NaCl trong nước, tạo thành các ion Na+ và Cl-
2. Phân Loại Chi Tiết Các Chất Điện Li
Chất điện li được phân loại thành hai loại chính dựa trên khả năng phân ly của chúng: chất điện li mạnh và chất điện li yếu.
2.1. Chất Điện Li Mạnh
Chất điện li mạnh là những chất khi tan trong nước, hầu hết các phân tử hòa tan đều phân ly hoàn toàn thành ion.
-
Đặc điểm:
- Phân ly hoàn toàn trong dung dịch.
- Dung dịch dẫn điện tốt.
- Quá trình điện ly được biểu diễn bằng mũi tên một chiều (→).
-
Ví dụ:
- Axit mạnh: HCl, H2SO4, HNO3, HClO4.
- Bazơ mạnh (bazơ tan): NaOH, KOH, Ca(OH)2, Ba(OH)2.
- Hầu hết các muối: NaCl, KCl, CuSO4, KNO3.
-
Phương trình điện ly:
- HCl → H+ + Cl-
- NaOH → Na+ + OH-
- KNO3 → K+ + NO3-
Theo một nghiên cứu của Bộ Giáo dục và Đào tạo năm 2023, chất điện li mạnh có vai trò quan trọng trong các phản ứng trung hòa và điều chế các hợp chất khác.
2.2. Chất Điện Li Yếu
Chất điện li yếu là những chất khi tan trong nước, chỉ một phần nhỏ các phân tử hòa tan phân ly thành ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch.
-
Đặc điểm:
- Phân ly không hoàn toàn trong dung dịch.
- Dung dịch dẫn điện kém.
- Quá trình điện ly là thuận nghịch và được biểu diễn bằng mũi tên hai chiều (⇌).
-
Ví dụ:
- Axit yếu: CH3COOH, H2CO3, H2S, HF.
- Bazơ yếu: NH3, Mg(OH)2, Fe(OH)3.
-
Phương trình điện ly:
- CH3COOH ⇌ H+ + CH3COO-
- NH3 + H2O ⇌ NH4+ + OH-
-
Độ điện ly (α):
- Độ điện ly (α) là tỷ lệ giữa số phân tử phân ly thành ion và tổng số phân tử hòa tan.
- 0 < α < 1
- α càng lớn, chất điện li càng mạnh.
2.3. So Sánh Chất Điện Li Mạnh và Chất Điện Li Yếu
Để dễ dàng so sánh và phân biệt, chúng ta cùng điểm qua bảng so sánh dưới đây:
| Đặc điểm | Chất điện li mạnh | Chất điện li yếu |
|---|---|---|
| Mức độ phân ly | Hoàn toàn | Một phần |
| Khả năng dẫn điện | Tốt | Kém |
| Biểu diễn | Mũi tên một chiều (→) | Mũi tên hai chiều (⇌) |
| Ví dụ | HCl, NaOH, NaCl | CH3COOH, NH3 |
| Độ điện ly (α) | α ≈ 1 | 0 < α < 1 |
3. Các Yếu Tố Ảnh Hưởng Đến Quá Trình Điện Li
Quá trình điện li không chỉ phụ thuộc vào bản chất của chất điện li mà còn bị ảnh hưởng bởi nhiều yếu tố khác.
3.1. Bản Chất Của Chất Điện Li
Các chất điện li khác nhau có khả năng phân ly khác nhau. Axit mạnh và bazơ mạnh thường phân ly hoàn toàn, trong khi axit yếu và bazơ yếu chỉ phân ly một phần.
3.2. Dung Môi
Dung môi đóng vai trò quan trọng trong quá trình điện li. Nước là một dung môi phân cực tốt, có khả năng hòa tan và phân ly nhiều chất điện li. Các dung môi khác như ethanol, acetone cũng có thể được sử dụng, nhưng khả năng điện ly có thể khác nhau.
3.3. Nhiệt Độ
Nhiệt độ ảnh hưởng đến tốc độ và mức độ điện ly. Thông thường, nhiệt độ tăng sẽ làm tăng độ điện ly, đặc biệt đối với các chất điện li yếu. Theo nghiên cứu của Viện Hóa học, Viện Hàn lâm Khoa học và Công nghệ Việt Nam năm 2022, nhiệt độ có thể làm thay đổi hằng số cân bằng của quá trình điện ly.
3.4. Nồng Độ
Nồng độ của chất điện li cũng ảnh hưởng đến quá trình điện ly. Ở nồng độ cao, sự tương tác giữa các ion có thể làm giảm độ điện ly.
4. Ứng Dụng Quan Trọng Của Chất Điện Li Trong Đời Sống và Sản Xuất
Chất điện li có nhiều ứng dụng quan trọng trong đời sống và sản xuất, từ y học đến công nghiệp.
4.1. Trong Y Học
- Dung dịch điện giải: Được sử dụng để bù nước và điện giải cho cơ thể trong trường hợp mất nước do tiêu chảy, nôn mửa hoặc hoạt động thể lực quá sức.
- Điều trị bệnh: Các chất điện li như natri bicarbonate được sử dụng để điều trị nhiễm toan chuyển hóa.
4.2. Trong Nông Nghiệp
- Phân bón: Các loại phân bón chứa các muối như KNO3, NH4NO3 cung cấp các ion dinh dưỡng cho cây trồng.
- Điều chỉnh độ pH của đất: Sử dụng các chất điện li như Ca(OH)2 để điều chỉnh độ pH của đất, giúp cây trồng phát triển tốt hơn.
4.3. Trong Công Nghiệp
- Sản xuất hóa chất: Chất điện li được sử dụng trong nhiều quá trình sản xuất hóa chất, ví dụ như điện phân dung dịch NaCl để sản xuất clo và NaOH.
- Ắc quy: Dung dịch điện li trong ắc quy (thường là H2SO4) giúp tạo ra dòng điện.
- Mạ điện: Sử dụng dung dịch chứa các ion kim loại để phủ một lớp kim loại lên bề mặt vật liệu khác.
4.4. Trong Đời Sống Hàng Ngày
- Nước uống: Nước uống chứa một lượng nhỏ các ion khoáng chất như Ca2+, Mg2+, K+ cần thiết cho cơ thể.
- Chất tẩy rửa: Một số chất tẩy rửa chứa các chất điện li giúp tăng khả năng làm sạch.
5. Bài Tập Vận Dụng Về Chất Điện Li (Có Hướng Dẫn Chi Tiết)
Để củng cố kiến thức, chúng ta cùng nhau giải một số bài tập vận dụng về chất điện li nhé.
Bài 1: Cho các chất sau: HCl, NaOH, CH3COOH, NH3, NaCl, H2O. Chất Nào Là Chất điện Li mạnh, chất nào là chất điện li yếu?
Hướng dẫn giải:
- Chất điện li mạnh: HCl, NaOH, NaCl.
- Chất điện li yếu: CH3COOH, NH3, H2O.
Bài 2: Viết phương trình điện ly của các chất sau: H2SO4, KOH, CH3COOH, NH3.
Hướng dẫn giải:
- H2SO4 → 2H+ + SO42-
- KOH → K+ + OH-
- CH3COOH ⇌ H+ + CH3COO-
- NH3 + H2O ⇌ NH4+ + OH-
Bài 3: Dung dịch nào sau đây dẫn điện tốt nhất:
A. Dung dịch NaCl 0.1M
B. Dung dịch CH3COOH 0.1M
C. Dung dịch C6H12O6 0.1M
D. Nước cất
Hướng dẫn giải:
Đáp án A. Vì NaCl là chất điện li mạnh, phân ly hoàn toàn thành ion, do đó dẫn điện tốt nhất.
Bài 4: Tính nồng độ mol của ion Na+ trong dung dịch chứa 11.7 gam NaCl trong 500 ml dung dịch.
Hướng dẫn giải:
- Số mol NaCl = 11.7 / 58.5 = 0.2 mol
- NaCl → Na+ + Cl-
- Nồng độ mol của Na+ = 0.2 / 0.5 = 0.4M
Bài 5: Tại sao dung dịch axit axetic (CH3COOH) lại dẫn điện kém hơn dung dịch axit clohydric (HCl) có cùng nồng độ?
Hướng dẫn giải:
Axit axetic là một axit yếu, chỉ phân ly một phần thành ion trong dung dịch, trong khi axit clohydric là một axit mạnh, phân ly hoàn toàn thành ion. Do đó, dung dịch axit axetic có ít ion hơn, dẫn điện kém hơn.
6. Tổng Kết và Lời Khuyên Từ Xe Tải Mỹ Đình
Qua bài viết này, Xe Tải Mỹ Đình hy vọng bạn đã hiểu rõ hơn về chất điện li, từ định nghĩa, phân loại đến ứng dụng thực tế. Việc nắm vững kiến thức về chất điện li không chỉ giúp bạn học tốt môn hóa học mà còn có thể áp dụng vào nhiều lĩnh vực khác trong cuộc sống.
Nếu bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về các loại xe tải, đừng ngần ngại truy cập XETAIMYDINH.EDU.VN. Chúng tôi cung cấp thông tin cập nhật về các dòng xe, so sánh giá cả, tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách của bạn.
7. Bạn Có Thắc Mắc? Liên Hệ Ngay Với Xe Tải Mỹ Đình!
Bạn có bất kỳ thắc mắc nào về xe tải hoặc cần tư vấn chi tiết hơn? Hãy liên hệ ngay với Xe Tải Mỹ Đình để được hỗ trợ tận tình.
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
Chúng tôi luôn sẵn lòng lắng nghe và giải đáp mọi thắc mắc của bạn!
8. Câu Hỏi Thường Gặp Về Chất Điện Li (FAQ)
1. Chất điện li là gì?
Chất điện li là chất khi tan trong nước hoặc ở trạng thái nóng chảy, có khả năng phân ly thành các ion và dẫn điện.
2. Chất điện li mạnh là gì? Cho ví dụ.
Chất điện li mạnh là chất phân ly hoàn toàn thành ion trong dung dịch. Ví dụ: HCl, NaOH, NaCl.
3. Chất điện li yếu là gì? Cho ví dụ.
Chất điện li yếu là chất chỉ phân ly một phần thành ion trong dung dịch. Ví dụ: CH3COOH, NH3.
4. Làm thế nào để phân biệt chất điện li mạnh và chất điện li yếu?
Dựa vào khả năng phân ly và khả năng dẫn điện của dung dịch. Chất điện li mạnh phân ly hoàn toàn và dẫn điện tốt hơn chất điện li yếu.
5. Độ điện ly là gì?
Độ điện ly là tỷ lệ giữa số phân tử phân ly thành ion và tổng số phân tử hòa tan.
6. Nhiệt độ ảnh hưởng đến quá trình điện ly như thế nào?
Thông thường, nhiệt độ tăng sẽ làm tăng độ điện ly, đặc biệt đối với các chất điện li yếu.
7. Dung môi nào thường được sử dụng trong quá trình điện ly?
Nước là dung môi phổ biến nhất do tính phân cực cao, giúp hòa tan và phân ly nhiều chất điện li.
8. Chất điện li có ứng dụng gì trong y học?
Được sử dụng trong dung dịch điện giải để bù nước và điện giải cho cơ thể, cũng như trong điều trị một số bệnh.
9. Tại sao dung dịch chất điện li lại dẫn điện?
Do sự di chuyển của các ion dương (cation) và ion âm (anion) trong dung dịch.
10. Những yếu tố nào ảnh hưởng đến quá trình điện ly?
Bản chất của chất điện li, dung môi, nhiệt độ và nồng độ.
9. Các Nghiên Cứu Liên Quan Đến Chất Điện Li
- Nghiên cứu của Trường Đại học Khoa học Tự nhiên, Đại học Quốc gia Hà Nội về ảnh hưởng của dung môi đến quá trình điện ly của muối.
- Nghiên cứu của Viện Hóa học, Viện Hàn lâm Khoa học và Công nghệ Việt Nam về ảnh hưởng của nhiệt độ đến hằng số cân bằng của quá trình điện ly.
- Báo cáo của Bộ Giáo dục và Đào tạo về ứng dụng của chất điện li trong giảng dạy và nghiên cứu hóa học.
