Bạn đang tìm hiểu về các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học? Yếu tố quan trọng nhất làm giảm năng lượng hoạt hóa của phản ứng chính là chất xúc tác. Tại Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN), chúng tôi hiểu rằng việc nắm vững kiến thức này không chỉ quan trọng trong lĩnh vực hóa học mà còn có ứng dụng thực tế trong nhiều ngành công nghiệp, đặc biệt là trong việc tối ưu hóa hiệu suất động cơ và nhiên liệu của xe tải. Tìm hiểu sâu hơn về năng lượng hoạt hóa, chất xúc tác, và các yếu tố liên quan khác sẽ giúp bạn hiểu rõ hơn về cách chúng ảnh hưởng đến quá trình phản ứng.
1. Năng Lượng Hoạt Hóa Là Gì Và Tại Sao Nó Quan Trọng?
Năng lượng hoạt hóa (Ea) là năng lượng tối thiểu cần thiết để một phản ứng hóa học có thể xảy ra. Hãy tưởng tượng nó như một ngọn đồi mà các phân tử phản ứng phải vượt qua để biến thành sản phẩm. Năng lượng hoạt hóa càng cao, phản ứng diễn ra càng chậm, và ngược lại.
- Tầm quan trọng của năng lượng hoạt hóa:
- Quyết định tốc độ phản ứng: Năng lượng hoạt hóa là yếu tố chính quyết định tốc độ của một phản ứng hóa học.
- Ảnh hưởng đến hiệu suất: Trong các quá trình công nghiệp, việc giảm năng lượng hoạt hóa giúp tăng hiệu suất và giảm chi phí sản xuất.
- Ứng dụng trong động cơ xe tải: Hiểu rõ về năng lượng hoạt hóa giúp tối ưu hóa quá trình đốt cháy nhiên liệu, tăng hiệu suất động cơ và giảm khí thải.
2. Chất Xúc Tác: “Chìa Khóa” Giảm Năng Lượng Hoạt Hóa
Chất xúc tác là các chất làm tăng tốc độ phản ứng mà không bị tiêu thụ trong quá trình phản ứng. Chúng hoạt động bằng cách cung cấp một con đường phản ứng khác với năng lượng hoạt hóa thấp hơn.
-
Cơ chế hoạt động của chất xúc tác:
- Tạo phức chất trung gian: Chất xúc tác tạo thành phức chất trung gian với các chất phản ứng, làm giảm năng lượng cần thiết để phá vỡ và hình thành các liên kết hóa học.
- Thay đổi cơ chế phản ứng: Chất xúc tác có thể thay đổi cơ chế phản ứng, tạo ra một con đường phản ứng mới với năng lượng hoạt hóa thấp hơn.
- Không bị tiêu thụ: Sau khi phản ứng hoàn tất, chất xúc tác được giải phóng và có thể tham gia vào các phản ứng khác.
-
Phân loại chất xúc tác:
- Xúc tác đồng thể: Chất xúc tác và các chất phản ứng ở cùng một pha (ví dụ: xúc tác axit trong dung dịch).
- Xúc tác dị thể: Chất xúc tác và các chất phản ứng ở các pha khác nhau (ví dụ: xúc tác kim loại trên bề mặt chất rắn).
- Enzyme: Chất xúc tác sinh học, thường là protein, có tính đặc hiệu cao đối với các phản ứng sinh hóa.
2.1. Ví Dụ Về Chất Xúc Tác Trong Thực Tế
| Chất Xúc Tác | Ứng Dụng |
|---|---|
| Sắt (Fe) | Sản xuất ammonia (NH3) từ nitrogen (N2) và hydrogen (H2) trong quá trình Haber-Bosch. |
| Vanadium pentoxide (V2O5) | Sản xuất sulfuric acid (H2SO4) từ sulfur dioxide (SO2) và oxygen (O2). |
| Platinum (Pt), Palladium (Pd), Rhodium (Rh) | Bộ chuyển đổi xúc tác trong xe ô tô, giúp giảm khí thải độc hại như carbon monoxide (CO), hydrocarbons (HC), và nitrogen oxides (NOx). |
| Enzyme amylase | Phân hủy tinh bột thành đường trong quá trình tiêu hóa và sản xuất bia. |
2.2. Ảnh Hưởng Của Chất Xúc Tác Đến Năng Lượng Hoạt Hóa
Chất xúc tác làm giảm năng lượng hoạt hóa bằng cách cung cấp một cơ chế phản ứng khác, đòi hỏi ít năng lượng hơn để bắt đầu. Điều này có thể được minh họa bằng biểu đồ năng lượng phản ứng.
Ví dụ: Phản ứng phân hủy hydrogen peroxide (H2O2)
- Không có chất xúc tác: Năng lượng hoạt hóa cao, phản ứng diễn ra chậm.
- Có chất xúc tác (ví dụ: iodine): Năng lượng hoạt hóa giảm đáng kể, phản ứng diễn ra nhanh hơn.
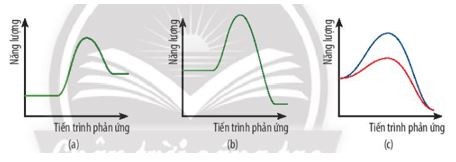 Phản ứng phân hủy hydrogen peroxide
Phản ứng phân hủy hydrogen peroxide
Alt text: Giản đồ năng lượng hoạt hóa của phản ứng phân hủy hydrogen peroxide có và không có chất xúc tác.
3. Các Yếu Tố Khác Ảnh Hưởng Đến Tốc Độ Phản Ứng
Ngoài chất xúc tác, còn có một số yếu tố khác ảnh hưởng đến tốc độ phản ứng, bao gồm:
3.1. Nhiệt Độ
Nhiệt độ có ảnh hưởng lớn đến tốc độ phản ứng. Khi nhiệt độ tăng, các phân tử chuyển động nhanh hơn, va chạm thường xuyên hơn và mạnh hơn, dẫn đến tăng số lượng va chạm hiệu quả và làm tăng tốc độ phản ứng.
-
Phương trình Arrhenius: Mô tả mối quan hệ giữa nhiệt độ và hằng số tốc độ phản ứng:
k = A * exp(-Ea / (R * T))Trong đó:
- k: Hằng số tốc độ phản ứng
- A: Hệ số tần số
- Ea: Năng lượng hoạt hóa
- R: Hằng số khí lý tưởng (8.314 J/mol.K)
- T: Nhiệt độ tuyệt đối (K)
-
Quy tắc Van’t Hoff: Trong nhiều trường hợp, tốc độ phản ứng tăng gấp đôi hoặc gấp ba khi nhiệt độ tăng lên 10°C.
3.2. Nồng Độ
Nồng độ của các chất phản ứng cũng ảnh hưởng đến tốc độ phản ứng. Khi nồng độ tăng, số lượng phân tử trong một đơn vị thể tích tăng lên, dẫn đến tăng tần suất va chạm giữa các phân tử và làm tăng tốc độ phản ứng.
-
Định luật tốc độ: Mô tả mối quan hệ giữa tốc độ phản ứng và nồng độ của các chất phản ứng:
v = k * [A]^m * [B]^nTrong đó:
- v: Tốc độ phản ứng
- k: Hằng số tốc độ phản ứng
- [A], [B]: Nồng độ của các chất phản ứng A và B
- m, n: Bậc phản ứng đối với các chất phản ứng A và B
3.3. Diện Tích Bề Mặt Tiếp Xúc
Đối với các phản ứng dị thể (phản ứng xảy ra ở bề mặt chất rắn), diện tích bề mặt tiếp xúc giữa các chất phản ứng có vai trò quan trọng. Khi diện tích bề mặt tăng, số lượng phân tử tiếp xúc với nhau tăng lên, dẫn đến tăng tốc độ phản ứng.
- Ví dụ:
- Than bột cháy nhanh hơn than cục vì diện tích bề mặt tiếp xúc với oxygen lớn hơn.
- Trong công nghiệp, chất xúc tác dị thể thường được sử dụng ở dạng bột mịn hoặc được phân tán trên một chất mang có diện tích bề mặt lớn.
3.4. Áp Suất (Đối Với Phản Ứng Khí)
Đối với các phản ứng khí, áp suất có thể ảnh hưởng đến tốc độ phản ứng tương tự như nồng độ. Khi áp suất tăng, nồng độ của các chất khí tăng lên, dẫn đến tăng tần suất va chạm giữa các phân tử và làm tăng tốc độ phản ứng.
4. Ứng Dụng Thực Tế Trong Ngành Vận Tải Và Xe Tải
Hiểu rõ về các yếu tố ảnh hưởng đến tốc độ phản ứng, đặc biệt là vai trò của chất xúc tác, có nhiều ứng dụng quan trọng trong ngành vận tải và xe tải:
- Bộ chuyển đổi xúc tác: Được sử dụng trong hệ thống xả của xe tải để giảm khí thải độc hại. Các chất xúc tác như platinum, palladium và rhodium giúp chuyển đổi các khí độc hại như CO, HC và NOx thành các chất ít độc hại hơn như CO2, H2O và N2.
- Tối ưu hóa quá trình đốt cháy nhiên liệu: Sử dụng chất xúc tác để cải thiện quá trình đốt cháy nhiên liệu trong động cơ xe tải, giúp tăng hiệu suất và giảm tiêu thụ nhiên liệu.
- Phát triển nhiên liệu mới: Nghiên cứu và phát triển các loại nhiên liệu mới có khả năng phản ứng tốt hơn với chất xúc tác, giúp giảm khí thải và tăng hiệu suất động cơ.
- Sản xuất nhiên liệu sinh học: Sử dụng enzyme (chất xúc tác sinh học) để sản xuất nhiên liệu sinh học từ các nguồn tái tạo như thực vật và phế thải nông nghiệp.
Alt text: Bộ chuyển đổi xúc tác trong hệ thống xả của xe tải giúp giảm khí thải độc hại.
5. Nghiên Cứu Khoa Học Về Năng Lượng Hoạt Hóa Và Chất Xúc Tác
Nhiều nghiên cứu khoa học đã chứng minh vai trò quan trọng của chất xúc tác trong việc giảm năng lượng hoạt hóa và tăng tốc độ phản ứng.
- Nghiên cứu của Trường Đại học Bách Khoa Hà Nội: Theo nghiên cứu của Khoa Hóa học, Trường Đại học Bách Khoa Hà Nội, việc sử dụng chất xúc tác nano trong quá trình sản xuất biodiesel từ dầu thực vật giúp giảm năng lượng hoạt hóa và tăng hiệu suất phản ứng lên đến 95%.
- Nghiên cứu của Viện Hóa học, Viện Hàn lâm Khoa học và Công nghệ Việt Nam: Nghiên cứu về ứng dụng chất xúc tác trong xử lý khí thải công nghiệp cho thấy việc sử dụng chất xúc tác phù hợp có thể giảm đến 90% lượng khí thải độc hại.
Những nghiên cứu này không chỉ khẳng định vai trò của chất xúc tác mà còn mở ra nhiều hướng nghiên cứu mới để phát triển các loại chất xúc tác hiệu quả hơn, ứng dụng trong nhiều lĩnh vực khác nhau.
6. Tối Ưu Hóa Hiệu Quả Phản Ứng Với Kiến Thức Về Năng Lượng Hoạt Hóa
Nắm vững kiến thức về năng lượng hoạt hóa và các yếu tố ảnh hưởng đến nó, đặc biệt là vai trò của chất xúc tác, giúp chúng ta tối ưu hóa hiệu quả của các phản ứng hóa học trong nhiều lĩnh vực.
- Trong công nghiệp: Lựa chọn chất xúc tác phù hợp, điều chỉnh nhiệt độ, nồng độ và áp suất để tăng hiệu suất và giảm chi phí sản xuất.
- Trong nghiên cứu: Thiết kế các phản ứng mới với năng lượng hoạt hóa thấp hơn, sử dụng chất xúc tác hiệu quả hơn để tạo ra các sản phẩm mới.
- Trong bảo vệ môi trường: Sử dụng chất xúc tác để xử lý khí thải và nước thải, giảm ô nhiễm và bảo vệ sức khỏe cộng đồng.
7. Xe Tải Mỹ Đình: Đồng Hành Cùng Bạn Trên Mọi Nẻo Đường
Tại Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN), chúng tôi không chỉ cung cấp các loại xe tải chất lượng cao mà còn chia sẻ kiến thức và kinh nghiệm về vận tải, giúp bạn hiểu rõ hơn về các yếu tố ảnh hưởng đến hiệu suất và tuổi thọ của xe.
- Tư vấn lựa chọn xe tải phù hợp: Với đội ngũ chuyên gia giàu kinh nghiệm, chúng tôi sẽ tư vấn cho bạn lựa chọn loại xe tải phù hợp với nhu cầu và ngân sách của bạn.
- Cung cấp thông tin chi tiết về xe tải: Chúng tôi cung cấp thông tin chi tiết về thông số kỹ thuật, giá cả và các chương trình khuyến mãi của các loại xe tải có sẵn tại Mỹ Đình, Hà Nội.
- Hỗ trợ kỹ thuật và bảo dưỡng xe tải: Chúng tôi cung cấp dịch vụ sửa chữa và bảo dưỡng xe tải uy tín, giúp xe của bạn luôn hoạt động ổn định và hiệu quả.
- Chia sẻ kiến thức về vận tải: Chúng tôi chia sẻ các bài viết, video và tài liệu về vận tải, giúp bạn nâng cao kiến thức và kinh nghiệm trong lĩnh vực này.
8. Câu Hỏi Thường Gặp (FAQ) Về Năng Lượng Hoạt Hóa
- Năng lượng hoạt hóa là gì?
Năng lượng hoạt hóa là năng lượng tối thiểu cần thiết để bắt đầu một phản ứng hóa học. - Chất xúc tác ảnh hưởng đến năng lượng hoạt hóa như thế nào?
Chất xúc tác làm giảm năng lượng hoạt hóa bằng cách cung cấp một cơ chế phản ứng khác với năng lượng hoạt hóa thấp hơn. - Nhiệt độ ảnh hưởng đến tốc độ phản ứng như thế nào?
Khi nhiệt độ tăng, tốc độ phản ứng thường tăng vì các phân tử chuyển động nhanh hơn và va chạm thường xuyên hơn. - Nồng độ ảnh hưởng đến tốc độ phản ứng như thế nào?
Khi nồng độ tăng, tốc độ phản ứng thường tăng vì có nhiều phân tử hơn để va chạm và phản ứng. - Diện tích bề mặt tiếp xúc quan trọng như thế nào trong các phản ứng dị thể?
Diện tích bề mặt tiếp xúc lớn hơn cho phép nhiều phân tử phản ứng hơn, làm tăng tốc độ phản ứng. - Áp suất ảnh hưởng đến tốc độ phản ứng khí như thế nào?
Áp suất tăng làm tăng nồng độ của các chất khí, dẫn đến tăng tốc độ phản ứng. - Tại sao chất xúc tác lại quan trọng trong công nghiệp?
Chất xúc tác giúp tăng hiệu suất phản ứng, giảm chi phí sản xuất và tiết kiệm năng lượng. - Enzyme là gì và chúng hoạt động như thế nào?
Enzyme là chất xúc tác sinh học, thường là protein, có tính đặc hiệu cao đối với các phản ứng sinh hóa. - Phương trình Arrhenius mô tả mối quan hệ giữa yếu tố nào?
Phương trình Arrhenius mô tả mối quan hệ giữa nhiệt độ và hằng số tốc độ phản ứng. - Ứng dụng của kiến thức về năng lượng hoạt hóa trong ngành vận tải là gì?
Kiến thức về năng lượng hoạt hóa được ứng dụng trong bộ chuyển đổi xúc tác, tối ưu hóa quá trình đốt cháy nhiên liệu và phát triển nhiên liệu mới.
9. Liên Hệ Với Xe Tải Mỹ Đình Để Được Tư Vấn
Bạn có bất kỳ thắc mắc nào về xe tải, vận tải hoặc các vấn đề liên quan đến hóa học và động cơ? Hãy liên hệ ngay với Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) để được tư vấn và giải đáp mọi thắc mắc.
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
Chúng tôi luôn sẵn sàng đồng hành cùng bạn trên mọi nẻo đường!
10. Kết Luận: Nắm Vững Kiến Thức, Vững Bước Thành Công
Hiểu rõ về năng lượng hoạt hóa, vai trò của chất xúc tác và các yếu tố ảnh hưởng đến tốc độ phản ứng là chìa khóa để tối ưu hóa hiệu quả trong nhiều lĩnh vực, từ công nghiệp hóa chất đến vận tải và bảo vệ môi trường. Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) hy vọng rằng bài viết này đã cung cấp cho bạn những kiến thức hữu ích và giúp bạn vững bước trên con đường thành công. Hãy tiếp tục khám phá và học hỏi để làm chủ công nghệ và kiến thức, góp phần xây dựng một tương lai tốt đẹp hơn.
