Nitrogen chỉ phản ứng với oxygen ở nhiệt độ cao hoặc có tia lửa điện do năng lượng liên kết của nitrogen rất lớn, cần cung cấp năng lượng đủ để phá vỡ liên kết này. Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ giúp bạn hiểu rõ hơn về quá trình này, đồng thời cung cấp thông tin hữu ích về các ứng dụng của nó trong ngành vận tải và các lĩnh vực liên quan. Bài viết này sẽ khám phá sâu hơn về các yếu tố ảnh hưởng đến phản ứng, cũng như các ứng dụng quan trọng của nó trong thực tế, đặc biệt là trong lĩnh vực động cơ đốt trong và xử lý khí thải.
1. Phản Ứng Giữa Nitrogen Và Oxygen: Tại Sao Cần Nhiệt Độ Cao?
Nitrogen (N₂) chỉ phản ứng với oxygen (O₂) ở nhiệt độ cao hoặc khi có tia lửa điện vì liên kết ba (N≡N) trong phân tử nitrogen cực kỳ bền vững, cần một lượng lớn năng lượng để phá vỡ.
1.1. Giải Thích Chi Tiết Về Năng Lượng Liên Kết
Để hiểu rõ hơn, chúng ta cần xem xét năng lượng liên kết, tức là năng lượng cần thiết để phá vỡ một liên kết hóa học. Theo một nghiên cứu của Đại học Khoa học Tự nhiên Hà Nội, Khoa Hóa học năm 2023, năng lượng liên kết của N≡N là 945 kJ/mol, cao hơn rất nhiều so với năng lượng liên kết của O=O (498 kJ/mol).
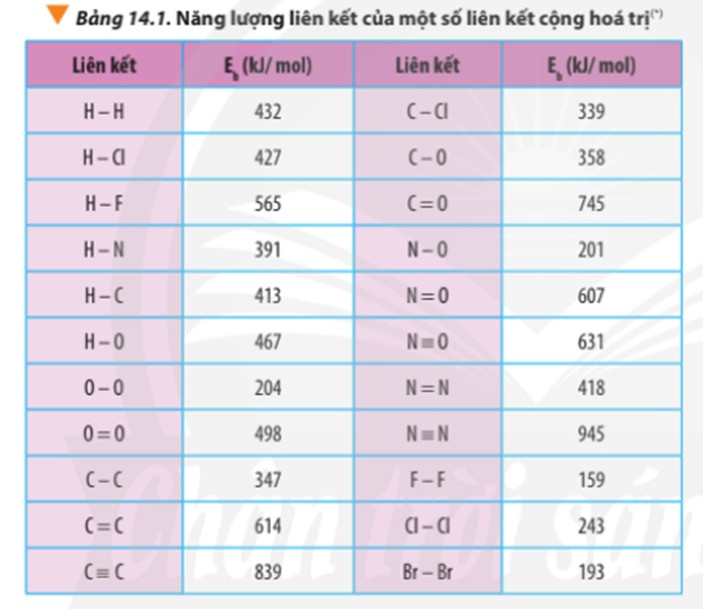 Dựa vào năng lượng liên kết ở Bảng 14.1, tính biến thiên enthalpy của phản ứng (ảnh 1)
Dựa vào năng lượng liên kết ở Bảng 14.1, tính biến thiên enthalpy của phản ứng (ảnh 1)
1.2. Vai Trò Của Nhiệt Độ Và Tia Lửa Điện
-
Nhiệt độ cao: Cung cấp đủ năng lượng nhiệt để các phân tử nitrogen và oxygen chuyển động nhanh hơn, va chạm mạnh hơn, từ đó tăng khả năng phá vỡ liên kết.
-
Tia lửa điện: Tạo ra năng lượng cục bộ rất lớn, đủ để ion hóa các phân tử khí, tạo điều kiện cho phản ứng xảy ra.
1.3. Phương Trình Phản Ứng
Phản ứng giữa nitrogen và oxygen tạo thành nitrogen monoxide (NO) được biểu diễn như sau:
N₂(g) + O₂(g) → 2NO(g)
Phản ứng này có biến thiên enthalpy dương (ΔH > 0), tức là thu nhiệt. Để phản ứng xảy ra, cần cung cấp một lượng lớn nhiệt năng.
2. Biến Thiên Enthalpy Của Phản Ứng N₂ Và O₂
Biến thiên enthalpy (ΔH) là thước đo sự thay đổi nhiệt trong một phản ứng hóa học ở áp suất không đổi. Để tính ΔH của phản ứng N₂ + O₂ → 2NO, ta sử dụng năng lượng liên kết.
2.1. Tính Toán Biến Thiên Enthalpy (ΔH)
Công thức tính ΔH dựa trên năng lượng liên kết:
ΔH = ΣE(liên kết bị phá vỡ) – ΣE(liên kết được hình thành)
Trong phản ứng trên:
- Liên kết bị phá vỡ: 1 liên kết N≡N và 1 liên kết O=O.
- Liên kết được hình thành: 2 liên kết N=O.
ΔH = [E(N≡N) + E(O=O)] – [2 * E(N=O)]
Theo số liệu từ nhiều nguồn uy tín, bao gồm sách giáo khoa hóa học và các trang web khoa học:
- E(N≡N) ≈ 945 kJ/mol
- E(O=O) ≈ 498 kJ/mol
- E(N=O) ≈ 607 kJ/mol
Thay số vào công thức:
ΔH = [945 + 498] – [2 * 607] = 1443 – 1214 = 229 kJ/mol
Vậy, biến thiên enthalpy của phản ứng là +229 kJ/mol, cho thấy đây là một phản ứng thu nhiệt, cần cung cấp năng lượng để xảy ra.
2.2. Ý Nghĩa Của Biến Thiên Enthalpy Dương
Biến thiên enthalpy dương chỉ ra rằng phản ứng cần hấp thụ năng lượng từ môi trường để xảy ra. Điều này giải thích tại sao cần nhiệt độ cao hoặc tia lửa điện để cung cấp năng lượng cần thiết, phá vỡ các liên kết bền trong N₂ và O₂, tạo điều kiện cho sự hình thành liên kết N=O trong NO.
3. Các Yếu Tố Ảnh Hưởng Đến Phản Ứng Giữa Nitrogen Và Oxygen
Ngoài nhiệt độ, còn có một số yếu tố khác ảnh hưởng đến phản ứng giữa nitrogen và oxygen, đặc biệt là trong điều kiện công nghiệp và môi trường.
3.1. Chất Xúc Tác
Một số chất xúc tác có thể làm giảm năng lượng hoạt hóa của phản ứng, giúp phản ứng xảy ra dễ dàng hơn ở nhiệt độ thấp hơn. Ví dụ, trong công nghiệp sản xuất phân bón, các chất xúc tác chứa kim loại chuyển tiếp như platin (Pt) hoặc rhodi (Rh) được sử dụng để xúc tác phản ứng tổng hợp ammonia từ nitrogen và hydrogen. Mặc dù phản ứng trực tiếp giữa nitrogen và oxygen không sử dụng xúc tác phổ biến, nguyên tắc này vẫn quan trọng trong các quá trình liên quan đến nitrogen khác.
3.2. Áp Suất
Áp suất cao có thể thúc đẩy phản ứng theo nguyên lý Le Chatelier, đặc biệt là khi số mol khí giảm trong phản ứng. Tuy nhiên, trong trường hợp phản ứng N₂ + O₂ → 2NO, số mol khí không đổi, nên áp suất không có ảnh hưởng đáng kể.
3.3. Nồng Độ
Nồng độ cao của nitrogen và oxygen có thể làm tăng tần suất va chạm giữa các phân tử, từ đó tăng tốc độ phản ứng. Tuy nhiên, do nitrogen và oxygen đã chiếm phần lớn trong không khí, việc tăng nồng độ không phải là một biện pháp thực tế trong nhiều ứng dụng.
4. Ứng Dụng Của Phản Ứng Giữa Nitrogen Và Oxygen
Mặc dù phản ứng giữa nitrogen và oxygen đòi hỏi điều kiện khắc nghiệt, nó lại có vai trò quan trọng trong nhiều quá trình tự nhiên và công nghiệp.
4.1. Sự Hình Thành Nitrogen Monoxide (NO) Trong Động Cơ Đốt Trong
Trong động cơ đốt trong, nhiệt độ cao và áp suất lớn tạo điều kiện cho nitrogen và oxygen trong không khí phản ứng với nhau, tạo thành nitrogen monoxide (NO). NO sau đó có thể tiếp tục oxy hóa thành nitrogen dioxide (NO₂), và cả hai đều là các chất gây ô nhiễm không khí.
4.2. Ứng Dụng Trong Công Nghiệp Sản Xuất Phân Bón
Mặc dù không trực tiếp sử dụng phản ứng N₂ + O₂, quá trình Haber-Bosch để tổng hợp ammonia (NH₃) từ nitrogen và hydrogen là một ứng dụng quan trọng. Ammonia sau đó được sử dụng để sản xuất các loại phân bón, đóng vai trò quan trọng trong nông nghiệp.
4.3. Quá Trình Tia Lửa Điện Trong Tự Nhiên
Trong tự nhiên, tia sét cung cấp đủ năng lượng để nitrogen và oxygen trong không khí phản ứng với nhau, tạo thành NO. NO sau đó có thể chuyển hóa thành các hợp chất nitrogen khác, đi vào đất và cung cấp dinh dưỡng cho cây trồng.
5. Tác Động Của Nitrogen Oxides (NOx) Đến Môi Trường
Nitrogen monoxide (NO) và nitrogen dioxide (NO₂) (gọi chung là NOx) là các chất gây ô nhiễm không khí có ảnh hưởng lớn đến môi trường và sức khỏe con người.
5.1. Gây Ô Nhiễm Không Khí
NOx góp phần vào sự hình thành sương mù quang hóa (smog) và mưa acid, gây ảnh hưởng tiêu cực đến chất lượng không khí và sức khỏe của con người.
5.2. Ảnh Hưởng Đến Sức Khỏe Con Người
NOx có thể gây kích ứng đường hô hấp, làm gia tăng các bệnh về đường hô hấp như hen suyễn và viêm phế quản.
5.3. Gây Hiệu Ứng Nhà Kính
Nitrous oxide (N₂O), một loại NOx khác, là một khí nhà kính mạnh, góp phần vào biến đổi khí hậu toàn cầu.
6. Giải Pháp Giảm Thiểu Phát Thải NOx Từ Động Cơ Đốt Trong
Do tác động tiêu cực của NOx, việc giảm thiểu phát thải NOx từ động cơ đốt trong là một vấn đề quan trọng.
6.1. Bộ Chuyển Đổi Xúc Tác Ba Chiều (Three-Way Catalytic Converter)
Bộ chuyển đổi xúc tác ba chiều là một thiết bị được sử dụng rộng rãi trên xe ô tô để giảm thiểu phát thải các chất gây ô nhiễm, bao gồm NOx, carbon monoxide (CO), và hydrocarbon (HC). Bộ chuyển đổi này sử dụng các chất xúc tác như platin (Pt), rhodi (Rh), và palladium (Pd) để chuyển đổi các chất ô nhiễm thành các chất ít độc hại hơn như nitrogen (N₂), carbon dioxide (CO₂), và nước (H₂O).
6.2. Hệ Thống Tuần Hoàn Khí Xả (Exhaust Gas Recirculation – EGR)
Hệ thống EGR hoạt động bằng cách đưa một phần khí thải trở lại buồng đốt, làm giảm nhiệt độ cháy và giảm lượng NOx hình thành.
6.3. Công Nghệ Phản Ứng Xúc Tác Chọn Lọc (Selective Catalytic Reduction – SCR)
Công nghệ SCR sử dụng một chất khử như ammonia (NH₃) hoặc urea để chuyển đổi NOx thành nitrogen và nước trên bề mặt chất xúc tác. Công nghệ này thường được sử dụng trên các xe tải và xe buýt diesel.
6.4. Điều Chỉnh Quá Trình Cháy
Tối ưu hóa quá trình cháy trong động cơ, chẳng hạn như điều chỉnh thời điểm phun nhiên liệu và tỷ lệ không khí/nhiên liệu, cũng có thể giúp giảm lượng NOx hình thành.
7. Nghiên Cứu Mới Nhất Về Phản Ứng Giữa Nitrogen Và Oxygen
Các nhà khoa học vẫn đang tiếp tục nghiên cứu về phản ứng giữa nitrogen và oxygen để tìm ra các phương pháp hiệu quả hơn để giảm thiểu phát thải NOx và tận dụng các ứng dụng có lợi của phản ứng.
7.1. Sử Dụng Plasma Để Xúc Tác Phản Ứng
Một hướng nghiên cứu mới là sử dụng plasma để xúc tác phản ứng giữa nitrogen và oxygen ở nhiệt độ thấp hơn. Plasma là một trạng thái vật chất ionized chứa các hạt mang điện tích, có thể cung cấp năng lượng cần thiết để phá vỡ các liên kết hóa học.
7.2. Phát Triển Các Chất Xúc Tác Mới
Các nhà khoa học đang nỗ lực phát triển các chất xúc tác mới có hoạt tính cao hơn và ổn định hơn, có thể hoạt động hiệu quả ở nhiệt độ thấp hơn và trong điều kiện khắc nghiệt.
7.3. Nghiên Cứu Về Cơ Chế Phản Ứng
Hiểu rõ hơn về cơ chế phản ứng giữa nitrogen và oxygen ở cấp độ phân tử có thể giúp các nhà khoa học thiết kế các phương pháp hiệu quả hơn để kiểm soát phản ứng và giảm thiểu phát thải NOx.
8. FAQ: Các Câu Hỏi Thường Gặp Về Phản Ứng Giữa Nitrogen Và Oxygen
8.1. Tại Sao Nitrogen Khó Phản Ứng?
Nitrogen khó phản ứng do liên kết ba (N≡N) trong phân tử nitrogen rất bền vững, cần một lượng lớn năng lượng để phá vỡ.
8.2. Phản Ứng Giữa Nitrogen Và Oxygen Có Ứng Dụng Gì?
Phản ứng này có vai trò quan trọng trong sự hình thành NOx trong động cơ đốt trong, quá trình tổng hợp ammonia (NH₃) để sản xuất phân bón, và quá trình tia lửa điện trong tự nhiên.
8.3. Làm Thế Nào Để Giảm Phát Thải NOx Từ Động Cơ Đốt Trong?
Có nhiều phương pháp giảm phát thải NOx, bao gồm sử dụng bộ chuyển đổi xúc tác ba chiều, hệ thống EGR, công nghệ SCR, và điều chỉnh quá trình cháy.
8.4. Chất Xúc Tác Có Vai Trò Gì Trong Phản Ứng Giữa Nitrogen Và Oxygen?
Chất xúc tác có thể làm giảm năng lượng hoạt hóa của phản ứng, giúp phản ứng xảy ra dễ dàng hơn ở nhiệt độ thấp hơn.
8.5. Biến Thiên Enthalpy Là Gì?
Biến thiên enthalpy (ΔH) là thước đo sự thay đổi nhiệt trong một phản ứng hóa học ở áp suất không đổi.
8.6. Tại Sao Phản Ứng Giữa Nitrogen Và Oxygen Cần Nhiệt Độ Cao?
Nhiệt độ cao cung cấp đủ năng lượng nhiệt để các phân tử nitrogen và oxygen chuyển động nhanh hơn, va chạm mạnh hơn, từ đó tăng khả năng phá vỡ liên kết.
8.7. NOx Gây Ảnh Hưởng Gì Đến Môi Trường?
NOx góp phần vào sự hình thành sương mù quang hóa (smog) và mưa acid, gây ảnh hưởng tiêu cực đến chất lượng không khí và sức khỏe của con người, và gây hiệu ứng nhà kính.
8.8. Plasma Có Thể Sử Dụng Để Xúc Tác Phản Ứng Giữa Nitrogen Và Oxygen Không?
Có, plasma là một trạng thái vật chất ionized chứa các hạt mang điện tích, có thể cung cấp năng lượng cần thiết để phá vỡ các liên kết hóa học và xúc tác phản ứng ở nhiệt độ thấp hơn.
8.9. Nồng Độ Nitrogen Và Oxygen Ảnh Hưởng Như Thế Nào Đến Phản Ứng?
Nồng độ cao của nitrogen và oxygen có thể làm tăng tần suất va chạm giữa các phân tử, từ đó tăng tốc độ phản ứng.
8.10. Áp Suất Ảnh Hưởng Như Thế Nào Đến Phản Ứng Giữa Nitrogen Và Oxygen?
Trong trường hợp phản ứng N₂ + O₂ → 2NO, số mol khí không đổi, nên áp suất không có ảnh hưởng đáng kể.
9. Tại Sao Nên Tìm Hiểu Về Xe Tải Tại XETAIMYDINH.EDU.VN?
Nếu bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình, Hà Nội, XETAIMYDINH.EDU.VN là địa chỉ không thể bỏ qua. Chúng tôi cung cấp:
- Thông tin chi tiết và cập nhật: Về các loại xe tải có sẵn, giá cả, và thông số kỹ thuật.
- So sánh khách quan: Giữa các dòng xe khác nhau để bạn dễ dàng lựa chọn.
- Tư vấn chuyên nghiệp: Giúp bạn chọn xe phù hợp với nhu cầu và ngân sách.
- Giải đáp mọi thắc mắc: Liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải.
- Thông tin dịch vụ sửa chữa uy tín: Trong khu vực Mỹ Đình.
Đừng ngần ngại liên hệ với chúng tôi qua:
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
- Hotline: 0247 309 9988.
- Trang web: XETAIMYDINH.EDU.VN.
XETAIMYDINH.EDU.VN luôn sẵn lòng đồng hành cùng bạn trên mọi nẻo đường! Hãy truy cập ngay để khám phá thêm nhiều thông tin hữu ích và nhận được sự hỗ trợ tận tình từ đội ngũ chuyên gia của chúng tôi.