Trong Phân Tử Benzen Có cấu trúc vòng phẳng với 6 nguyên tử cacbon liên kết với nhau, mỗi nguyên tử cacbon liên kết với một nguyên tử hydro và ba liên kết pi (π) liên hợp trải đều trên toàn bộ vòng. Hãy cùng Xe Tải Mỹ Đình khám phá chi tiết hơn về cấu trúc đặc biệt này và những ảnh hưởng của nó đến tính chất hóa học của benzen. Bài viết này sẽ cung cấp cho bạn cái nhìn toàn diện và dễ hiểu nhất về benzen, từ cấu tạo đến ứng dụng thực tế, cùng những lưu ý quan trọng khi sử dụng chất hóa học này.
1. Benzen Là Gì? Tổng Quan Về Hợp Chất Hữu Cơ Benzen
Benzen là một hợp chất hữu cơ thuộc loại hydrocacbon thơm, có dạng lỏng, không màu, dễ bay hơi và có mùi thơm đặc trưng. Benzen không tan trong nước nhưng tan tốt trong các dung môi hữu cơ như ether, rượu và các hydrocacbon khác.
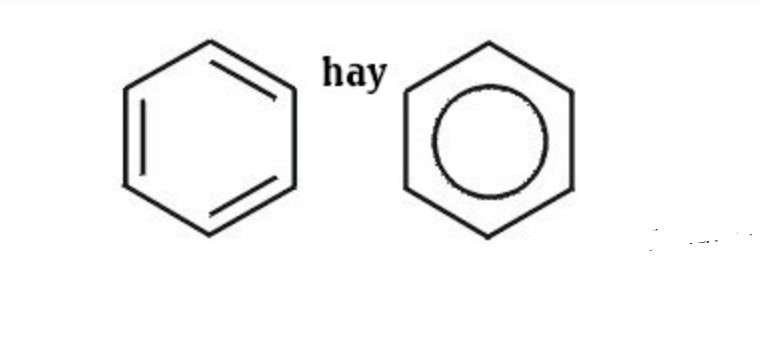 Công thức cấu tạo của benzen
Công thức cấu tạo của benzen
1.1. Đặc Điểm Cấu Tạo Phân Tử Benzen
Phân tử benzen có cấu trúc vòng lục giác đều, với 6 nguyên tử cacbon (C) và 6 nguyên tử hydro (H). Các nguyên tử cacbon liên kết với nhau bằng các liên kết sigma (σ) và pi (π) xen kẽ.
1.2. Công Thức Cấu Tạo và Phân Tử Của Benzen
Công thức phân tử của benzen là C6H6. Công thức cấu tạo của benzen thường được biểu diễn bằng một vòng lục giác đều với một vòng tròn bên trong, thể hiện sự phân bố đều của các electron pi.
1.3. Tính Chất Vật Lý Đặc Trưng Của Benzen
- Trạng thái: Chất lỏng ở điều kiện thường.
- Màu sắc: Không màu.
- Mùi: Mùi thơm đặc trưng.
- Độ tan: Không tan trong nước, tan tốt trong dung môi hữu cơ.
- Khối lượng riêng: Nhẹ hơn nước.
- Độc tính: Độc hại, có thể gây ung thư. Theo báo cáo của Bộ Y tế, tiếp xúc lâu dài với benzen có thể gây ra các bệnh về máu và hệ thần kinh.
2. Cấu Trúc Chi Tiết Phân Tử Benzen: “Trong Phân Tử Benzen Có” Gì Đặc Biệt?
Để hiểu rõ hơn về benzen, chúng ta cần đi sâu vào cấu trúc phân tử của nó. Vậy, trong phân tử benzen có những yếu tố nào tạo nên tính chất đặc biệt của hợp chất này?
2.1. Các Nguyên Tử Cacbon Trong Vòng Benzen
- Số lượng: 6 nguyên tử cacbon.
- Trạng thái lai hóa: Mỗi nguyên tử cacbon ở trạng thái lai hóa sp2. Trạng thái lai hóa sp2 cho phép mỗi nguyên tử cacbon tạo ra 3 liên kết sigma (σ) và 1 obitan p không lai hóa.
- Vị trí: Các nguyên tử cacbon liên kết với nhau tạo thành một vòng lục giác đều.
2.2. Các Nguyên Tử Hydro Liên Kết Với Vòng Benzen
- Số lượng: 6 nguyên tử hydro.
- Vị trí: Mỗi nguyên tử cacbon liên kết với một nguyên tử hydro thông qua liên kết sigma (σ).
- Góc liên kết: Các nguyên tử hydro nằm trên cùng một mặt phẳng với vòng benzen, tạo thành góc 120° so với các liên kết cacbon-cacbon.
2.3. Hệ Thống Liên Kết Pi (π) Liên Hợp Trong Phân Tử Benzen
- Số lượng: 3 liên kết pi (π).
- Cấu trúc: Các obitan p không lai hóa của 6 nguyên tử cacbon xen phủ bên tạo thành một hệ thống liên kết pi (π) liên hợp, trải đều trên toàn bộ vòng benzen.
- Tính chất: Hệ thống liên kết pi (π) liên hợp này làm cho phân tử benzen trở nên bền vững hơn so với các anken thông thường. Theo nghiên cứu của Đại học Quốc gia Hà Nội, hệ thống pi liên hợp là yếu tố quyết định tính thơm của benzen.
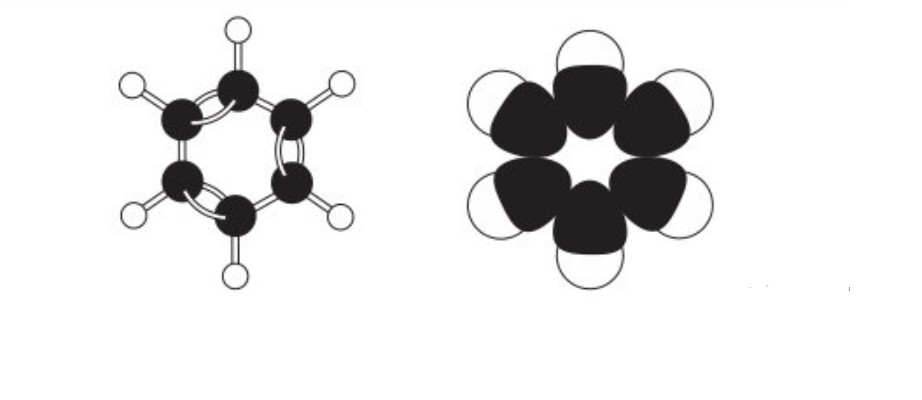 Mô hình phân tử benzen
Mô hình phân tử benzen
2.4. Độ Dài Liên Kết Trong Vòng Benzen
Độ dài liên kết cacbon-cacbon trong benzen là 0.139 nm, nằm giữa độ dài liên kết đơn (0.154 nm) và liên kết đôi (0.134 nm). Điều này chứng tỏ rằng các liên kết trong benzen không phải là liên kết đơn hay liên kết đôi thực sự, mà là sự trung hòa giữa hai loại liên kết này do hiệu ứng liên hợp.
3. Ý Nghĩa Của Cấu Trúc Phân Tử Benzen Đến Tính Chất Hóa Học
Cấu trúc đặc biệt của benzen ảnh hưởng lớn đến tính chất hóa học của nó. Benzen có tính bền vững cao và tham gia các phản ứng theo cơ chế thế electrophile, thay vì cộng như các anken.
3.1. Tính Bền Vững Của Vòng Benzen
Hệ thống liên kết pi (π) liên hợp làm cho vòng benzen trở nên rất bền vững, khó bị phá vỡ. Năng lượng cộng hưởng của benzen là khoảng 150 kJ/mol, cao hơn nhiều so với các anken thông thường.
3.2. Phản Ứng Thế Electrophile Đặc Trưng Của Benzen
Do tính bền vững cao, benzen khó tham gia phản ứng cộng. Thay vào đó, benzen thường tham gia các phản ứng thế electrophile, trong đó một nguyên tử hydro trên vòng benzen bị thay thế bởi một nhóm thế electrophile.
- Phản ứng halogen hóa: Benzen phản ứng với halogen (ví dụ: Cl2, Br2) khi có xúc tác FeX3 (X là Cl hoặc Br) tạo thành halogenbenzen và HX.
- Phản ứng nitro hóa: Benzen phản ứng với hỗn hợp HNO3 đặc và H2SO4 đặc tạo thành nitrobenzen và H2O.
- Phản ứng sulfon hóa: Benzen phản ứng với H2SO4 đặc tạo thành benzenesulfonic acid và H2O.
- Phản ứng ankyl hóa và acyl hóa Friedel-Crafts: Benzen phản ứng với alkyl halogen hoặc acyl halogen khi có xúc tác AlCl3 tạo thành alkylbenzen hoặc acylbenzen và HX.
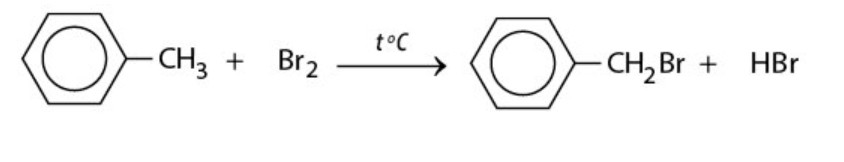
 Phản ứng thế electrophile của benzen
Phản ứng thế electrophile của benzen
3.3. Khả Năng Tham Gia Phản Ứng Cộng Trong Điều Kiện Khắc Nghiệt
Trong điều kiện khắc nghiệt (nhiệt độ cao, áp suất lớn, xúc tác mạnh), benzen cũng có thể tham gia phản ứng cộng.
- Phản ứng cộng hydro: Benzen cộng hydro tạo thành cyclohexane.
- Phản ứng cộng clo: Benzen cộng clo tạo thành hexachlorocyclohexane (thuốc trừ sâu 666).
4. Benzen Và Các Ứng Dụng Quan Trọng Trong Đời Sống Và Công Nghiệp
Benzen là một hóa chất công nghiệp quan trọng, được sử dụng rộng rãi trong nhiều lĩnh vực khác nhau. Tuy nhiên, cần lưu ý rằng benzen là một chất độc hại và cần được sử dụng cẩn thận.
4.1. Ứng Dụng Của Benzen Trong Sản Xuất Hóa Chất
Benzen là nguyên liệu để sản xuất nhiều hóa chất quan trọng, bao gồm:
- Styrene: Dùng để sản xuất polystyrene, một loại nhựa nhiệt dẻo được sử dụng rộng rãi trong sản xuất đồ gia dụng, vật liệu cách nhiệt và bao bì.
- Phenol: Dùng để sản xuất nhựa phenolic, epoxy và các hóa chất khác.
- Aniline: Dùng để sản xuất thuốc nhuộm, dược phẩm và các hóa chất khác.
- Cyclohexane: Dùng để sản xuất nylon, một loại polymer được sử dụng trong sản xuất sợi, vải và các sản phẩm khác.
4.2. Benzen Là Dung Môi Trong Công Nghiệp
Benzen được sử dụng làm dung môi trong nhiều quy trình công nghiệp, đặc biệt là trong sản xuất sơn, mực in, chất kết dính và các sản phẩm khác. Tuy nhiên, do độc tính cao, việc sử dụng benzen làm dung môi đang dần được thay thế bằng các dung môi ít độc hại hơn.
4.3. Benzen Trong Sản Xuất Dược Phẩm Và Thuốc Trừ Sâu
Benzen là một thành phần quan trọng trong sản xuất nhiều loại dược phẩm và thuốc trừ sâu. Tuy nhiên, việc sử dụng benzen trong các sản phẩm này cần được kiểm soát chặt chẽ để đảm bảo an toàn cho sức khỏe con người và môi trường.
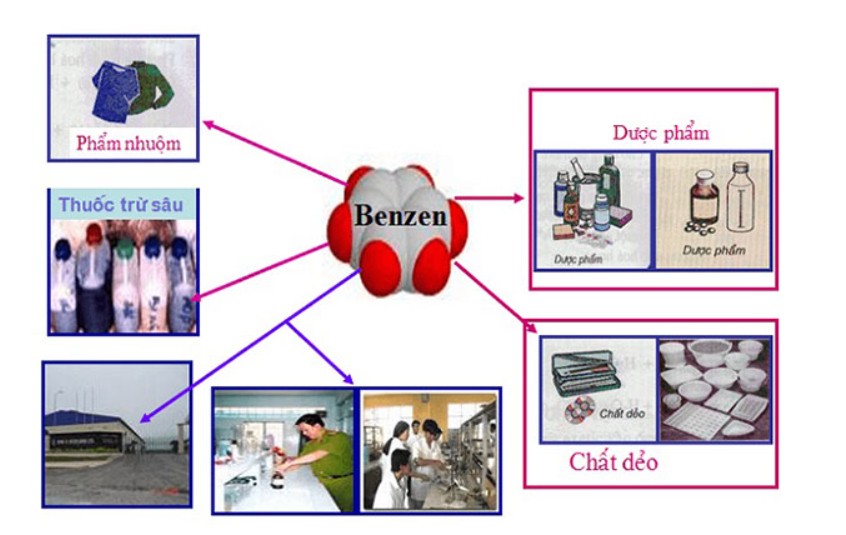 Ứng dụng của benzen trong sản xuất
Ứng dụng của benzen trong sản xuất
5. Các Biện Pháp An Toàn Khi Tiếp Xúc Với Benzen
Do độc tính cao, việc tiếp xúc với benzen cần được thực hiện một cách cẩn thận và tuân thủ các biện pháp an toàn.
5.1. Trang Bị Bảo Hộ Cá Nhân Khi Làm Việc Với Benzen
Khi làm việc với benzen, cần trang bị đầy đủ các thiết bị bảo hộ cá nhân, bao gồm:
- Găng tay: Găng tay chịu hóa chất để bảo vệ da khỏi tiếp xúc trực tiếp với benzen.
- Kính bảo hộ: Kính bảo hộ để bảo vệ mắt khỏi hơi benzen.
- Khẩu trang: Khẩu trang có khả năng lọc hơi hữu cơ để bảo vệ hệ hô hấp.
- Quần áo bảo hộ: Quần áo bảo hộ để bảo vệ cơ thể khỏi tiếp xúc với benzen.
5.2. Đảm Bảo Thông Gió Tốt Trong Khu Vực Làm Việc
Khu vực làm việc với benzen cần được thông gió tốt để giảm nồng độ hơi benzen trong không khí. Nên sử dụng hệ thống thông gió cục bộ để loại bỏ hơi benzen ngay tại nguồn phát sinh.
5.3. Lưu Trữ Benzen Đúng Cách Để Tránh Rò Rỉ Và Phát Tán
Benzen cần được lưu trữ trong các容器 kín,放置在通风良好、远离 nguồn nhiệt và chất oxy hóa. Tránh làm đổ, vỡ容器chứa benzen.
5.4. Xử Lý Sự Cố Khi Tiếp Xúc Với Benzen
- Tiếp xúc qua da: Rửa kỹ vùng da bị tiếp xúc với benzen bằng xà phòng và nước sạch.
- Tiếp xúc qua mắt: Rửa mắt ngay lập tức bằng nước sạch trong ít nhất 15 phút.
- Hít phải hơi benzen: Di chuyển nạn nhân đến nơi thoáng khí và cung cấp oxy nếu cần thiết.
- Nuốt phải benzen: Không gây nôn. Đưa nạn nhân đến cơ sở y tế gần nhất để được điều trị.
6. Nhận Biết Các Đồng Đẳng Của Benzen
Đồng đẳng của benzen là các hợp chất hữu cơ có cấu trúc tương tự benzen, trong đó một hoặc nhiều nguyên tử hydro trên vòng benzen được thay thế bằng các nhóm alkyl. Các đồng đẳng phổ biến của benzen bao gồm toluene, xylene và ethylbenzene.
6.1. Toluene (C7H8)
Toluene là một chất lỏng không màu, có mùi thơm nhẹ và được sử dụng làm dung môi và nguyên liệu để sản xuất nhiều hóa chất khác.
 Công thức cấu tạo của toluene
Công thức cấu tạo của toluene
6.2. Xylene (C8H10)
Xylene là một hỗn hợp của ba đồng phân cấu trúc: ortho-xylene, meta-xylene và para-xylene. Xylene được sử dụng làm dung môi và nguyên liệu để sản xuất nhựa polyester và các hóa chất khác.
6.3. Ethylbenzene (C8H10)
Ethylbenzene là một chất lỏng không màu, có mùi thơm nhẹ và được sử dụng chủ yếu để sản xuất styrene.
7. Phân Biệt Benzen Với Các Hợp Chất Thơm Khác
Benzen là một hydrocacbon thơm đơn giản nhất, trong khi các hợp chất thơm khác có thể chứa nhiều vòng benzen hoặc các dị vòng. Các hợp chất thơm khác bao gồm naphthalene, anthracene và pyridine.
7.1. Naphthalene (C10H8)
Naphthalene là một chất rắn màu trắng, có mùi đặc trưng và được sử dụng trong sản xuất thuốc nhuộm và thuốc trừ sâu.
7.2. Anthracene (C14H10)
Anthracene là một chất rắn màu vàng, có huỳnh quang và được sử dụng trong sản xuất thuốc nhuộm và nhựa.
7.3. Pyridine (C5H5N)
Pyridine là một chất lỏng không màu, có mùi khó chịu và được sử dụng làm dung môi và nguyên liệu để sản xuất dược phẩm và hóa chất khác.
8. Các Câu Hỏi Thường Gặp Về Benzen (FAQ)
8.1. Benzen Có Tan Trong Nước Không?
Không, benzen không tan trong nước do tính chất không phân cực của nó.
8.2. Benzen Có Độc Không?
Có, benzen là một chất độc hại và có thể gây ung thư.
8.3. Benzen Được Sử Dụng Để Làm Gì?
Benzen được sử dụng làm nguyên liệu để sản xuất nhiều hóa chất quan trọng, làm dung môi trong công nghiệp và trong sản xuất dược phẩm và thuốc trừ sâu.
8.4. Làm Thế Nào Để Bảo Vệ Bản Thân Khi Tiếp Xúc Với Benzen?
Cần trang bị đầy đủ các thiết bị bảo hộ cá nhân, đảm bảo thông gió tốt trong khu vực làm việc và lưu trữ benzen đúng cách.
8.5. Benzen Có Thể Gây Ra Những Bệnh Gì?
Tiếp xúc lâu dài với benzen có thể gây ra các bệnh về máu (ví dụ: лейкемия), hệ thần kinh và các cơ quan khác.
8.6. Benzen Có Tồn Tại Trong Tự Nhiên Không?
Benzen có thể được tìm thấy trong dầu thô, khí đốt tự nhiên và một số loại thực vật.
8.7. Benzen Có Gây Ô Nhiễm Môi Trường Không?
Có, benzen có thể gây ô nhiễm môi trường nếu không được xử lý đúng cách.
8.8. Benzen Có Thể Thay Thế Bằng Chất Gì An Toàn Hơn Không?
Trong nhiều ứng dụng, benzen có thể được thay thế bằng các dung môi ít độc hại hơn như toluene, xylene hoặc các dung môi aliphatic.
8.9. Cấu trúc vòng benzen có đặc điểm gì nổi bật?
Cấu trúc vòng benzen có đặc điểm nổi bật là tính liên hợp cao của các liên kết pi, tạo nên tính thơm và độ bền vững đặc biệt cho phân tử.
8.10. Làm thế nào để nhận biết benzen trong phòng thí nghiệm?
Benzen có thể được nhận biết thông qua các phản ứng hóa học đặc trưng như phản ứng nitro hóa, halogen hóa hoặc bằng các phương pháp phân tích như sắc ký khí hoặc quang phổ.
Hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích về benzen và trả lời câu hỏi “trong phân tử benzen có” những gì. Nếu bạn cần thêm thông tin hoặc có bất kỳ thắc mắc nào về xe tải hoặc các vấn đề liên quan đến vận tải, đừng ngần ngại liên hệ với Xe Tải Mỹ Đình. Chúng tôi luôn sẵn sàng hỗ trợ bạn.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình?
Hãy truy cập ngay XETAIMYDINH.EDU.VN để được tư vấn và giải đáp mọi thắc mắc. Chúng tôi cung cấp thông tin cập nhật về các loại xe tải, so sánh giá cả và thông số kỹ thuật, giúp bạn lựa chọn xe phù hợp với nhu cầu và ngân sách.
Liên hệ ngay:
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
Xe Tải Mỹ Đình – Đồng hành cùng bạn trên mọi nẻo đường!