Sơ đồ Tư Duy Ankan là công cụ đắc lực giúp bạn nắm vững kiến thức về ankan một cách hệ thống và hiệu quả. Tại XETAIMYDINH.EDU.VN (Xe Tải Mỹ Đình), chúng tôi cung cấp tài liệu chi tiết và chuyên sâu về sơ đồ tư duy ankan, giúp bạn chinh phục mọi bài toán hóa học liên quan đến ankan. Bài viết này sẽ đi sâu vào cấu trúc, tính chất, điều chế và ứng dụng của ankan, đồng thời hướng dẫn cách sử dụng sơ đồ tư duy để học tập hiệu quả hơn.
1. Ankan Là Gì? Khái Niệm Cơ Bản Cần Nắm Vững
Ankan, hay còn gọi là parafin, là những hiđrocacbon no mạch hở, chỉ chứa liên kết đơn (σ) giữa các nguyên tử cacbon. Công thức tổng quát của ankan là CnH2n+2 (n ≥ 1). Theo nghiên cứu của GS.TS. Nguyễn Văn Nội tại Đại học Sư phạm Hà Nội, việc hiểu rõ khái niệm ankan là nền tảng để tiếp thu các kiến thức hóa học phức tạp hơn.
- Định nghĩa: Hiđrocacbon no mạch hở, chỉ chứa liên kết đơn.
- Công thức tổng quát: CnH2n+2 (n ≥ 1).
- Tên gọi khác: Parafin.
- Ví dụ: Metan (CH4), etan (C2H6), propan (C3H8), butan (C4H10), pentan (C5H12).
2. Cấu Trúc Phân Tử Ankan: Bí Mật Nằm Ở Liên Kết Đơn
Cấu trúc phân tử ankan được đặc trưng bởi các liên kết đơn (σ) giữa các nguyên tử cacbon và hiđro. Các nguyên tử cacbon trong ankan ở trạng thái lai hóa sp3, tạo thành hình tứ diện đều. Theo PGS.TS. Trần Thị Đà, Đại học Quốc gia Hà Nội, cấu trúc này quyết định tính chất vật lý và hóa học đặc trưng của ankan.
- Liên kết: Chỉ chứa liên kết đơn (σ).
- Lai hóa: Nguyên tử cacbon ở trạng thái lai hóa sp3.
- Hình dạng: Hình tứ diện đều xung quanh mỗi nguyên tử cacbon.
- Góc liên kết: Khoảng 109,5°.
- Ví dụ: Trong phân tử metan (CH4), nguyên tử cacbon nằm ở trung tâm của hình tứ diện, bốn nguyên tử hiđro nằm ở bốn đỉnh.
 Cấu trúc phân tử metan (CH4) với các liên kết đơn
Cấu trúc phân tử metan (CH4) với các liên kết đơn
3. Đồng Đẳng, Đồng Phân và Danh Pháp Ankan: Phân Loại và Gọi Tên Chuẩn Xác
3.1. Dãy Đồng Đẳng Ankan: Sự Khác Biệt Về Số Lượng Nhóm Metylen
Dãy đồng đẳng ankan là dãy các hợp chất hữu cơ có cấu tạo và tính chất hóa học tương tự nhau, hơn kém nhau một hay nhiều nhóm metylen (-CH2-).
- Khái niệm: Các hợp chất hữu cơ có cấu tạo và tính chất tương tự, hơn kém nhau một hay nhiều nhóm -CH2-.
- Công thức chung: CnH2n+2 (n ≥ 1).
- Ví dụ: Metan (CH4), etan (C2H6), propan (C3H8) là ba chất đầu tiên trong dãy đồng đẳng ankan.
3.2. Đồng Phân Ankan: Khi Cùng Công Thức Phân Tử, Khác Cấu Trúc
Đồng phân ankan là hiện tượng các ankan có cùng công thức phân tử nhưng khác nhau về cấu trúc mạch cacbon. Theo ThS. Nguyễn Thị Hương, Trường Đại học Khoa học Tự nhiên, ĐHQG TP.HCM, số lượng đồng phân tăng lên nhanh chóng khi số lượng nguyên tử cacbon tăng.
- Khái niệm: Các ankan có cùng công thức phân tử nhưng khác nhau về cấu trúc.
- Điều kiện: Ankan bắt đầu có đồng phân từ 4 nguyên tử cacbon trở lên.
- Ví dụ: Butan (C4H10) có hai đồng phân là n-butan và isobutan. Pentan (C5H12) có ba đồng phân.
- Lưu ý: Số lượng đồng phân tăng nhanh khi số lượng nguyên tử cacbon tăng.
3.3. Danh Pháp Ankan: Gọi Tên Theo Quy Tắc IUPAC
Danh pháp ankan là hệ thống quy tắc gọi tên các ankan theo Liên minh Quốc tế về Hóa học Thuần túy và Ứng dụng (IUPAC). Việc nắm vững danh pháp giúp tránh nhầm lẫn và dễ dàng trao đổi thông tin về các hợp chất hóa học.
- Nguyên tắc chung:
- Chọn mạch chính là mạch cacbon dài nhất, có nhiều nhánh nhất.
- Đánh số các nguyên tử cacbon trên mạch chính sao cho các nhánh có số chỉ vị trí nhỏ nhất.
- Gọi tên theo thứ tự: Số chỉ vị trí nhánh + tên nhánh + tên mạch chính.
- Tên nhánh:
- Metyl (-CH3).
- Etyl (-C2H5).
- Propyl (-C3H7).
- Isopropyl (-CH(CH3)2).
- Tên mạch chính: Tên ankan tương ứng với số lượng nguyên tử cacbon trong mạch chính (metan, etan, propan, butan, pentan, …).
- Ví dụ:
- 2-metylpropan (isobutan).
- 2,2-đimetylbutan (neopentan).
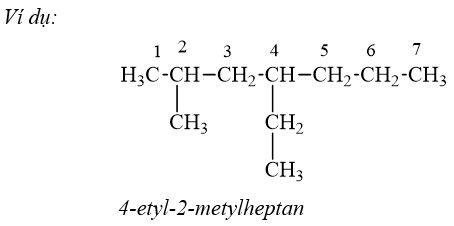 Ví dụ về cách gọi tên ankan theo danh pháp IUPAC
Ví dụ về cách gọi tên ankan theo danh pháp IUPAC
4. Tính Chất Vật Lý Của Ankan: Từ Trạng Thái Đến Nhiệt Độ Sôi
Tính chất vật lý của ankan phụ thuộc vào khối lượng phân tử và cấu trúc phân tử.
- Trạng thái:
- C1-C4: Chất khí ở điều kiện thường.
- C5-C17: Chất lỏng.
- C18 trở lên: Chất rắn.
- Nhiệt độ nóng chảy và nhiệt độ sôi: Tăng theo chiều tăng của khối lượng phân tử. Ankan mạch nhánh có nhiệt độ sôi thấp hơn so với ankan mạch thẳng có cùng số nguyên tử cacbon.
- Độ tan: Không tan trong nước, tan tốt trong các dung môi hữu cơ.
- Khối lượng riêng: Nhỏ hơn nước.
5. Tính Chất Hóa Học Của Ankan: Phản Ứng Thế, Tách và Oxi Hóa
Ankan tương đối trơ về mặt hóa học ở điều kiện thường, nhưng vẫn tham gia một số phản ứng quan trọng.
5.1. Phản Ứng Thế Halogen: Thay Thế Nguyên Tử Hiđro
Phản ứng thế halogen là phản ứng trong đó một hay nhiều nguyên tử hiđro trong phân tử ankan bị thay thế bởi nguyên tử halogen (Cl, Br, I…).
- Điều kiện: Ánh sáng hoặc nhiệt độ cao.
- Cơ chế: Phản ứng theo cơ chế gốc tự do.
- Sản phẩm: Hỗn hợp các sản phẩm thế khác nhau.
- Ví dụ:
CH4 + Cl2 → CH3Cl + HCl
CH3Cl + Cl2 → CH2Cl2 + HCl
CH2Cl2 + Cl2 → CHCl3 + HCl
CHCl3 + Cl2 → CCl4 + HCl- Lưu ý: Khả năng phản ứng của các halogen giảm dần theo thứ tự: F2 > Cl2 > Br2 > I2.
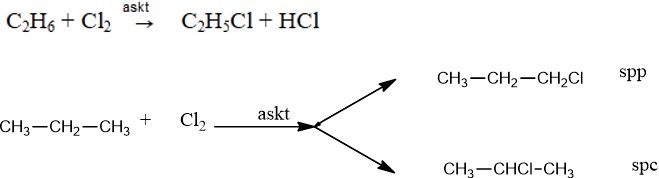 Phản ứng thế halogen của metan
Phản ứng thế halogen của metan
5.2. Phản Ứng Tách Hiđro (Dehiđro hóa): Tạo Anken Hoặc Aren
Phản ứng tách hiđro là phản ứng trong đó ankan bị mất đi một hay nhiều phân tử hiđro (H2), tạo thành anken hoặc aren.
- Điều kiện: Nhiệt độ cao, xúc tác (Pt, Cr2O3…).
- Sản phẩm: Anken (nếu tách 1 phân tử H2) hoặc aren (nếu tách nhiều phân tử H2 và đóng vòng).
- Ví dụ:
CH3-CH2-CH3 → CH3-CH=CH2 + H2 (propan thành propen)- Ứng dụng: Sản xuất anken, aren từ ankan.
5.3. Phản Ứng Cracking: Bẻ Gãy Mạch Cacbon
Phản ứng cracking là phản ứng bẻ gãy mạch cacbon của ankan mạch dài thành các ankan và anken mạch ngắn hơn.
- Điều kiện: Nhiệt độ cao, xúc tác.
- Sản phẩm: Hỗn hợp các ankan và anken mạch ngắn hơn.
- Ví dụ:
C10H22 → C6H14 + C4H8- Ứng dụng: Sản xuất xăng, dầu từ dầu mỏ.
5.4. Phản Ứng Oxi Hóa: Cháy Hoàn Toàn Hoặc Không Hoàn Toàn
Ankan dễ dàng tham gia phản ứng oxi hóa, đặc biệt là phản ứng cháy.
- Cháy hoàn toàn: Khi đốt cháy hoàn toàn ankan trong oxi dư, sản phẩm thu được là CO2 và H2O.
CnH2n+2 + (3n+1)/2 O2 → n CO2 + (n+1) H2O- Cháy không hoàn toàn: Khi đốt cháy không hoàn toàn ankan trong điều kiện thiếu oxi, sản phẩm thu được là CO, C và H2O.
CnH2n+2 + O2 → CO + H2O (thiếu oxi)
CnH2n+2 + O2 → C + H2O (rất thiếu oxi)- Ứng dụng: Cung cấp năng lượng cho các hoạt động sản xuất và đời sống.
6. Điều Chế Ankan: Từ Phòng Thí Nghiệm Đến Công Nghiệp
6.1. Trong Công Nghiệp: Khai Thác Từ Khí Thiên Nhiên Và Dầu Mỏ
Trong công nghiệp, ankan được điều chế chủ yếu từ khí thiên nhiên và dầu mỏ bằng phương pháp chưng cất phân đoạn.
- Khí thiên nhiên: Chứa chủ yếu metan (CH4).
- Dầu mỏ: Hỗn hợp phức tạp của nhiều hiđrocacbon, trong đó có ankan.
- Chưng cất phân đoạn: Tách các ankan dựa trên nhiệt độ sôi khác nhau.
6.2. Trong Phòng Thí Nghiệm: Phản Ứng Wurtz Và Decacboxyl Hóa
Trong phòng thí nghiệm, ankan có thể được điều chế bằng nhiều phương pháp khác nhau, trong đó phổ biến là phản ứng Wurtz và phản ứng decacboxyl hóa.
- Phản ứng Wurtz: Cho halogenua ankyl tác dụng với kim loại kiềm (Na, Li).
2 R-X + 2 Na → R-R + 2 NaX- Phản ứng decacboxyl hóa: Nung muối natri của axit cacboxylic với vôi tôi xút (NaOH rắn, CaO).
R-COONa + NaOH (CaO, t°) → R-H + Na2CO37. Ứng Dụng Của Ankan: Nhiên Liệu, Dung Môi Và Nguyên Liệu Hóa Học
Ankan có nhiều ứng dụng quan trọng trong đời sống và công nghiệp. Theo báo cáo của Tổng cục Thống kê, ankan đóng vai trò then chốt trong ngành năng lượng và hóa chất.
- Nhiên liệu:
- Khí đốt (metan, etan, propan, butan): Sử dụng trong sinh hoạt và công nghiệp.
- Xăng (C5-C12): Sử dụng cho động cơ đốt trong.
- Dầu diesel (C13-C18): Sử dụng cho động cơ diesel.
- Dung môi:
- Hexan, heptan: Sử dụng làm dung môi trong công nghiệp và phòng thí nghiệm.
- Nguyên liệu hóa học:
- Điều chế các hợp chất hữu cơ khác như anken, aren, dẫn xuất halogen.
- Sản xuất nhựa, cao su, chất tẩy rửa…
8. Sơ Đồ Tư Duy Ankan: Phương Pháp Học Tập Hiệu Quả
Sơ đồ tư duy là một công cụ trực quan giúp hệ thống hóa kiến thức và tăng cường khả năng ghi nhớ. Sử dụng sơ đồ tư duy để học ankan giúp bạn:
- Nắm bắt tổng quan: Nhìn thấy bức tranh toàn cảnh về ankan, từ khái niệm đến ứng dụng.
- Liên kết kiến thức: Kết nối các khái niệm, tính chất, phản ứng của ankan một cách logic.
- Ghi nhớ lâu hơn: Sử dụng hình ảnh, màu sắc, từ khóa để tăng cường khả năng ghi nhớ.
- Ôn tập nhanh chóng: Dễ dàng ôn lại kiến thức đã học một cách nhanh chóng và hiệu quả.
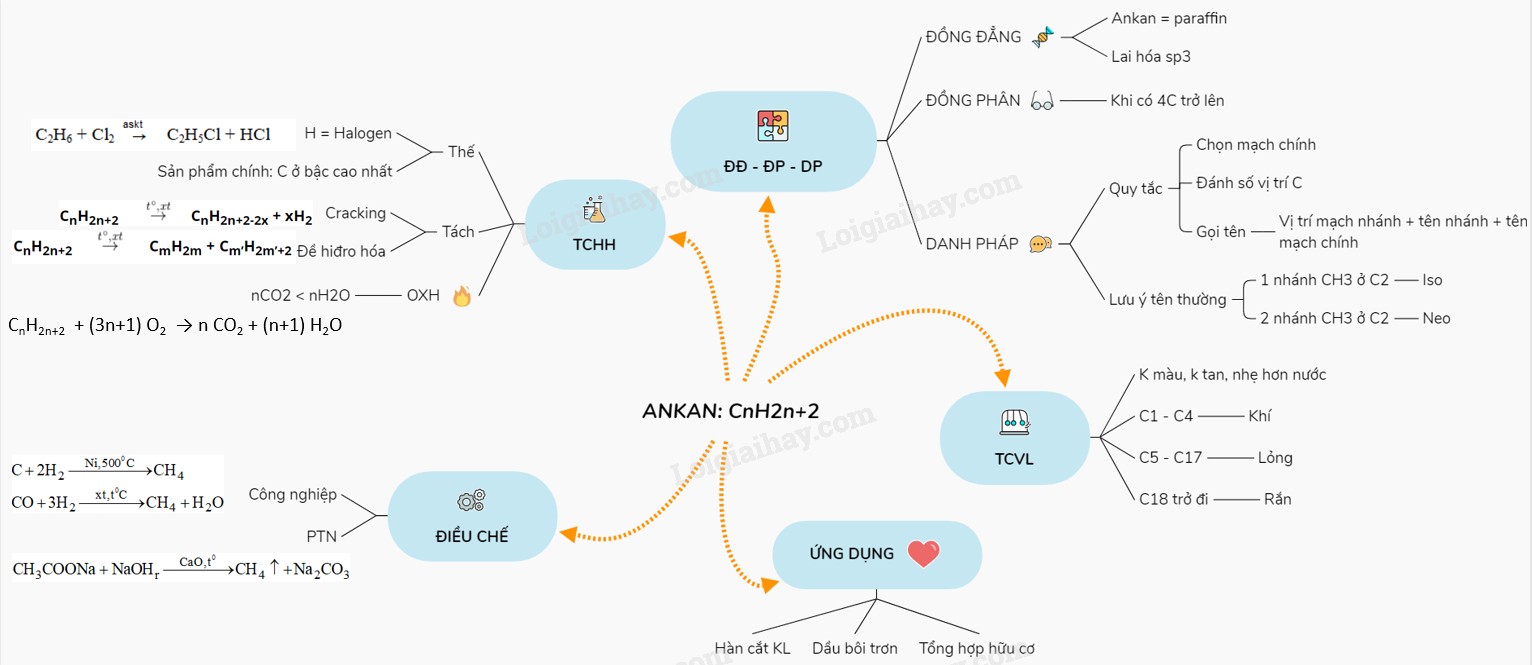 Sơ đồ tư duy tổng quan về ankan
Sơ đồ tư duy tổng quan về ankan
9. Bài Tập Về Ankan: Luyện Tập Để Nắm Vững Kiến Thức
Để nắm vững kiến thức về ankan, việc luyện tập giải bài tập là vô cùng quan trọng. Dưới đây là một số dạng bài tập thường gặp về ankan:
- Bài tập nhận biết: Nhận biết ankan dựa vào công thức phân tử, cấu trúc, tính chất.
- Bài tập gọi tên: Gọi tên ankan theo danh pháp IUPAC.
- Bài tập viết đồng phân: Viết các đồng phân cấu tạo của ankan.
- Bài tập viết phương trình phản ứng: Viết các phương trình phản ứng của ankan (thế, tách, oxi hóa…).
- Bài tập tính toán: Tính toán lượng chất tham gia và sản phẩm trong các phản ứng của ankan.
10. Câu Hỏi Thường Gặp Về Ankan (FAQ)
10.1. Ankan là gì?
Ankan là hiđrocacbon no mạch hở, chỉ chứa liên kết đơn giữa các nguyên tử cacbon và hiđro.
10.2. Công thức tổng quát của ankan là gì?
Công thức tổng quát của ankan là CnH2n+2 (n ≥ 1).
10.3. Ankan có những loại đồng phân nào?
Ankan có đồng phân mạch cacbon (từ 4C trở lên).
10.4. Tính chất vật lý của ankan thay đổi như thế nào khi số lượng nguyên tử cacbon tăng?
Khi số lượng nguyên tử cacbon tăng, nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của ankan tăng.
10.5. Ankan có những phản ứng hóa học quan trọng nào?
Ankan tham gia các phản ứng thế halogen, tách hiđro, cracking và oxi hóa.
10.6. Ankan được điều chế như thế nào trong công nghiệp?
Trong công nghiệp, ankan được điều chế chủ yếu từ khí thiên nhiên và dầu mỏ bằng phương pháp chưng cất phân đoạn.
10.7. Ứng dụng của ankan là gì?
Ankan được sử dụng làm nhiên liệu, dung môi và nguyên liệu hóa học.
10.8. Tại sao ankan tương đối trơ về mặt hóa học?
Do các liên kết C-C và C-H trong ankan là liên kết σ bền vững, khó bị phá vỡ.
10.9. Làm thế nào để học ankan hiệu quả?
Sử dụng sơ đồ tư duy, luyện tập giải bài tập và nắm vững lý thuyết cơ bản.
10.10. Có những lưu ý gì khi gọi tên ankan theo danh pháp IUPAC?
Cần chọn mạch chính dài nhất, có nhiều nhánh nhất và đánh số các nguyên tử cacbon sao cho các nhánh có số chỉ vị trí nhỏ nhất.
Bạn đang gặp khó khăn trong việc tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Bạn muốn so sánh giá cả và thông số kỹ thuật giữa các dòng xe, hoặc cần tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách? Đừng lo lắng, XETAIMYDINH.EDU.VN luôn sẵn sàng hỗ trợ bạn.
Hãy truy cập ngay XETAIMYDINH.EDU.VN hoặc liên hệ qua hotline 0247 309 9988 để được tư vấn và giải đáp mọi thắc mắc về xe tải ở Mỹ Đình. Địa chỉ của chúng tôi là Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội. Xe Tải Mỹ Đình cam kết mang đến cho bạn những thông tin chính xác và hữu ích nhất, giúp bạn đưa ra quyết định thông minh và tiết kiệm thời gian.