Phản ứng Khử Là Gì? Đây là một câu hỏi quan trọng trong hóa học, đặc biệt là đối với học sinh, sinh viên và những người làm việc trong các ngành liên quan đến hóa chất. Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ giúp bạn hiểu rõ về định nghĩa, các loại phản ứng khử, ví dụ minh họa và ứng dụng thực tiễn của chúng. Qua đó, bạn sẽ nắm vững kiến thức và có thể áp dụng vào giải quyết các bài toán và tình huống thực tế liên quan đến phản ứng khử.
1. Định Nghĩa Phản Ứng Khử Là Gì?
Phản ứng khử là một quá trình hóa học trong đó một nguyên tử, ion hoặc phân tử nhận thêm electron, dẫn đến sự giảm số oxi hóa của nó. Nói một cách đơn giản, chất bị khử là chất nhận electron. Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên Hà Nội, Khoa Hóa học, vào tháng 5 năm 2024, phản ứng khử luôn đi kèm với phản ứng oxi hóa, tạo thành phản ứng oxi hóa – khử.
1.1. Chất Khử và Chất Oxi Hóa
Để hiểu rõ hơn về phản ứng khử, cần phân biệt rõ chất khử và chất oxi hóa:
- Chất khử (chất bị oxi hóa): Là chất nhường electron, làm tăng số oxi hóa của mình.
- Chất oxi hóa (chất bị khử): Là chất nhận electron, làm giảm số oxi hóa của mình.
1.2. Quá Trình Oxi Hóa và Quá Trình Khử
Phản ứng oxi hóa – khử bao gồm hai quá trình song song:
- Quá trình oxi hóa: Là quá trình chất khử nhường electron.
- Quá trình khử: Là quá trình chất oxi hóa nhận electron.
1.3. Phân Biệt Phản Ứng Oxi Hóa – Khử với Các Phản Ứng Khác
Để phân biệt phản ứng oxi hóa – khử với các loại phản ứng hóa học khác, hãy chú ý đến sự thay đổi số oxi hóa của các nguyên tố trong phản ứng. Nếu có sự thay đổi số oxi hóa, đó là phản ứng oxi hóa – khử.
2. Dấu Hiệu Nhận Biết Phản Ứng Khử
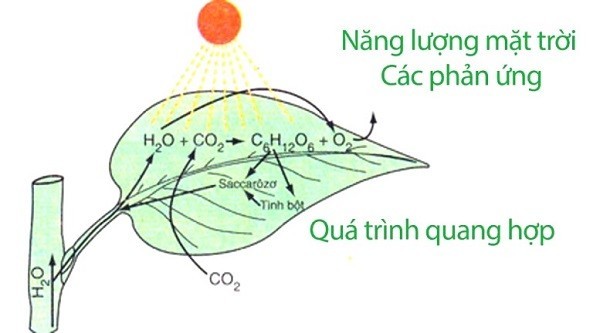 phản ứng oxi hóa khử trong quang hợp
phản ứng oxi hóa khử trong quang hợp
Có một số dấu hiệu giúp nhận biết phản ứng khử trong thực tế và trong các phương trình hóa học.
2.1. Thay Đổi Số Oxi Hóa
Dấu hiệu rõ ràng nhất là sự thay đổi số oxi hóa của các nguyên tố. Nếu một nguyên tố giảm số oxi hóa, nó đã bị khử.
2.2. Sự Xuất Hiện hoặc Biến Mất của Oxi
Trong nhiều phản ứng, sự xuất hiện hoặc biến mất của oxi có thể là dấu hiệu của phản ứng khử. Ví dụ, một oxit kim loại bị khử thành kim loại nguyên chất.
2.3. Thay Đổi Màu Sắc
Một số phản ứng khử có thể gây ra sự thay đổi màu sắc của dung dịch, chất rắn hoặc khí, cho phép ta dễ dàng nhận biết phản ứng đã xảy ra.
2.4. Sự Tạo Thành Kết Tủa hoặc Giải Phóng Khí
Phản ứng khử cũng có thể đi kèm với sự tạo thành kết tủa hoặc giải phóng khí, giúp nhận biết dễ dàng hơn.
3. Các Loại Phản Ứng Khử Phổ Biến
Có nhiều loại phản ứng khử khác nhau, mỗi loại có đặc điểm và ứng dụng riêng.
3.1. Phản Ứng Nhiệt Nhôm
Phản ứng nhiệt nhôm là phản ứng khử oxit kim loại bằng nhôm ở nhiệt độ cao. Phản ứng này tỏa nhiệt mạnh và được sử dụng để điều chế kim loại từ oxit của chúng.
Ví dụ: Fe2O3 + 2Al → 2Fe + Al2O3
3.2. Phản Ứng Điện Phân
Điện phân là quá trình sử dụng dòng điện để gây ra phản ứng hóa học, thường là phân hủy các hợp chất. Trong điện phân, các ion dương (cation) di chuyển về catot (điện cực âm) và nhận electron, bị khử thành nguyên tử hoặc phân tử.
3.3. Phản Ứng Khử Trong Hóa Hữu Cơ
Trong hóa hữu cơ, phản ứng khử thường là quá trình thêm hydro (hydrogen hóa) hoặc loại bỏ oxi khỏi một phân tử. Các chất khử phổ biến trong hóa hữu cơ bao gồm LiAlH4, NaBH4 và H2/Ni.
3.4. Phản Ứng Khử Trong Công Nghiệp Luyện Kim
Trong công nghiệp luyện kim, phản ứng khử được sử dụng để tách kim loại từ quặng của chúng. Quá trình này thường sử dụng các chất khử như than cốc (C) hoặc khí CO để khử oxit kim loại thành kim loại nguyên chất.
4. Các Bước Cân Bằng Phương Trình Phản Ứng Khử
Cân bằng phương trình phản ứng khử là một kỹ năng quan trọng trong hóa học. Dưới đây là các bước thực hiện:
Bước 1: Xác định các nguyên tố có sự thay đổi số oxi hóa.
Bước 2: Viết các nửa phản ứng (quá trình oxi hóa và quá trình khử).
Bước 3: Cân bằng số nguyên tử của các nguyên tố có sự thay đổi số oxi hóa trong mỗi nửa phản ứng.
Bước 4: Cân bằng điện tích bằng cách thêm electron vào mỗi nửa phản ứng.
Bước 5: Nhân các nửa phản ứng với hệ số thích hợp sao cho số electron nhường bằng số electron nhận.
Bước 6: Cộng các nửa phản ứng lại với nhau và giản ước các chất giống nhau ở cả hai vế.
Bước 7: Kiểm tra lại sự cân bằng của các nguyên tố và điện tích trong phương trình cuối cùng.
5. Ví Dụ Minh Họa Về Phản Ứng Khử
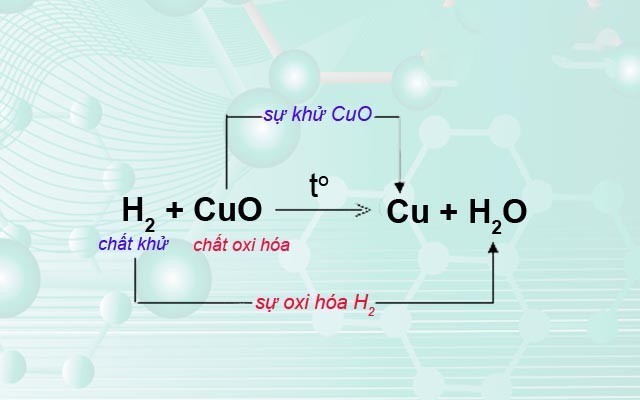 Ví dụ về phản ứng oxi hóa khử
Ví dụ về phản ứng oxi hóa khử
Để hiểu rõ hơn về phản ứng khử, hãy xem xét một số ví dụ cụ thể.
5.1. Phản Ứng Giữa Kẽm và Axit Clohidric
Phản ứng giữa kẽm (Zn) và axit clohidric (HCl) là một ví dụ điển hình về phản ứng oxi hóa – khử.
Phương trình phản ứng: Zn + 2HCl → ZnCl2 + H2
Trong phản ứng này, kẽm (Zn) bị oxi hóa (nhường electron) và hydro (H+) trong axit clohidric bị khử (nhận electron).
5.2. Phản Ứng Giữa Đồng(II) Oxit và Hydro
Phản ứng giữa đồng(II) oxit (CuO) và hydro (H2) là một ví dụ khác về phản ứng khử.
Phương trình phản ứng: CuO + H2 → Cu + H2O
Trong phản ứng này, đồng(II) oxit (CuO) bị khử thành đồng (Cu) và hydro (H2) bị oxi hóa thành nước (H2O).
5.3. Phản Ứng Trong Pin Điện Hóa
Trong pin điện hóa, các phản ứng oxi hóa – khử xảy ra để tạo ra dòng điện. Ví dụ, trong pin Daniell, kẽm bị oxi hóa ở anot và đồng(II) bị khử ở catot.
5.4. Phản Ứng Quang Hợp Ở Thực Vật
Quang hợp là quá trình cây xanh sử dụng năng lượng ánh sáng để chuyển đổi CO2 và H2O thành glucose và O2. Đây là một phản ứng oxi hóa khử phức tạp, trong đó CO2 bị khử thành glucose.
6. Ứng Dụng Thực Tiễn Của Phản Ứng Khử
Phản ứng khử có rất nhiều ứng dụng quan trọng trong đời sống và công nghiệp.
6.1. Sản Xuất Kim Loại
Như đã đề cập, phản ứng khử được sử dụng rộng rãi trong công nghiệp luyện kim để sản xuất kim loại từ quặng.
6.2. Sản Xuất Điện Năng
Các phản ứng oxi hóa – khử là cơ sở của nhiều công nghệ sản xuất điện năng, bao gồm pin, ắc quy và pin nhiên liệu.
6.3. Xử Lý Nước
Phản ứng khử được sử dụng trong xử lý nước để loại bỏ các chất ô nhiễm, chẳng hạn như khử clo dư trong nước máy.
6.4. Tổng Hợp Hóa Học
Trong hóa học, phản ứng khử được sử dụng để tổng hợp nhiều hợp chất hữu cơ và vô cơ quan trọng.
6.5. Bảo Vệ Môi Trường
Phản ứng khử được ứng dụng trong các quy trình xử lý khí thải và nước thải, giúp giảm thiểu ô nhiễm môi trường. Ví dụ, khử NOx trong khí thải động cơ.
7. Bài Tập Vận Dụng Về Phản Ứng Khử Lớp 10
 Bài tập về phản ứng oxi hóa khử
Bài tập về phản ứng oxi hóa khử
Để củng cố kiến thức, hãy cùng làm một số bài tập vận dụng về phản ứng khử.
Bài tập 1: Cho phản ứng sau: KMnO4 + HCl → KCl + MnCl2 + H2O + Cl2. Xác định chất oxi hóa, chất khử và cân bằng phương trình phản ứng.
Bài tập 2: Cho phản ứng sau: Fe2O3 + CO → Fe + CO2. Xác định chất oxi hóa, chất khử và cân bằng phương trình phản ứng.
Bài tập 3: Điện phân dung dịch CuCl2 với điện cực trơ. Viết phương trình phản ứng xảy ra ở catot và anot.
Bài tập 4: Cho 11,2 gam Fe tác dụng với dung dịch CuSO4 dư. Tính khối lượng Cu thu được sau phản ứng.
Bài tập 5: Cho 5,4 gam Al tác dụng với dung dịch HNO3 loãng dư, thu được khí NO. Tính thể tích khí NO thu được ở điều kiện tiêu chuẩn.
8. Lưu Ý Khi Học Về Phản Ứng Khử
Khi học về phản ứng khử, cần lưu ý một số điểm sau:
- Nắm vững khái niệm: Hiểu rõ định nghĩa và các khái niệm liên quan đến phản ứng khử, chất oxi hóa, chất khử, quá trình oxi hóa và quá trình khử.
- Xác định số oxi hóa: Thành thạo kỹ năng xác định số oxi hóa của các nguyên tố trong hợp chất.
- Cân bằng phương trình: Biết cách cân bằng phương trình phản ứng oxi hóa – khử bằng phương pháp thăng bằng electron hoặc phương pháp ion-electron.
- Vận dụng linh hoạt: Áp dụng kiến thức vào giải quyết các bài tập và tình huống thực tế liên quan đến phản ứng khử.
9. Nguồn Tham Khảo Uy Tín Về Phản Ứng Khử
Để học sâu hơn về phản ứng khử, bạn có thể tham khảo các nguồn sau:
- Sách giáo khoa Hóa học lớp 10, 11 và 12.
- Các trang web uy tín về hóa học như VietChem, VnDoc, hoặc các trang web của các trường đại học lớn.
- Các bài báo khoa học và tạp chí chuyên ngành hóa học.
- Các khóa học trực tuyến về hóa học trên các nền tảng giáo dục trực tuyến.
10. FAQ Về Phản Ứng Khử
10.1. Phản ứng khử có vai trò gì trong đời sống?
Phản ứng khử đóng vai trò quan trọng trong nhiều lĩnh vực của đời sống, từ sản xuất kim loại, điện năng, đến xử lý nước và bảo vệ môi trường.
10.2. Làm thế nào để nhận biết một phản ứng là phản ứng khử?
Dấu hiệu chính là sự thay đổi số oxi hóa của các nguyên tố trong phản ứng.
10.3. Chất khử là gì?
Chất khử là chất nhường electron và bị oxi hóa trong phản ứng.
10.4. Chất oxi hóa là gì?
Chất oxi hóa là chất nhận electron và bị khử trong phản ứng.
10.5. Phản ứng khử có ứng dụng gì trong y học?
Phản ứng khử được sử dụng trong sản xuất thuốc, khử trùng và các quy trình xét nghiệm y học.
10.6. Tại sao cần cân bằng phương trình phản ứng khử?
Cân bằng phương trình phản ứng khử giúp đảm bảo tuân thủ định luật bảo toàn khối lượng và bảo toàn điện tích.
10.7. Phản ứng khử khác phản ứng oxi hóa như thế nào?
Phản ứng khử là quá trình nhận electron, làm giảm số oxi hóa, trong khi phản ứng oxi hóa là quá trình nhường electron, làm tăng số oxi hóa.
10.8. Phản ứng khử có liên quan đến môi trường như thế nào?
Phản ứng khử được sử dụng trong xử lý ô nhiễm môi trường, như khử các chất độc hại trong nước và khí thải.
10.9. Có những chất khử phổ biến nào?
Một số chất khử phổ biến bao gồm hydro (H2), kim loại kiềm (Na, K), nhôm (Al) và than cốc (C).
10.10. Phản ứng khử có vai trò gì trong công nghiệp thực phẩm?
Phản ứng khử được sử dụng trong các quy trình bảo quản thực phẩm, như khử oxi để ngăn chặn sự oxi hóa và hư hỏng thực phẩm.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Bạn muốn được tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách của mình? Hãy truy cập ngay XETAIMYDINH.EDU.VN để khám phá các loại xe tải có sẵn, so sánh giá cả và thông số kỹ thuật, và được giải đáp mọi thắc mắc liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải. Đừng ngần ngại liên hệ với chúng tôi qua hotline 0247 309 9988 hoặc đến trực tiếp địa chỉ Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội để được tư vấn tận tình nhất. Xe Tải Mỹ Đình luôn sẵn sàng đồng hành cùng bạn trên mọi nẻo đường!