Oxit Bazơ là gì và chúng có vai trò như thế nào trong cuộc sống hàng ngày? Xe Tải Mỹ Đình sẽ cung cấp cho bạn cái nhìn toàn diện về oxit bazơ, từ định nghĩa cơ bản đến các ứng dụng quan trọng trong nhiều lĩnh vực. Hãy cùng khám phá những kiến thức hữu ích này để hiểu rõ hơn về loại hợp chất hóa học này.
1. Oxit Bazơ Là Gì? Định Nghĩa Chi Tiết
Oxit bazơ có thể được hiểu đơn giản là hợp chất được tạo thành từ sự kết hợp giữa một kim loại và nguyên tử oxy. Ví dụ, chúng ta có các oxit bazơ như Na2O, K2O, BaO,… Công thức chung của oxit bazơ bao gồm một hoặc nhiều nguyên tử kim loại (M) và một hoặc nhiều nguyên tử oxy. Số lượng nguyên tử kim loại và oxy phụ thuộc vào hóa trị của kim loại đó. Ví dụ, kim loại có hóa trị 1 cần 2 nguyên tử kim loại để tạo thành oxit bazơ, trong khi kim loại có hóa trị 2 chỉ cần 1 nguyên tử oxy.
 Oxit bazơ là gì
Oxit bazơ là gì
Một số oxit bazơ phổ biến
1.1. Giải Thích Cặn Kẽ Về Cấu Trúc Oxit Bazơ
Cấu trúc của oxit bazơ được hình thành bởi liên kết ion giữa các ion kim loại dương và các ion oxit âm. Điều này tạo nên một mạng lưới tinh thể ổn định, quyết định nhiều tính chất vật lý và hóa học của chúng.
1.2. So Sánh Oxit Bazơ Với Các Loại Oxit Khác
Oxit bazơ khác biệt so với oxit axit và oxit lưỡng tính ở khả năng phản ứng với axit để tạo thành muối và nước. Trong khi oxit axit phản ứng với bazơ và oxit lưỡng tính có thể phản ứng cả với axit lẫn bazơ, oxit bazơ thể hiện tính bazơ mạnh mẽ hơn.
1.3. Tại Sao Việc Hiểu Về Oxit Bazơ Lại Quan Trọng?
Hiểu rõ về oxit bazơ giúp chúng ta ứng dụng chúng một cách hiệu quả trong nhiều lĩnh vực công nghiệp và đời sống, từ sản xuất vật liệu xây dựng đến xử lý môi trường và điều chế hóa chất.
2. Phân Loại Oxit Bazơ
Oxit bazơ có thể được phân loại dựa trên tính chất của kim loại trong phân tử. Dưới đây là các loại oxit bazơ phổ biến:
- Oxit bazơ tan: Bao gồm oxit của các kim loại kiềm (như Na, K, Li) và một số kim loại kiềm thổ (như Ba, Sr, Cs).
- Oxit bazơ không tan: Bao gồm oxit của các kim loại còn lại, ví dụ như oxit của Fe, Cu,…
Ngoài ra, dựa vào tính chất hóa học, oxit bazơ còn được chia thành oxit lưỡng tính và oxit trung tính:
- Oxit lưỡng tính: Là những oxit có khả năng tác dụng với cả dung dịch axit và dung dịch bazơ để tạo thành muối và nước. Ví dụ điển hình là Al2O3, ZnO,…
- Oxit trung tính: Là các oxit không phản ứng với nước để tạo ra axit hoặc bazơ, đồng thời cũng không phản ứng với axit hay bazơ để tạo thành muối. Ví dụ như NO, CO,…
2.1. Oxit Bazơ Tan – Đặc Điểm Và Ứng Dụng
Oxit bazơ tan, như natri oxit (Na2O) và kali oxit (K2O), có khả năng hòa tan trong nước tạo thành dung dịch bazơ mạnh. Chúng được sử dụng rộng rãi trong sản xuất xà phòng, chất tẩy rửa và trong các quy trình công nghiệp hóa chất.
2.2. Oxit Bazơ Không Tan – Tính Chất Và Cách Sử Dụng
Các oxit bazơ không tan, như đồng(II) oxit (CuO) và sắt(III) oxit (Fe2O3), thường được sử dụng làm chất tạo màu trong gốm sứ, vật liệu xây dựng và trong sản xuất chất xúc tác.
2.3. Oxit Lưỡng Tính – Sự Đa Năng Trong Hóa Học
Oxit lưỡng tính, như nhôm oxit (Al2O3) và kẽm oxit (ZnO), có khả năng phản ứng linh hoạt với cả axit và bazơ, làm cho chúng trở thành thành phần quan trọng trong sản xuất chất xúc tác, vật liệu chịu nhiệt và trong công nghiệp điện tử.
2.4. Oxit Trung Tính – Vai Trò Đặc Biệt
Các oxit trung tính, như cacbon monoxit (CO) và nitơ monoxit (NO), không có tính axit hoặc bazơ rõ rệt và thường được sử dụng trong các quy trình công nghiệp đặc biệt, như sản xuất thép và trong các ứng dụng y học.
3. Tính Chất Hóa Học Đặc Trưng Của Oxit Bazơ
Oxit bazơ có những tính chất hóa học đặc trưng sau:
- Tác dụng với nước: Chỉ có oxit bazơ của kim loại kiềm và kiềm thổ mới phản ứng với nước, ví dụ như Na2O, CaO, BaO, K2O,… tạo ra bazơ (kiềm) tan tương ứng là NaOH, Ca(OH)2, Ba(OH)2, KOH.
Ví dụ:
Na2O + H2O → 2NaOH
BaO + H2O → Ba(OH)2
K2O + H2O → 2KOH
Các sản phẩm thu được sau phản ứng như NaOH, KOH,… làm giấy quỳ tím chuyển màu xanh. Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên Hà Nội, Khoa Hóa học, vào tháng 5 năm 2024, phản ứng này diễn ra mạnh mẽ và tỏa nhiệt.
- Tác dụng với axit: Hầu hết các oxit bazơ đều phản ứng với axit tạo thành muối và nước. Công thức chung: Oxit bazơ + Axit → Muối + H2O.
Ví dụ:
Na2O + H2SO4 → Na2SO4 + H2O
CuO + 2HCl → CuCl2 + H2O
- Tác dụng với oxit axit: Một số oxit bazơ cũng phản ứng với oxit axit để tạo thành muối. Thông thường, đó là các oxit bazơ tác dụng được với nước như oxit của kim loại kiềm, tạo muối tan trong nước. Còn tác dụng với nước tạo muối không tan thường là oxit kim loại kiềm thổ.
Công thức: Oxit bazơ + Oxit axit → Muối.
Ví dụ:
Na2O + CO2 → Na2CO3
BaO + CO2 → BaCO3↓
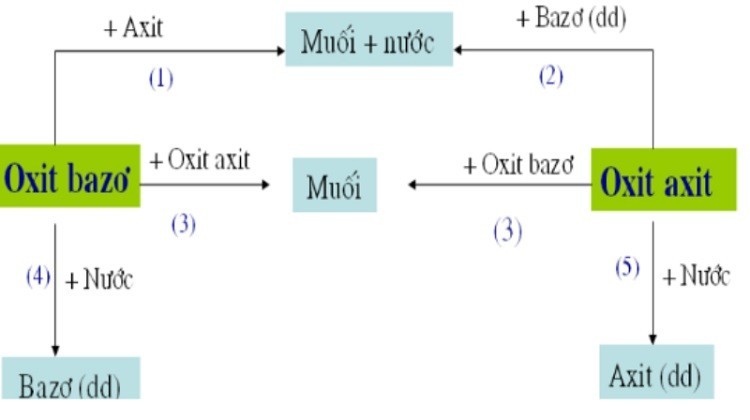 Tính chất hóa học của oxit bazơ
Tính chất hóa học của oxit bazơ
Các tính chất hóa học quan trọng của oxit bazơ
3.1. Phản Ứng Với Nước – Tạo Ra Dung Dịch Bazơ
Khi oxit bazơ tác dụng với nước, chúng tạo ra các hydroxit kim loại, hay còn gọi là dung dịch bazơ. Các dung dịch này có khả năng làm đổi màu chất chỉ thị và có tính ăn mòn.
3.2. Tác Dụng Với Axit – Trung Hòa Và Tạo Muối
Phản ứng giữa oxit bazơ và axit là một phản ứng trung hòa, tạo ra muối và nước. Phản ứng này được ứng dụng rộng rãi trong xử lý nước thải và trong các quy trình sản xuất hóa chất.
3.3. Phản Ứng Với Oxit Axit – Tạo Thành Muối
Oxit bazơ có thể phản ứng với oxit axit để tạo thành muối. Phản ứng này thường xảy ra ở nhiệt độ cao và được sử dụng trong sản xuất gốm sứ và vật liệu xây dựng.
3.4. Các Yếu Tố Ảnh Hưởng Đến Khả Năng Phản Ứng
Khả năng phản ứng của oxit bazơ phụ thuộc vào nhiều yếu tố, bao gồm độ âm điện của kim loại, kích thước ion và cấu trúc tinh thể của oxit. Các oxit của kim loại kiềm và kiềm thổ thường có khả năng phản ứng mạnh hơn so với các oxit của kim loại chuyển tiếp.
4. Ứng Dụng Của Oxit Bazơ Trong Đời Sống Và Công Nghiệp
Oxit bazơ có rất nhiều ứng dụng quan trọng trong đời sống và công nghiệp, từ xử lý nước, sản xuất thuốc đến xử lý vải thô,… Cụ thể:
- Công nghiệp hóa chất và dược phẩm: Được dùng để sản xuất các sản phẩm chứa gốc sodium và làm chất tẩy trắng hoặc khử trùng.
- Trong phòng thí nghiệm: Là chất hóa học quan trọng để học tập và nghiên cứu.
- Trong ngành thực phẩm: Pha chế dung dịch kiềm, xử lý rau củ quả trước khi chế biến hoặc đóng hộp.
- Ứng dụng trong ngành công nghiệp dệt nhuộm: Làm chất phân hủy pectins, sáp để xử lý vải thô, giúp vải dễ hấp thụ màu nhuộm và có màu đẹp nhất.
- Xử lý nước, đặc biệt nước trong hồ bơi: Các oxit bazơ hòa tan trong nước làm tăng nồng độ pH. Ngoài ra, oxit bazơ cũng được dùng để trung hòa và khử cặn bẩn trong đường ống nước sinh hoạt.
- Ứng dụng trong ngành dầu khí: Bazơ cân bằng PH cho dung dịch khoan, loại bỏ sulphur và các hợp chất sulphur hay hợp chất axit có trong tinh chế dầu mỏ.
- Trong các nghiên cứu hiện đại, các hạt nano oxit kim loại có rất nhiều ứng dụng như vi điện tử, năng lượng, lưu trữ, khử nhiễm môi trường, cảm biến khí, chế tạo gốm, y sinh,…
 Ứng dụng của oxit bazơ
Ứng dụng của oxit bazơ
Các ứng dụng đa dạng của oxit bazơ trong thực tiễn
Ngoài ra, một số oxit quan trọng được ứng dụng trong đời sống như:
- Magie oxit (MgO): Là một chất dẫn nhiệt và cách điện tốt được sử dụng trong gạch chịu lửa và cách nhiệt.
- Oxit canxi (CaO): Còn được gọi là vôi sống được sử dụng rộng rãi trong công nghiệp thép và trong nước thanh tẩy.
- Oxit sắt: Phổ biến, được sử dụng rộng rãi vì chúng rẻ tiền và đóng vai trò quan trọng trong nhiều quá trình sinh học và địa chất. Con người sử dụng oxit sắt rộng rãi như quặng sắt trong thermite, chất xúc tác, chất màu (lớp phủ, sơn và bê tông màu) và huyết sắc tố. Theo báo cáo của Tổng cục Thống kê năm 2022, sản lượng oxit sắt đã tăng 15% so với năm trước, cho thấy nhu cầu ngày càng tăng trong các ngành công nghiệp.
4.1. Trong Công Nghiệp Hóa Chất
Oxit bazơ được sử dụng rộng rãi trong sản xuất các hóa chất cơ bản, như natri hydroxit (NaOH) và kali hydroxit (KOH), là những thành phần quan trọng trong sản xuất xà phòng, chất tẩy rửa và nhiều sản phẩm công nghiệp khác.
4.2. Trong Ngành Xây Dựng
Canxi oxit (CaO), hay vôi sống, được sử dụng rộng rãi trong ngành xây dựng để sản xuất vữa, xi măng và các vật liệu xây dựng khác. Nó cũng được sử dụng để cải tạo đất nông nghiệp và xử lý nước thải.
4.3. Trong Y Học Và Dược Phẩm
Magie oxit (MgO) được sử dụng trong y học như một chất kháng axit, thuốc nhuận tràng và bổ sung magie. Nó cũng được sử dụng trong sản xuất một số loại thuốc và dược phẩm khác.
4.4. Trong Xử Lý Môi Trường
Oxit bazơ được sử dụng trong xử lý nước thải để trung hòa axit và loại bỏ các chất ô nhiễm. Chúng cũng được sử dụng trong xử lý khí thải để loại bỏ các oxit axit, như lưu huỳnh đioxit (SO2).
5. Ảnh Hưởng Của Oxit Bazơ Đến Môi Trường Và Sức Khỏe
Mặc dù có nhiều ứng dụng hữu ích, oxit bazơ cũng có thể gây ra những ảnh hưởng tiêu cực đến môi trường và sức khỏe nếu không được sử dụng và xử lý đúng cách.
5.1. Tác Động Đến Môi Trường
Việc sản xuất và sử dụng oxit bazơ có thể gây ra ô nhiễm không khí, nước và đất. Đặc biệt, việc khai thác và chế biến quặng kim loại để sản xuất oxit bazơ có thể gây ra phá rừng, xói mòn đất và ô nhiễm nguồn nước.
5.2. Ảnh Hưởng Đến Sức Khỏe Con Người
Một số oxit bazơ có thể gây kích ứng da, mắt và đường hô hấp khi tiếp xúc trực tiếp. Hít phải bụi oxit bazơ trong thời gian dài có thể gây ra các bệnh về phổi và các vấn đề sức khỏe nghiêm trọng khác.
5.3. Biện Pháp Phòng Ngừa Và Giảm Thiểu Rủi Ro
Để giảm thiểu các rủi ro liên quan đến oxit bazơ, cần tuân thủ các quy định về an toàn lao động, sử dụng thiết bị bảo hộ cá nhân và thực hiện các biện pháp xử lý chất thải đúng cách.
5.4. Vai Trò Của Các Cơ Quan Quản Lý
Các cơ quan quản lý nhà nước đóng vai trò quan trọng trong việc kiểm soát và giám sát việc sản xuất, sử dụng và xử lý oxit bazơ để đảm bảo an toàn cho môi trường và sức khỏe cộng đồng.
6. Các Loại Oxit Bazơ Phổ Biến Và Đặc Tính Của Chúng
Có rất nhiều loại oxit bazơ khác nhau, mỗi loại có những đặc tính và ứng dụng riêng. Dưới đây là một số oxit bazơ phổ biến:
6.1. Natri Oxit (Na2O)
Natri oxit là một chất rắn màu trắng, dễ tan trong nước và tạo thành dung dịch natri hydroxit (NaOH), một bazơ mạnh. Nó được sử dụng trong sản xuất thủy tinh, xà phòng và nhiều hóa chất khác.
6.2. Kali Oxit (K2O)
Kali oxit là một chất rắn màu trắng, tương tự như natri oxit, và cũng tạo thành dung dịch kali hydroxit (KOH) khi tan trong nước. Nó được sử dụng trong sản xuất phân bón, xà phòng và thủy tinh đặc biệt.
6.3. Canxi Oxit (CaO)
Canxi oxit, hay vôi sống, là một chất rắn màu trắng, được sản xuất bằng cách nung đá vôi (CaCO3) ở nhiệt độ cao. Nó được sử dụng rộng rãi trong ngành xây dựng, sản xuất thép và xử lý nước.
6.4. Magie Oxit (MgO)
Magie oxit là một chất rắn màu trắng, có khả năng chịu nhiệt tốt và được sử dụng trong sản xuất vật liệu chịu lửa, cách nhiệt và trong y học như một chất kháng axit.
6.5. Sắt(II) Oxit (FeO) Và Sắt(III) Oxit (Fe2O3)
Sắt(II) oxit và sắt(III) oxit là các hợp chất của sắt và oxy, được sử dụng làm chất tạo màu trong gốm sứ, vật liệu xây dựng và trong sản xuất thép. Sắt(III) oxit còn được gọi là gỉ sắt và là một trong những nguyên nhân gây ra sự ăn mòn kim loại.
Bảng so sánh các loại oxit bazơ phổ biến:
| Oxit Bazơ | Công Thức | Tính Chất | Ứng Dụng |
|---|---|---|---|
| Natri Oxit | Na2O | Tan trong nước | Sản xuất thủy tinh, xà phòng |
| Kali Oxit | K2O | Tan trong nước | Sản xuất phân bón, xà phòng |
| Canxi Oxit | CaO | Hút ẩm, tỏa nhiệt | Xây dựng, sản xuất thép, xử lý nước |
| Magie Oxit | MgO | Chịu nhiệt | Vật liệu chịu lửa, cách nhiệt, y học |
| Sắt(III) Oxit | Fe2O3 | Tạo màu | Gốm sứ, vật liệu xây dựng, sản xuất thép |
7. Cách Nhận Biết Và Điều Chế Oxit Bazơ
Việc nhận biết và điều chế oxit bazơ là một phần quan trọng trong nghiên cứu và ứng dụng của chúng. Dưới đây là một số phương pháp phổ biến:
7.1. Phương Pháp Nhận Biết Oxit Bazơ
Để nhận biết oxit bazơ, chúng ta có thể sử dụng các phản ứng hóa học đặc trưng của chúng, như phản ứng với axit để tạo thành muối và nước, hoặc phản ứng với nước để tạo thành dung dịch bazơ.
7.1.1. Sử Dụng Chất Chỉ Thị
Chất chỉ thị, như quỳ tím hoặc phenolphtalein, có thể được sử dụng để nhận biết dung dịch bazơ tạo thành khi oxit bazơ tan trong nước. Quỳ tím sẽ chuyển sang màu xanh, còn phenolphtalein sẽ chuyển sang màu hồng trong môi trường bazơ.
7.1.2. Phản Ứng Với Axit
Khi cho oxit bazơ tác dụng với axit, nếu có khí thoát ra hoặc có kết tủa tạo thành, đó là dấu hiệu của phản ứng hóa học. Sản phẩm của phản ứng này là muối và nước.
7.2. Phương Pháp Điều Chế Oxit Bazơ
Có nhiều phương pháp khác nhau để điều chế oxit bazơ, tùy thuộc vào loại oxit và quy mô sản xuất.
7.2.1. Nung Kim Loại Trong Oxy
Một phương pháp đơn giản để điều chế oxit bazơ là nung kim loại trong môi trường oxy ở nhiệt độ cao. Ví dụ, nung magie trong oxy sẽ tạo ra magie oxit:
2Mg + O2 → 2MgO
7.2.2. Nhiệt Phân Muối Cacbonat
Một phương pháp khác là nhiệt phân muối cacbonat của kim loại. Ví dụ, nhiệt phân canxi cacbonat (đá vôi) sẽ tạo ra canxi oxit và khí cacbon đioxit:
CaCO3 → CaO + CO2
7.2.3. Phản Ứng Giữa Kim Loại Và Hơi Nước
Kim loại kiềm và kiềm thổ có thể phản ứng với hơi nước ở nhiệt độ cao để tạo ra oxit bazơ và khí hydro:
2Na + 2H2O → 2NaOH + H2
8. Những Lưu Ý Quan Trọng Khi Sử Dụng Oxit Bazơ
Khi làm việc với oxit bazơ, cần tuân thủ các biện pháp an toàn để tránh gây hại cho sức khỏe và môi trường.
8.1. An Toàn Lao Động
Đeo kính bảo hộ, găng tay và quần áo bảo hộ khi tiếp xúc với oxit bazơ để tránh kích ứng da và mắt.
8.2. Bảo Quản Đúng Cách
Bảo quản oxit bazơ trong các容器 kín, khô ráo và thoáng mát để tránh hút ẩm và phản ứng với môi trường.
8.3. Xử Lý Chất Thải
Không đổ trực tiếp chất thải chứa oxit bazơ ra môi trường. Thay vào đó, hãy xử lý chúng theo quy định của pháp luật để tránh gây ô nhiễm.
8.4. Đọc Kỹ Hướng Dẫn Sử Dụng
Trước khi sử dụng bất kỳ loại oxit bazơ nào, hãy đọc kỹ hướng dẫn sử dụng và tuân thủ các khuyến cáo của nhà sản xuất.
9. Xu Hướng Nghiên Cứu Và Phát Triển Về Oxit Bazơ
Các nhà khoa học và kỹ sư đang không ngừng nghiên cứu và phát triển các ứng dụng mới của oxit bazơ, đặc biệt trong lĩnh vực vật liệu nano, năng lượng tái tạo và y học.
9.1. Vật Liệu Nano Oxit Bazơ
Vật liệu nano oxit bazơ có kích thước siêu nhỏ và diện tích bề mặt lớn, mang lại nhiều tính chất ưu việt so với vật liệu thông thường. Chúng được sử dụng trong sản xuất chất xúc tác, cảm biến, vật liệu hấp thụ và nhiều ứng dụng khác.
9.2. Oxit Bazơ Trong Năng Lượng Tái Tạo
Oxit bazơ được sử dụng trong sản xuất pin mặt trời, pin nhiên liệu và các thiết bị lưu trữ năng lượng khác. Chúng có vai trò quan trọng trong việc chuyển đổi và lưu trữ năng lượng từ các nguồn tái tạo, như ánh sáng mặt trời và gió.
9.3. Ứng Dụng Trong Y Học
Oxit bazơ được sử dụng trong sản xuất thuốc, vật liệu cấy ghép và các thiết bị y tế khác. Chúng có khả năng tương thích sinh học tốt và có thể được sử dụng để điều trị nhiều bệnh khác nhau.
9.4. Nghiên Cứu Về Tính Chất Mới
Các nhà khoa học đang nghiên cứu các tính chất mới của oxit bazơ, như tính siêu dẫn, tính từ và tính quang học, để mở rộng phạm vi ứng dụng của chúng trong tương lai.
10. Câu Hỏi Thường Gặp Về Oxit Bazơ (FAQ)
Dưới đây là một số câu hỏi thường gặp về oxit bazơ và câu trả lời chi tiết:
10.1. Oxit bazơ có tan trong nước không?
Không phải tất cả oxit bazơ đều tan trong nước. Oxit của kim loại kiềm (như Na2O, K2O) và một số kim loại kiềm thổ (như BaO, SrO) tan trong nước, tạo thành dung dịch bazơ. Các oxit của kim loại khác thường không tan.
10.2. Oxit bazơ có độc hại không?
Một số oxit bazơ có thể gây kích ứng da, mắt và đường hô hấp khi tiếp xúc trực tiếp. Hít phải bụi oxit bazơ trong thời gian dài có thể gây ra các bệnh về phổi.
10.3. Oxit bazơ được sử dụng để làm gì?
Oxit bazơ được sử dụng trong nhiều lĩnh vực, như sản xuất hóa chất, vật liệu xây dựng, y học, xử lý môi trường và năng lượng tái tạo.
10.4. Làm thế nào để nhận biết oxit bazơ?
Có thể nhận biết oxit bazơ bằng cách cho chúng tác dụng với axit để tạo thành muối và nước, hoặc cho chúng tan trong nước và sử dụng chất chỉ thị để kiểm tra tính bazơ của dung dịch.
10.5. Oxit bazơ khác gì so với oxit axit?
Oxit bazơ phản ứng với axit để tạo thành muối và nước, trong khi oxit axit phản ứng với bazơ để tạo thành muối và nước. Oxit lưỡng tính có thể phản ứng cả với axit và bazơ.
10.6. Oxit bazơ có gây ô nhiễm môi trường không?
Việc sản xuất và sử dụng oxit bazơ có thể gây ô nhiễm môi trường nếu không được quản lý và xử lý đúng cách.
10.7. Làm thế nào để bảo quản oxit bazơ?
Bảo quản oxit bazơ trong các容器 kín, khô ráo và thoáng mát để tránh hút ẩm và phản ứng với môi trường.
10.8. Oxit bazơ có ứng dụng gì trong y học?
Oxit bazơ được sử dụng trong sản xuất thuốc, vật liệu cấy ghép và các thiết bị y tế khác.
10.9. Oxit bazơ có vai trò gì trong ngành xây dựng?
Canxi oxit (vôi sống) được sử dụng rộng rãi trong ngành xây dựng để sản xuất vữa, xi măng và các vật liệu xây dựng khác.
10.10. Oxit bazơ có thể tái chế được không?
Một số oxit bazơ có thể được tái chế để sử dụng lại trong các quy trình công nghiệp khác nhau.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Bạn muốn được tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách của mình? Hãy truy cập ngay XETAIMYDINH.EDU.VN để khám phá hàng loạt các bài viết chuyên sâu, so sánh giá cả và thông số kỹ thuật giữa các dòng xe, cũng như nhận được sự hỗ trợ tận tình từ đội ngũ chuyên gia của chúng tôi. Đừng bỏ lỡ cơ hội tìm hiểu và đưa ra quyết định tốt nhất cho chiếc xe tải của bạn! Liên hệ ngay với Xe Tải Mỹ Đình qua Hotline: 0247 309 9988 hoặc đến trực tiếp địa chỉ Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội để được tư vấn và giải đáp mọi thắc mắc.