Ngâm một đinh sắt sạch trong 200ml dung dịch CuSO4 sẽ tạo ra một phản ứng hóa học thú vị, làm tăng khối lượng đinh sắt. Bài viết này của Xe Tải Mỹ Đình, tại XETAIMYDINH.EDU.VN, sẽ giải thích chi tiết về hiện tượng này, cùng những ứng dụng và kiến thức liên quan, giúp bạn hiểu rõ hơn về quá trình này và các yếu tố ảnh hưởng đến nó. Đừng bỏ lỡ những thông tin quan trọng về phản ứng oxi hóa khử, nồng độ dung dịch và ứng dụng thực tế!
1. Phản Ứng Khi Ngâm Đinh Sắt Trong Dung Dịch CuSO4 Là Gì?
Khi ngâm một đinh sắt (Fe) vào dung dịch đồng sunfat (CuSO4), một phản ứng hóa học xảy ra, trong đó sắt tan ra và đồng kim loại bám vào đinh sắt. Phản ứng này thuộc loại phản ứng oxi hóa khử, cụ thể là phản ứng thế.
Giải thích chi tiết:
- Phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu
- Sắt (Fe): Sắt là chất khử, nó nhường electron và bị oxi hóa thành ion sắt (Fe2+), tan vào dung dịch.
- Đồng sunfat (CuSO4): Đồng (Cu2+) trong dung dịch nhận electron và bị khử thành đồng kim loại (Cu), bám vào bề mặt đinh sắt.
Phản ứng này dẫn đến những thay đổi sau:
- Đinh sắt: Khối lượng tăng lên do đồng kim loại bám vào. Bề mặt đinh sắt chuyển sang màu đỏ của đồng.
- Dung dịch CuSO4: Màu xanh lam của dung dịch nhạt dần do nồng độ ion đồng (Cu2+) giảm. Dung dịch chứa ion sắt (Fe2+), có màu xanh nhạt hơn.
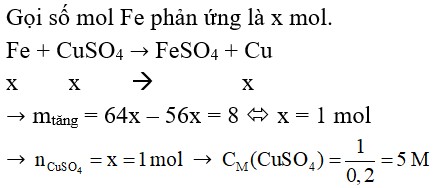 Đinh sắt sau khi ngâm trong dung dịch CuSO4
Đinh sắt sau khi ngâm trong dung dịch CuSO4
2. Tại Sao Khối Lượng Đinh Sắt Tăng Lên Khi Ngâm Trong Dung Dịch CuSO4?
Khối lượng đinh sắt tăng lên là do đồng (Cu) từ dung dịch CuSO4 bám vào đinh sắt, thay thế cho lượng sắt (Fe) đã tan ra.
Giải thích chi tiết:
- Nguyên tắc: Phản ứng thế xảy ra theo nguyên tắc: Kim loại mạnh hơn sẽ đẩy kim loại yếu hơn ra khỏi dung dịch muối. Trong trường hợp này, sắt mạnh hơn đồng, nên sắt sẽ tan vào dung dịch và đồng bám vào đinh sắt.
- Khối lượng mol: Khối lượng mol của đồng (Cu) là 64 g/mol, lớn hơn khối lượng mol của sắt (Fe) là 56 g/mol. Do đó, mỗi mol sắt tan ra sẽ được thay thế bằng một mol đồng, làm tăng khối lượng của đinh sắt.
Ví dụ:
Nếu khối lượng đinh sắt tăng lên 8 gam, có nghĩa là:
- Số mol đồng bám vào: 8 gam / 64 g/mol = 0.125 mol
- Số mol sắt tan ra: 0.125 mol
3. Những Yếu Tố Nào Ảnh Hưởng Đến Sự Thay Đổi Khối Lượng Đinh Sắt Khi Ngâm Trong Dung Dịch CuSO4?
Có nhiều yếu tố ảnh hưởng đến sự thay đổi khối lượng đinh sắt khi ngâm trong dung dịch CuSO4, bao gồm:
- Nồng độ dung dịch CuSO4: Nồng độ càng cao, phản ứng xảy ra càng nhanh và lượng đồng bám vào đinh sắt càng nhiều.
- Thời gian ngâm: Thời gian ngâm càng lâu, phản ứng xảy ra càng triệt để và khối lượng đinh sắt tăng lên càng nhiều.
- Nhiệt độ: Nhiệt độ tăng, phản ứng xảy ra nhanh hơn.
- Diện tích bề mặt đinh sắt: Diện tích bề mặt càng lớn, phản ứng xảy ra càng nhanh.
- Độ tinh khiết của đinh sắt: Đinh sắt càng tinh khiết, phản ứng xảy ra càng dễ dàng.
- Khuấy trộn: Khuấy trộn giúp dung dịch đồng nhất, tăng tốc độ phản ứng.
4. Làm Sao Tính Được Nồng Độ Dung Dịch CuSO4 Ban Đầu Khi Biết Độ Tăng Khối Lượng Đinh Sắt?
Để tính nồng độ dung dịch CuSO4 ban đầu, ta cần dựa vào độ tăng khối lượng của đinh sắt sau phản ứng.
Các bước thực hiện:
- Tính số mol đồng (Cu) bám vào đinh sắt:
- Số mol Cu = Độ tăng khối lượng / (Khối lượng mol Cu – Khối lượng mol Fe)
- Ví dụ: Nếu độ tăng khối lượng là 8 gam, số mol Cu = 8 / (64 – 56) = 1 mol
- Tính số mol CuSO4 đã phản ứng:
- Số mol CuSO4 phản ứng = Số mol Cu
- Tính nồng độ dung dịch CuSO4 ban đầu:
- Nồng độ CuSO4 = Số mol CuSO4 / Thể tích dung dịch (lít)
- Ví dụ: Nếu thể tích dung dịch là 200ml (0.2 lít), nồng độ CuSO4 = 1 mol / 0.2 lít = 5M
Lưu ý:
- Công thức trên chỉ đúng khi phản ứng xảy ra hoàn toàn.
- Cần đảm bảo đơn vị đo lường chính xác.
5. Ứng Dụng Thực Tế Của Phản Ứng Giữa Sắt Và CuSO4 Là Gì?
Phản ứng giữa sắt và CuSO4 có nhiều ứng dụng trong thực tế, bao gồm:
- Luyện kim:
- Điều chế đồng: Trong công nghiệp, phản ứng này được sử dụng để thu hồi đồng từ dung dịch đồng sunfat.
- Làm sạch quặng: Loại bỏ tạp chất sắt từ quặng đồng.
- Nông nghiệp:
- Điều chế thuốc trừ sâu: CuSO4 được sử dụng làm thuốc trừ sâu, diệt nấm. Phản ứng với sắt giúp tăng hiệu quả của thuốc.
- Bổ sung vi lượng sắt cho cây trồng: FeSO4 tạo ra từ phản ứng cung cấp sắt cho cây.
- Giáo dục:
- Thí nghiệm hóa học: Phản ứng này là một thí nghiệm thú vị và dễ thực hiện, giúp học sinh hiểu rõ hơn về phản ứng oxi hóa khử.
- Mạ điện:
- Mạ đồng lên sắt: Tạo lớp bảo vệ chống ăn mòn.
6. Các Biện Pháp Phòng Ngừa Ăn Mòn Kim Loại Trong Môi Trường Tương Tự Phản Ứng Sắt Và CuSO4?
Ăn mòn kim loại là một vấn đề lớn trong nhiều ngành công nghiệp. Để phòng ngừa ăn mòn kim loại trong môi trường tương tự phản ứng giữa sắt và CuSO4, có thể áp dụng các biện pháp sau:
- Sử dụng vật liệu chống ăn mòn:
- Thép không gỉ: Chứa crom, niken, tạo lớp oxit bảo vệ.
- Nhựa, composite: Không bị ăn mòn bởi axit và muối.
- Sơn phủ bề mặt:
- Sơn chống ăn mòn: Tạo lớp bảo vệ, ngăn kim loại tiếp xúc với môi trường.
- Mạ kim loại: Mạ kẽm, crom, niken để bảo vệ kim loại nền.
- Sử dụng chất ức chế ăn mòn:
- Thêm chất ức chế vào môi trường: Giảm tốc độ ăn mòn.
- Ví dụ: Photphat, silicat.
- Kiểm soát môi trường:
- Giảm độ ẩm: Hạn chế quá trình ăn mòn điện hóa.
- Điều chỉnh pH: Duy trì môi trường trung tính hoặc kiềm.
- Bảo vệ điện hóa:
- Anốt hy sinh: Sử dụng kim loại dễ bị ăn mòn hơn để bảo vệ kim loại chính.
- Cực âm hóa: Sử dụng dòng điện ngoài để bảo vệ kim loại.
7. So Sánh Phản Ứng Giữa Sắt Với CuSO4 Và Các Kim Loại Khác?
Phản ứng giữa sắt và CuSO4 là một ví dụ điển hình của phản ứng thế trong hóa học. Tuy nhiên, phản ứng của sắt với các dung dịch muối kim loại khác có thể khác nhau, tùy thuộc vào vị trí của kim loại đó trong dãy điện hóa.
Dãy điện hóa:
K > Na > Mg > Al > Zn > Fe > Ni > Sn > Pb > H > Cu > Ag > Pt > Au
Nguyên tắc:
- Kim loại đứng trước trong dãy điện hóa có khả năng đẩy kim loại đứng sau ra khỏi dung dịch muối.
- Phản ứng xảy ra càng mạnh mẽ khi khoảng cách giữa hai kim loại trong dãy điện hóa càng lớn.
Ví dụ:
- Sắt và AgNO3: Sắt phản ứng mạnh mẽ với AgNO3, tạo ra Ag và Fe(NO3)2. Phản ứng này xảy ra nhanh chóng do Ag đứng rất xa Fe trong dãy điện hóa.
- Sắt và ZnSO4: Sắt không phản ứng với ZnSO4 vì Zn đứng trước Fe trong dãy điện hóa.
Bảng so sánh:
| Dung dịch muối | Phản ứng | Mức độ phản ứng |
|---|---|---|
| CuSO4 | Fe + CuSO4 → FeSO4 + Cu | Trung bình |
| AgNO3 | Fe + 2AgNO3 → Fe(NO3)2 + 2Ag | Mạnh mẽ |
| ZnSO4 | Không phản ứng | Không |
| Pb(NO3)2 | Fe + Pb(NO3)2 → Fe(NO3)2 + Pb | Chậm |
8. Ảnh Hưởng Của Phản Ứng Sắt Và CuSO4 Đến Môi Trường?
Phản ứng giữa sắt và CuSO4 có thể gây ra một số tác động đến môi trường, đặc biệt là khi xảy ra ở quy mô lớn hoặc không được kiểm soát.
Tác động tiêu cực:
- Ô nhiễm nguồn nước:
- Ion sắt (Fe2+) có thể làm thay đổi màu sắc và tính chất của nước.
- CuSO4 dư thừa có thể gây độc cho sinh vật thủy sinh.
- Ô nhiễm đất:
- FeSO4 có thể làm thay đổi độ pH của đất.
- CuSO4 có thể tích tụ trong đất, gây hại cho cây trồng.
- Ảnh hưởng đến hệ sinh thái:
- Thay đổi thành phần hóa học của môi trường có thể ảnh hưởng đến sự sinh trưởng và phát triển của các loài sinh vật.
Biện pháp giảm thiểu tác động:
- Kiểm soát lượng hóa chất sử dụng: Sử dụng đúng liều lượng, tránh dư thừa.
- Xử lý nước thải: Loại bỏ ion kim loại trước khi thải ra môi trường.
- Thu gom và tái chế: Tái chế các sản phẩm chứa kim loại để giảm thiểu ô nhiễm.
- Sử dụng phương pháp thân thiện với môi trường: Thay thế CuSO4 bằng các chất ít độc hại hơn.
9. Làm Thế Nào Để Tăng Tốc Độ Phản Ứng Giữa Đinh Sắt Và Dung Dịch CuSO4?
Để tăng tốc độ phản ứng giữa đinh sắt và dung dịch CuSO4, bạn có thể áp dụng một số biện pháp sau:
- Tăng nồng độ dung dịch CuSO4: Nồng độ dung dịch càng cao, số lượng ion Cu2+ có sẵn càng nhiều, dẫn đến tốc độ phản ứng tăng lên.
- Tăng nhiệt độ: Nâng cao nhiệt độ của dung dịch sẽ làm tăng động năng của các phân tử, giúp chúng va chạm với nhau thường xuyên hơn và mạnh hơn, từ đó tăng tốc độ phản ứng.
- Khuấy trộn dung dịch: Khuấy trộn giúp các ion Cu2+ tiếp xúc đều hơn với bề mặt đinh sắt, ngăn chặn sự hình thành lớp đồng bám trên bề mặt, giúp phản ứng diễn ra liên tục.
- Sử dụng đinh sắt có diện tích bề mặt lớn: Đinh sắt có diện tích bề mặt lớn hơn sẽ tiếp xúc với nhiều ion Cu2+ hơn, làm tăng tốc độ phản ứng. Bạn có thể sử dụng các mảnh sắt vụn hoặc bột sắt thay vì đinh sắt nguyên khối.
- Làm sạch bề mặt đinh sắt: Đảm bảo bề mặt đinh sắt không bị gỉ sét hoặc các chất bẩn khác. Bề mặt sạch sẽ giúp ion Cu2+ dễ dàng tiếp xúc và phản ứng với sắt hơn.
- Sử dụng chất xúc tác (nếu có): Trong một số trường hợp, việc thêm chất xúc tác có thể giúp tăng tốc độ phản ứng. Tuy nhiên, cần phải nghiên cứu kỹ để chọn chất xúc tác phù hợp và đảm bảo an toàn.
10. Phản Ứng Giữa Sắt Và CuSO4 Có Tuân Theo Định Luật Bảo Toàn Khối Lượng Không?
Có, phản ứng giữa sắt (Fe) và đồng sunfat (CuSO4) tuân theo định luật bảo toàn khối lượng. Định luật này phát biểu rằng trong một hệ kín, tổng khối lượng của các chất trước phản ứng bằng tổng khối lượng của các chất sau phản ứng.
Giải thích chi tiết:
Trong phản ứng Fe + CuSO4 → FeSO4 + Cu, các nguyên tử sắt (Fe) và đồng (Cu) chỉ chuyển từ trạng thái này sang trạng thái khác, chứ không bị mất đi hoặc tạo ra thêm. Khối lượng của sắt tan ra từ đinh sắt sẽ tương ứng với khối lượng đồng bám vào đinh sắt.
Ví dụ:
Giả sử ban đầu ta có:
- mFe (ban đầu) = 56 gam (1 mol)
- mCuSO4 = 159.5 gam (1 mol)
Sau phản ứng, ta thu được:
- mFeSO4 = 151.9 gam (1 mol)
- mCu = 64 gam (1 mol)
Tổng khối lượng trước phản ứng: 56 + 159.5 = 215.5 gam
Tổng khối lượng sau phản ứng: 151.9 + 64 = 215.9 gam
Như vậy, sai số nhỏ có thể xảy ra do điều kiện thí nghiệm (ví dụ: thất thoát nhỏ trong quá trình thu thập sản phẩm), nhưng về cơ bản, định luật bảo toàn khối lượng vẫn được tuân thủ.
Tầm quan trọng của định luật bảo toàn khối lượng:
Định luật bảo toàn khối lượng là một trong những định luật cơ bản của hóa học, giúp chúng ta hiểu và tính toán được lượng chất tham gia và tạo thành trong các phản ứng hóa học.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về các loại xe tải, giá cả, địa điểm mua bán uy tín và dịch vụ sửa chữa chất lượng tại Mỹ Đình? Bạn lo ngại về chi phí vận hành, bảo trì và các vấn đề pháp lý liên quan đến xe tải? Hãy đến với XETAIMYDINH.EDU.VN ngay hôm nay để được tư vấn và giải đáp mọi thắc mắc! Liên hệ hotline 0247 309 9988 hoặc đến địa chỉ Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội để được hỗ trợ tốt nhất.
FAQ: Câu Hỏi Thường Gặp Về Phản Ứng Ngâm Đinh Sắt Trong Dung Dịch CuSO4
1. Tại sao đinh sắt bị gỉ khi ngâm trong dung dịch CuSO4?
Hiện tượng gỉ sét trên đinh sắt khi ngâm trong dung dịch CuSO4 không phải là gỉ sét thông thường (Fe2O3.nH2O), mà là lớp đồng (Cu) bám trên bề mặt. Quá trình này xảy ra do phản ứng oxi hóa khử giữa sắt (Fe) và ion đồng (Cu2+) trong dung dịch CuSO4.
2. Có thể sử dụng loại sắt nào để thực hiện phản ứng này?
Bạn có thể sử dụng bất kỳ loại sắt nào, miễn là bề mặt sắt sạch và không bị gỉ sét quá nhiều. Đinh sắt, lá sắt, hoặc thậm chí bột sắt đều có thể được sử dụng. Tuy nhiên, để quan sát hiện tượng rõ ràng nhất, nên sử dụng đinh sắt sạch.
3. Dung dịch CuSO4 có thể thay thế bằng dung dịch nào khác không?
Có, bạn có thể thay thế dung dịch CuSO4 bằng các dung dịch muối của kim loại khác có tính oxi hóa mạnh hơn sắt, ví dụ như dung dịch AgNO3 (bạc nitrat). Tuy nhiên, cần lưu ý rằng phản ứng với AgNO3 sẽ diễn ra mạnh mẽ hơn và tạo ra bạc kim loại thay vì đồng.
4. Phản ứng này có nguy hiểm không? Cần lưu ý gì khi thực hiện?
Phản ứng giữa sắt và CuSO4 không quá nguy hiểm, nhưng bạn vẫn cần tuân thủ các biện pháp an toàn hóa học cơ bản:
- Đeo kính bảo hộ để tránh dung dịch bắn vào mắt.
- Đeo găng tay để bảo vệ da tay.
- Thực hiện thí nghiệm trong khu vực thông thoáng.
- Không được nuốt dung dịch hoặc hít phải hơi của dung dịch.
5. Làm thế nào để nhận biết phản ứng đã xảy ra hoàn toàn?
Bạn có thể nhận biết phản ứng đã xảy ra hoàn toàn bằng các dấu hiệu sau:
- Màu xanh lam của dung dịch CuSO4 nhạt dần hoặc biến mất hoàn toàn.
- Lượng đồng (Cu) bám trên đinh sắt không tăng thêm nữa.
- Không còn khí thoát ra (nếu có).
6. Có thể tái sử dụng dung dịch sau phản ứng không?
Dung dịch sau phản ứng chứa FeSO4 (sắt sunfat) và có thể còn dư CuSO4. Dung dịch này có thể được sử dụng trong một số ứng dụng như:
- Xử lý nước thải (loại bỏ photphat).
- Sản xuất phân bón.
- Tuy nhiên, cần phải xử lý dung dịch cẩn thận trước khi thải ra môi trường để tránh gây ô nhiễm.
7. Tại sao khối lượng đinh sắt lại tăng lên thay vì giảm đi?
Khối lượng đinh sắt tăng lên vì khối lượng mol của đồng (Cu) (64 g/mol) lớn hơn khối lượng mol của sắt (Fe) (56 g/mol). Khi một nguyên tử sắt tan ra và được thay thế bằng một nguyên tử đồng, khối lượng tổng thể của đinh sắt sẽ tăng lên.
8. Phản ứng này có ứng dụng gì trong thực tế ngoài thí nghiệm?
Ngoài thí nghiệm, phản ứng này còn có ứng dụng trong:
- Mạ đồng: Phủ một lớp đồng lên bề mặt sắt để bảo vệ chống ăn mòn hoặc tăng tính thẩm mỹ.
- Thu hồi đồng: Tách đồng từ các dung dịch chứa đồng (ví dụ: nước thải công nghiệp).
9. Làm thế nào để loại bỏ lớp đồng bám trên đinh sắt sau phản ứng?
Bạn có thể loại bỏ lớp đồng bám trên đinh sắt bằng cách ngâm đinh sắt trong dung dịch axit clohydric (HCl) loãng. Axit sẽ hòa tan lớp đồng, nhưng cần cẩn thận vì axit cũng có thể ăn mòn sắt nếu ngâm quá lâu.
10. Phản ứng này có xảy ra với các kim loại khác không?
Có, phản ứng tương tự có thể xảy ra với các kim loại khác, tùy thuộc vào tính khử của kim loại đó so với kim loại trong dung dịch muối. Kim loại có tính khử mạnh hơn sẽ đẩy kim loại yếu hơn ra khỏi dung dịch muối của nó.
