Hiđrocacbon là hợp chất hữu cơ quan trọng, cấu tạo nên nhiều chất trong thực phẩm và cơ thể sống. Bạn muốn tìm hiểu hiđrocacbon là gì, có bao nhiêu loại và đặc điểm của chúng? Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ cung cấp cho bạn cái nhìn tổng quan nhất về thành phần hóa học quan trọng này. Chúng ta cùng khám phá về cấu trúc, phân loại và ứng dụng của hiđrocacbon, đồng thời mở ra những kiến thức mới về lĩnh vực hóa học hữu cơ.
1. Hiđrocacbon Là Gì? Định Nghĩa và Phân Loại
1.1. Định Nghĩa Hiđrocacbon
Hiđrocacbon là hợp chất hữu cơ mà phân tử chỉ chứa hai nguyên tố: cacbon (C) và hiđro (H). Các nguyên tử cacbon có thể liên kết với nhau bằng liên kết đơn, đôi hoặc ba, tạo nên sự đa dạng về cấu trúc của hiđrocacbon.
1.2. Các Loại Hiđrocacbon Phổ Biến
Hiđrocacbon được phân loại dựa trên cấu trúc và loại liên kết giữa các nguyên tử cacbon:
- Hiđrocacbon no: Chỉ chứa liên kết đơn trong phân tử, bao gồm ankan và xicloankan.
- Hiđrocacbon không no: Chứa ít nhất một liên kết đôi hoặc ba trong phân tử, bao gồm anken, ankadien và ankin.
- Hiđrocacbon thơm: Chứa vòng benzen, một cấu trúc vòng đặc biệt với các liên kết pi liên hợp.
 Hợp chất Hidrocacbon là gì
Hợp chất Hidrocacbon là gì
2. Hiđrocacbon No: Ankan và Xicloankan
2.1. Ankan: Cấu Trúc và Tính Chất
Ankan là hiđrocacbon no mạch hở, chỉ chứa liên kết đơn giữa các nguyên tử cacbon. Ankan còn được gọi là parafin.
2.1.1. Công Thức và Tên Gọi Ankan
- Công thức chung: CₙH₂ₙ₊₂ (n ≥ 1)
- Tên gọi:
- Tên thay thế: Số chỉ vị trí nhánh + tên nhánh + tên mạch chính + “an”
- Tên thông thường: Thêm tiền tố “iso” nếu có một nhánh CH₃ ở vị trí C số 2, thêm tiền tố “neo” nếu có hai nhánh CH₃ ở vị trí C số 2.
2.1.2. Tính Chất Vật Lý của Ankan
- Trạng thái: Từ C₁ đến C₄ ở trạng thái khí, từ C₅ đến C₁₀ ở trạng thái lỏng, từ C₁₀ trở lên ở trạng thái rắn (ở điều kiện thường).
- Nhiệt độ nóng chảy và sôi: Tăng theo số lượng nguyên tử cacbon trong phân tử.
- Khối lượng riêng: Nhỏ hơn nước.
- Độ tan: Không tan trong nước, là chất không màu.
2.1.3. Tính Chất Hóa Học của Ankan
-
Phản ứng thế halogen: Nguyên tử halogen (như clo) có thể thay thế lần lượt các nguyên tử hiđro trong phân tử ankan khi có ánh sáng hoặc nhiệt độ. Phản ứng ưu tiên thế hiđro ở cacbon bậc cao.
Ví dụ: CH₄ + Cl₂ → CH₃Cl + HCl, CH₃Cl + Cl₂ → CH₂Cl₂ + HCl, CH₂Cl₂ + Cl₂ → CHCl₃ + HCl, CHCl₃ + Cl₂ → CCl₄ + HCl
-
Phản ứng tách:
- Tách hiđro (dehydrogen hóa): Ankan bị tách hiđro tạo thành anken hoặc ankin.
- Cracking (bẻ gãy mạch cacbon): Ankan mạch dài bị bẻ gãy thành các ankan và anken mạch ngắn hơn dưới tác dụng của nhiệt và xúc tác.
-
Phản ứng oxi hóa hoàn toàn (cháy): Ankan cháy tạo ra CO₂ và H₂O.
Công thức tổng quát: CₙH₂ₙ₊₂ + (3n+1)/2 O₂ → n CO₂ + (n+1)H₂O
2.1.4. Điều Chế Ankan
-
Trong phòng thí nghiệm: Hiđro hóa anken hoặc ankin với xúc tác Pt, Ni hoặc Pd.
Ví dụ: CₙH₂ₙ + H₂ (Pt, Ni, Pd, t°) → CₙH₂ₙ₊₂
-
Trong công nghiệp: Tách metan và các đồng đẳng từ khí thiên nhiên và dầu mỏ.
2.1.5. Ứng Dụng của Ankan
- Làm nhiên liệu (gas, xăng, dầu diesel).
- Điều chế chất sinh hàn.
- Sản xuất các hóa chất cơ bản như HCHO (formaldehyd), rượu metylic, axit axetic thông qua các phản ứng oxi hóa không hoàn toàn.
- Làm dung môi hữu cơ và dầu bôi trơn.
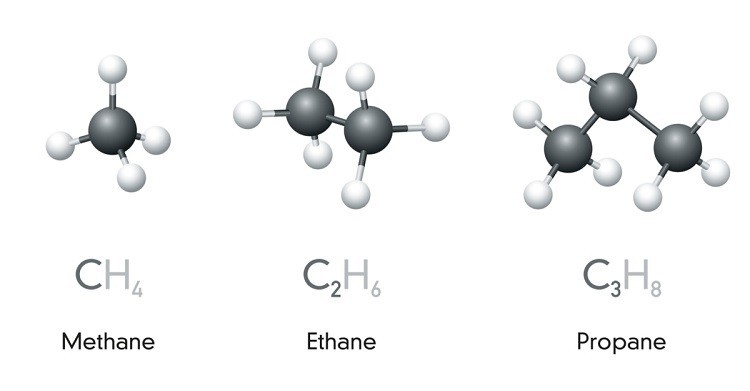 Một số hợp chất của ankan
Một số hợp chất của ankan
2.2. Xicloankan: Cấu Trúc và Tính Chất
Xicloankan là hiđrocacbon no mạch vòng, chỉ chứa liên kết đơn trong phân tử.
2.2.1. Công Thức và Tên Gọi Xicloankan
- Công thức chung: CₙH₂ₙ (n ≥ 3)
- Tên gọi: Số chỉ vị trí nhánh + tên nhánh + “xiclo” + tên mạch chính + “an”
2.2.2. Tính Chất Hóa Học của Xicloankan
-
Phản ứng thế: Xảy ra tương tự như ankan khi có ánh sáng hoặc nhiệt độ.
-
Phản ứng cháy: Xicloankan cháy tạo ra CO₂ và H₂O.
Công thức tổng quát: CₙH₂ₙ + (3n/2) O₂ → n CO₂ + n H₂O
-
Phản ứng cộng mở vòng: Xiclopropan và xiclobutan có thể tham gia phản ứng cộng mở vòng với H₂, halogen hoặc axit. Xiclopropan phản ứng dễ hơn do sức căng vòng lớn.
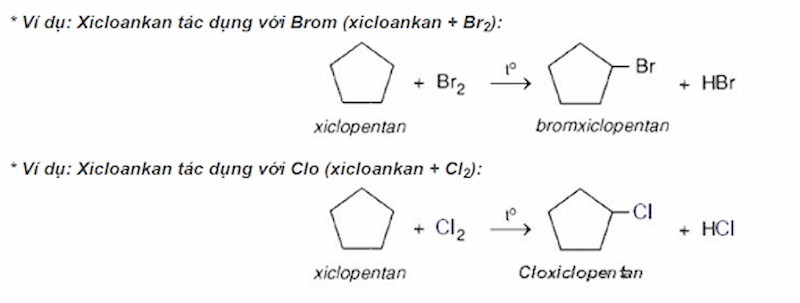 Phản ứng thế của Xicloankan
Phản ứng thế của Xicloankan
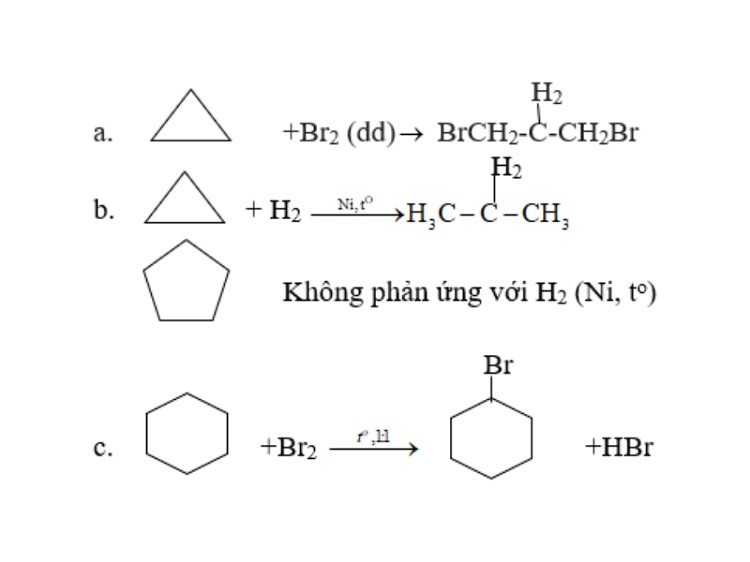 Phản ứng cộng xicloankan
Phản ứng cộng xicloankan
2.2.3. Điều Chế Xicloankan
- Chưng cất dầu mỏ và khí tự nhiên để tách các xicloankan có sẵn.
- Hiđro hóa và đóng vòng ankan.
3. Hiđrocacbon Không No: Anken, Ankadien và Ankin
3.1. Định Nghĩa và Phân Loại Hiđrocacbon Không No
Hiđrocacbon không no là hiđrocacbon chứa ít nhất một liên kết đôi (C=C) hoặc ba (C≡C) trong phân tử.
- Anken: Chứa một liên kết đôi (CₙH₂ₙ, n ≥ 2).
- Ankadien: Chứa hai liên kết đôi (CₙH₂ₙ₋₂, n ≥ 3).
- Ankin: Chứa một liên kết ba (CₙH₂ₙ₋₂, n ≥ 2).
3.2. Đồng Phân Cis-Trans
Một số hiđrocacbon không no có đồng phân cis-trans (đồng phân hình học) do sự khác biệt về vị trí tương đối của các nhóm thế xung quanh liên kết đôi. Đồng phân cis có các nhóm thế lớn nằm cùng một phía của liên kết đôi, trong khi đồng phân trans có các nhóm thế lớn nằm ở hai phía đối diện.
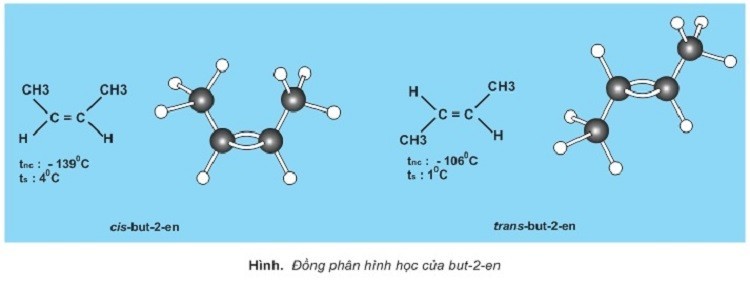 Đồng phân hình học của but-2-en
Đồng phân hình học của but-2-en
3.3. Tính Chất Hóa Học của Hiđrocacbon Không No
Hiđrocacbon không no có tính chất hóa học đặc trưng là phản ứng cộng vào liên kết đôi hoặc ba.
-
Phản ứng cộng hiđro (hiđro hóa): Hiđrocacbon không no cộng hiđro tạo thành hiđrocacbon no.
Ví dụ: H₂ + C₃H₆ → C₃H₈, 2H₂ + C₃H₄ → C₃H₈
-
Phản ứng cộng halogen (halogen hóa): Hiđrocacbon không no cộng halogen tạo thành dẫn xuất halogen.
-
Phản ứng cộng hiđro halogenua (hiđro halogen hóa): Hiđrocacbon không no cộng hiđro halogenua (như HCl) tạo thành dẫn xuất halogen.
Ví dụ: HCl + C₃H₆ → C₃H₇Cl, CH≡CH + HCl → CH₂=CHCl
-
Phản ứng trùng hợp: Nhiều phân tử hiđrocacbon không no kết hợp với nhau tạo thành polime mạch dài.
-
Phản ứng oxi hóa:
-
Phản ứng cháy: Hiđrocacbon không no cháy tạo ra CO₂ và H₂O.
Anken: CₙH₂ₙ + (3n/2) O₂ → n CO₂ + n H₂O
Ankadien và ankin: CₙH₂ₙ₋₂ + ((3n-1)/2) O₂ → n CO₂ + (n-1) H₂O
-
Phản ứng oxi hóa không hoàn toàn: Tạo ra các sản phẩm như andehit, rượu, axit, v.v.
-
4. Hiđrocacbon Thơm: Benzen và Đồng Đẳng
4.1. Định Nghĩa và Phân Loại Hiđrocacbon Thơm
Hiđrocacbon thơm là hiđrocacbon chứa vòng benzen (C₆H₆) trong phân tử.
- Benzen và đồng đẳng: Các hiđrocacbon có công thức chung CₙH₂ₙ₋₆ (n ≥ 6), bao gồm benzen, toluen, xylen, v.v.
- Hiđrocacbon thơm đa vòng: Chứa nhiều vòng benzen liên kết với nhau, ví dụ như naphtalen, antraxen.
- Hợp chất thơm không chứa vòng benzen: Chứa các vòng khác không phải benzen, nhưng vẫn có tính chất thơm.
4.2. Tính Chất Hóa Học của Hiđrocacbon Thơm
Hiđrocacbon thơm có tính chất hóa học đặc trưng là phản ứng thế vào vòng benzen.
- Phản ứng thế electrophin: Nguyên tử hiđro trên vòng benzen bị thay thế bởi các nhóm electrophin (như halogen, nhóm nitro, nhóm ankyl, nhóm acyl) dưới tác dụng của xúc tác axit.
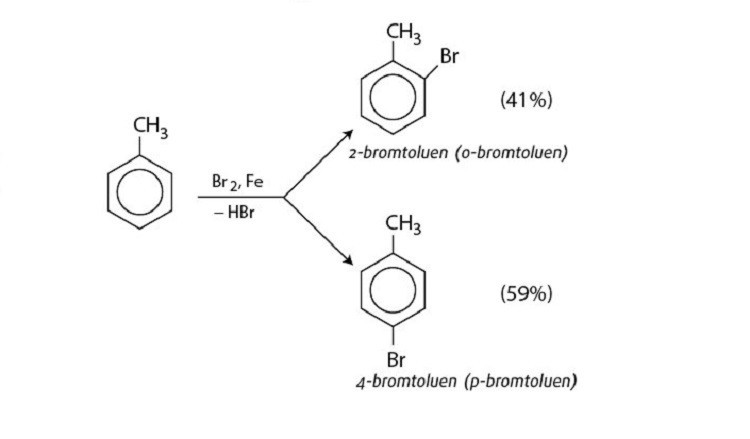 ankylbenzen phản ứng với brom
ankylbenzen phản ứng với brom
 benzen phản ứng với axit nitric
benzen phản ứng với axit nitric
-
Phản ứng cộng: Vòng benzen có thể cộng hiđro hoặc halogen khi có xúc tác mạnh và điều kiện khắc nghiệt.
-
Phản ứng oxi hóa:
-
Phản ứng oxi hóa hoàn toàn (cháy): Hiđrocacbon thơm cháy tạo ra CO₂ và H₂O.
Công thức tổng quát: CₙH₂ₙ₋₆ + ( (3n-3)/2 ) O₂ → n CO₂ + (n-3) H₂O
-
Phản ứng oxi hóa không hoàn toàn: Các ankylbenzen (benzen có nhóm ankyl) có thể bị oxi hóa bởi KMnO₄ tạo thành axit benzoic.
-
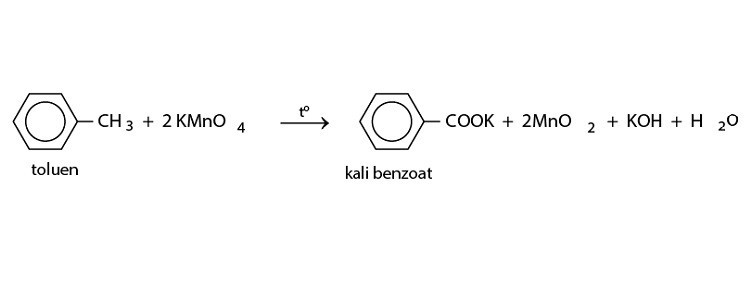 Phản ứng oxi hóa không hoàn toàn
Phản ứng oxi hóa không hoàn toàn
4.3. Ứng Dụng của Hiđrocacbon Thơm
Benzen và toluen là nguyên liệu quan trọng trong công nghiệp hóa chất, được sử dụng để sản xuất nhựa, sợi tổng hợp, thuốc nhuộm, dược phẩm, v.v. Chúng được sản xuất chủ yếu từ nhựa than đá hoặc từ quá trình dehydro hóa đóng vòng hexan và heptan.
5. Ứng Dụng Của Hiđrocacbon Trong Đời Sống và Công Nghiệp
Hiđrocacbon đóng vai trò vô cùng quan trọng trong nhiều lĩnh vực của đời sống và công nghiệp:
- Năng lượng: Hiđrocacbon là thành phần chính của nhiên liệu như xăng, dầu diesel, khí đốt tự nhiên, than đá. Chúng cung cấp năng lượng cho giao thông vận tải, sản xuất điện và hoạt động của các nhà máy.
- Nguyên liệu hóa học: Hiđrocacbon là nguyên liệu đầu vào để sản xuất nhiều loại hóa chất quan trọng, bao gồm nhựa, sợi tổng hợp, cao su, dung môi, chất tẩy rửa, phân bón, thuốc trừ sâu và dược phẩm.
- Vật liệu xây dựng: Một số polime được tạo ra từ hiđrocacbon (như polyetylen, polypropylen, PVC) được sử dụng rộng rãi trong xây dựng để sản xuất ống dẫn nước, vật liệu cách nhiệt, v.v.
- Đời sống hàng ngày: Hiđrocacbon có mặt trong nhiều sản phẩm tiêu dùng hàng ngày như mỹ phẩm, chất bôi trơn, chất dẻo, sơn, v.v.
Theo số liệu thống kê từ Tổng cục Thống kê, ngành công nghiệp hóa chất và sản phẩm hóa chất, trong đó có các sản phẩm từ hiđrocacbon, đóng góp khoảng 10-12% vào GDP của Việt Nam mỗi năm.
6. Các Thách Thức Liên Quan Đến Hiđrocacbon
Mặc dù có nhiều ứng dụng quan trọng, việc sử dụng hiđrocacbon cũng gây ra một số thách thức lớn:
- Ô nhiễm môi trường: Đốt cháy hiđrocacbon tạo ra khí thải gây ô nhiễm không khí, góp phần vào biến đổi khí hậu và các vấn đề sức khỏe. Theo báo cáo của Bộ Tài nguyên và Môi trường, giao thông vận tải (chủ yếu sử dụng nhiên liệu hiđrocacbon) là một trong những nguồn gây ô nhiễm không khí lớn nhất ở các đô thị lớn của Việt Nam.
- Cạn kiệt tài nguyên: Hiđrocacbon là tài nguyên không tái tạo, việc khai thác và sử dụng quá mức có thể dẫn đến cạn kiệt nguồn cung trong tương lai.
- Rủi ro cháy nổ: Hiđrocacbon dễ cháy và có thể gây ra các vụ cháy nổ nguy hiểm nếu không được xử lý và bảo quản đúng cách.
Để giảm thiểu các tác động tiêu cực này, cần có các giải pháp như:
- Sử dụng năng lượng tái tạo: Thay thế dần nhiên liệu hiđrocacbon bằng các nguồn năng lượng sạch hơn như năng lượng mặt trời, năng lượng gió, năng lượng sinh khối.
- Phát triển công nghệ sạch: Áp dụng các công nghệ tiên tiến để giảm thiểu khí thải và ô nhiễm trong quá trình khai thác, chế biến và sử dụng hiđrocacbon.
- Tiết kiệm năng lượng: Sử dụng năng lượng hiệu quả hơn trong các hoạt động sản xuất và tiêu dùng.
- Nghiên cứu và phát triển: Tìm kiếm các nguồn hiđrocacbon thay thế và các vật liệu mới thân thiện với môi trường hơn.
7. FAQ: Những Câu Hỏi Thường Gặp Về Hiđrocacbon
7.1. Hiđrocacbon có những loại liên kết nào?
Hiđrocacbon có thể chứa liên kết đơn (σ), liên kết đôi (σ và π) và liên kết ba (σ và 2π) giữa các nguyên tử cacbon.
7.2. Ankan và anken khác nhau như thế nào?
Ankan là hiđrocacbon no chỉ chứa liên kết đơn, trong khi anken là hiđrocacbon không no chứa một liên kết đôi.
7.3. Tại sao hiđrocacbon lại quan trọng?
Hiđrocacbon là nguồn nhiên liệu chính, nguyên liệu hóa học quan trọng và có nhiều ứng dụng trong đời sống và công nghiệp.
7.4. Hiđrocacbon có gây ô nhiễm môi trường không?
Có, việc đốt cháy hiđrocacbon tạo ra khí thải gây ô nhiễm không khí và góp phần vào biến đổi khí hậu.
7.5. Làm thế nào để giảm thiểu tác động tiêu cực của hiđrocacbon?
Sử dụng năng lượng tái tạo, phát triển công nghệ sạch, tiết kiệm năng lượng và nghiên cứu các nguồn hiđrocacbon thay thế.
7.6. Benzen có phải là một hiđrocacbon thơm?
Đúng, benzen là một hiđrocacbon thơm điển hình, có cấu trúc vòng với các liên kết pi liên hợp.
7.7. Công thức chung của anken là gì?
Công thức chung của anken là CₙH₂ₙ (n ≥ 2).
7.8. Ankin có những tính chất hóa học đặc trưng nào?
Ankin có tính chất hóa học đặc trưng là phản ứng cộng vào liên kết ba, tương tự như anken nhưng hoạt động hơn.
7.9. Xicloankan là gì?
Xicloankan là hiđrocacbon no mạch vòng, chỉ chứa liên kết đơn trong phân tử.
7.10. Ứng dụng của hiđrocacbon trong ngành vận tải là gì?
Hiđrocacbon được sử dụng làm nhiên liệu (xăng, dầu diesel, khí đốt) cho các phương tiện vận tải.
8. Xe Tải Mỹ Đình – Đối Tác Tin Cậy Của Bạn
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Hãy đến với XETAIMYDINH.EDU.VN, nơi bạn có thể tìm thấy mọi thứ bạn cần:
- Thông tin chi tiết và cập nhật: Về các loại xe tải có sẵn ở Mỹ Đình, Hà Nội.
- So sánh giá cả và thông số kỹ thuật: Giữa các dòng xe khác nhau để bạn dễ dàng lựa chọn.
- Tư vấn lựa chọn xe phù hợp: Với nhu cầu và ngân sách của bạn.
- Giải đáp thắc mắc: Về thủ tục mua bán, đăng ký và bảo dưỡng xe tải.
- Thông tin về dịch vụ sửa chữa xe tải uy tín: Trong khu vực Mỹ Đình.
Đừng chần chừ nữa! Hãy truy cập XETAIMYDINH.EDU.VN ngay hôm nay để được tư vấn và giải đáp mọi thắc mắc về xe tải ở Mỹ Đình!
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
Hotline: 0247 309 9988.
Trang web: XETAIMYDINH.EDU.VN.
