Liên kết hydro có vai trò quan trọng trong hóa học, ảnh hưởng đến nhiều tính chất của vật chất. Vậy, HCl có liên kết hydro không? Câu trả lời là không, HCl không hình thành liên kết hydro mạnh mẽ như các hợp chất chứa flo (F), oxy (O) hoặc nitơ (N). Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ giúp bạn hiểu rõ hơn về vấn đề này, đồng thời khám phá những yếu tố ảnh hưởng đến khả năng hình thành liên kết hydro, cũng như các hợp chất khác có khả năng tạo liên kết này. Qua đó, bạn sẽ nắm vững kiến thức về liên kết hydro và ứng dụng của nó trong thực tế, đồng thời khám phá những loại xe tải phù hợp với nhu cầu vận chuyển hàng hóa, tiết kiệm chi phí và nâng cao hiệu quả kinh doanh.
1. Liên Kết Hydro Là Gì?
Liên kết hydro, còn được gọi là liên kết hydrogen, là một loại lực hút tĩnh điện yếu xảy ra giữa một nguyên tử hydro (H) đã liên kết cộng hóa trị với một nguyên tử có độ âm điện cao (như N, O, F) và một nguyên tử khác có độ âm điện cao còn cặp electron tự do.
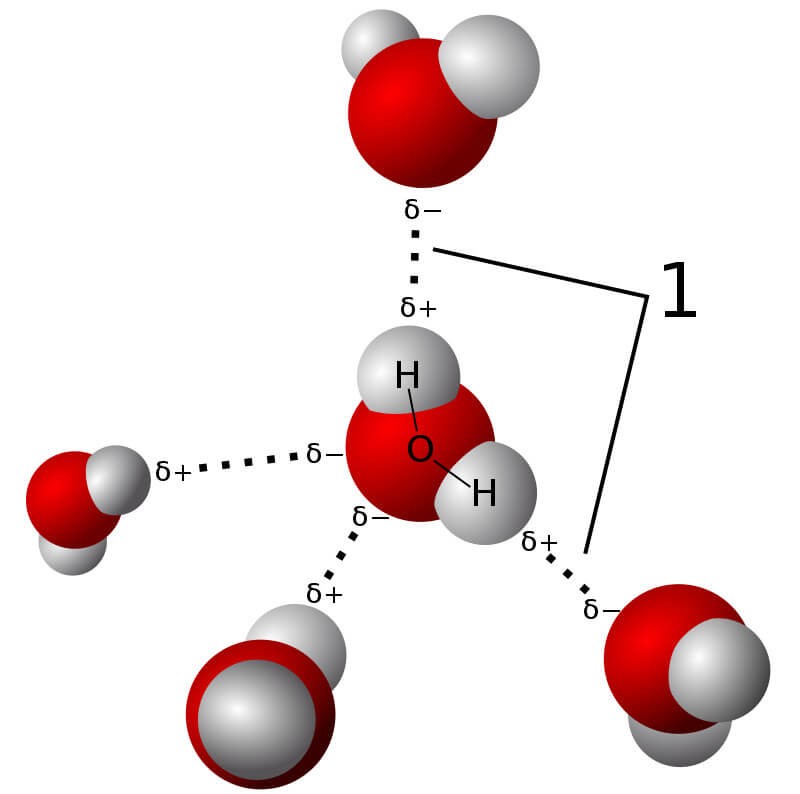 minh họa liên kết hydrogen
minh họa liên kết hydrogen
Liên kết hydro có thể xảy ra giữa các phân tử khác nhau (liên phân tử) hoặc giữa các phần khác nhau trong cùng một phân tử (nội phân tử). Năng lượng của liên kết hydro dao động từ 1 đến 40 kcal/mol, tùy thuộc vào các nguyên tử tham gia, hình học và môi trường xung quanh. Điều này làm cho liên kết hydro mạnh hơn tương tác Van der Waals nhưng yếu hơn liên kết cộng hóa trị hoặc ion. Liên kết hydro phổ biến trong các phân tử vô cơ như nước và các phân tử hữu cơ như protein và DNA.
2. Tại Sao HCl Không Tạo Liên Kết Hydro Mạnh?
Để hiểu tại sao HCl không tạo liên kết hydro mạnh, chúng ta cần xem xét các yếu tố sau:
2.1. Độ âm điện của clo (Cl)
Clo có độ âm điện là 3.16 theo thang Pauling. Mặc dù đây là một giá trị khá cao, nhưng nó vẫn thấp hơn đáng kể so với flo (3.98), oxy (3.44) và nitơ (3.04). Độ âm điện của clo không đủ cao để tạo ra một điện tích dương đủ lớn trên nguyên tử hydro trong phân tử HCl.
2.2. Kích thước của nguyên tử clo (Cl)
Kích thước của nguyên tử clo lớn hơn đáng kể so với flo, oxy và nitơ. Điều này làm cho mật độ điện tích âm trên clo giảm xuống, làm giảm khả năng hút các nguyên tử hydro của phân tử HCl khác.
2.3. Tính phân cực của liên kết H-Cl
Liên kết H-Cl phân cực, nhưng không phân cực mạnh như liên kết H-F, H-O hoặc H-N. Điều này có nghĩa là điện tích dương trên hydro trong HCl không đủ lớn để tạo ra một liên kết hydro mạnh.
2.4. So sánh với HF, H2O và NH3
- HF: Flo có độ âm điện cao nhất, tạo ra liên kết hydro mạnh nhất.
- H2O: Oxy có độ âm điện cao và kích thước nhỏ, tạo ra liên kết hydro mạnh mẽ. Liên kết hydro giữa các phân tử nước là nguyên nhân của nhiều tính chất đặc biệt của nước, chẳng hạn như nhiệt độ sôi cao và sức căng bề mặt lớn.
- NH3: Nitơ cũng có độ âm điện đủ cao để tạo ra liên kết hydro, mặc dù không mạnh bằng HF hoặc H2O.
2.5. Nghiên cứu khoa học về liên kết hydro trong HCl
Theo một nghiên cứu của Đại học California, Berkeley, sử dụng phương pháp quang phổ hồng ngoại, đã chỉ ra rằng HCl có khả năng tạo liên kết hydro yếu với một số phân tử nhất định trong điều kiện đặc biệt, chẳng hạn như trong dung môi có độ phân cực cao hoặc ở nhiệt độ rất thấp. Tuy nhiên, trong điều kiện thông thường, liên kết hydro giữa các phân tử HCl là rất yếu và không đáng kể.
3. Ý Định Tìm Kiếm Của Người Dùng Về “HCl Có Liên Kết Hydro Không?”
Dưới đây là 5 ý định tìm kiếm phổ biến của người dùng khi tìm kiếm từ khóa “HCl có liên kết hydro không?”:
- Tìm kiếm câu trả lời trực tiếp: Người dùng muốn biết ngay lập tức liệu HCl có tạo liên kết hydro hay không.
- Tìm hiểu lý do: Người dùng muốn hiểu tại sao HCl có hoặc không có khả năng tạo liên kết hydro.
- So sánh với các hợp chất khác: Người dùng muốn so sánh khả năng tạo liên kết hydro của HCl với các hợp chất tương tự như HF, H2O, NH3.
- Tìm kiếm thông tin chi tiết: Người dùng muốn tìm hiểu sâu hơn về các yếu tố ảnh hưởng đến khả năng tạo liên kết hydro của HCl, chẳng hạn như độ âm điện, kích thước nguyên tử, tính phân cực của liên kết.
- Tìm kiếm ứng dụng thực tế: Người dùng muốn biết liên kết hydro (hoặc thiếu nó) trong HCl ảnh hưởng đến các ứng dụng thực tế của hợp chất này như thế nào.
4. Các Tính Chất Đặc Trưng Của Liên Kết Hydro
Liên kết hydro có những tính chất đặc trưng sau:
- Trạng thái của chất: Các chất có khả năng tạo liên kết hydro mạnh thường tồn tại ở trạng thái lỏng hoặc rắn ở nhiệt độ phòng, do các liên kết hydro liên phân tử giữ các phân tử lại gần nhau hơn. Ví dụ, nước (H2O) là chất lỏng ở nhiệt độ phòng do liên kết hydro giữa các phân tử nước.
- Nhiệt độ nóng chảy và nhiệt độ sôi: Các chất có liên kết hydro có nhiệt độ nóng chảy và nhiệt độ sôi cao hơn so với các chất tương tự không có liên kết hydro. Điều này là do cần nhiều năng lượng hơn để phá vỡ các liên kết hydro và chuyển chất từ trạng thái rắn sang lỏng hoặc từ lỏng sang khí.
- Độ tan: Các chất có khả năng tạo liên kết hydro với nước thường tan tốt trong nước. Điều này là do các liên kết hydro giữa các phân tử nước và các phân tử chất tan giúp ổn định dung dịch. Ví dụ, etanol (C2H5OH) tan tốt trong nước do có khả năng tạo liên kết hydro với nước.
- Độ điện ly: Các chất có liên kết hydro yếu thường khó điện ly. Điều này là do các liên kết hydro giữ các ion lại với nhau, làm giảm khả năng chúng phân ly thành các ion tự do trong dung dịch.
5. Liên Kết Hydro Trong Nước
Các phân tử nước (H2O) tương tác với nhau thông qua liên kết hydro. Mỗi phân tử nước có thể tạo ra tối đa bốn liên kết hydro với các phân tử nước khác, tạo thành một mạng lưới ba chiều phức tạp.
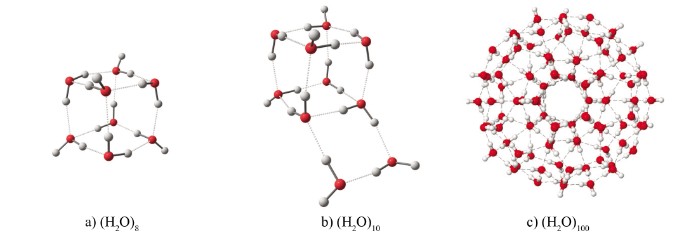 cụm phân tử nước hình thành từ liên kết hydrogen
cụm phân tử nước hình thành từ liên kết hydrogen
Liên kết hydro trong nước chịu trách nhiệm cho nhiều tính chất độc đáo của nước, bao gồm:
- Sức căng bề mặt cao: Các phân tử nước trên bề mặt chất lỏng liên kết với nhau bằng liên kết hydro, tạo ra một lực kéo vào bên trong làm cho bề mặt nước co lại.
- Nhiệt dung riêng cao: Nước có thể hấp thụ một lượng lớn nhiệt mà không tăng nhiệt độ đáng kể. Điều này là do một phần năng lượng nhiệt được sử dụng để phá vỡ các liên kết hydro, thay vì làm tăng động năng của các phân tử nước.
- Tính chất dung môi: Nước là một dung môi tuyệt vời cho nhiều chất phân cực và ion. Điều này là do nước có thể tạo liên kết hydro với các chất tan, giúp chúng hòa tan trong nước.
6. Vai Trò Và Ảnh Hưởng Của Liên Kết Hydro Đến Tính Chất Vật Lý Của Nước
Liên kết hydro có vai trò quan trọng trong việc xác định các tính chất vật lý của nước:
6.1. Đặc điểm tập hợp
Liên kết hydro cho phép các phân tử nước tập hợp lại với nhau, ngay cả ở thể hơi, tạo thành các cụm phân tử. Kích thước của các cụm phân tử này thay đổi tùy thuộc vào điều kiện nhiệt độ và áp suất.
6.2. Nhiệt độ sôi và nhiệt độ nóng chảy
Nước có nhiệt độ sôi và nhiệt độ nóng chảy cao hơn so với các chất có khối lượng phân tử tương đương. Điều này là do các phân tử nước liên kết chặt chẽ với nhau bằng liên kết hydro, cần nhiều năng lượng hơn để phá vỡ các liên kết này và chuyển nước từ trạng thái rắn sang lỏng hoặc từ lỏng sang khí.
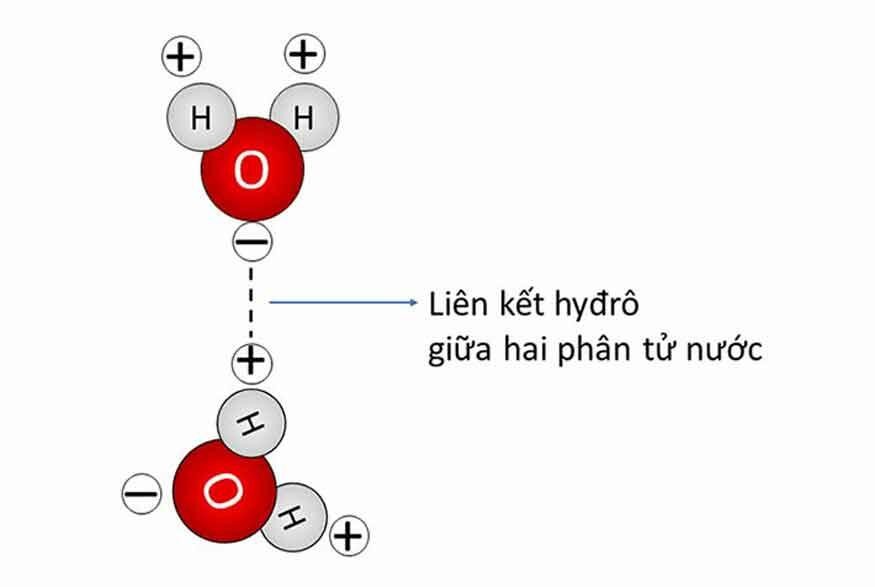 Liên kết hydrogen giữa 2 phân tử nước khá chặt chẽ
Liên kết hydrogen giữa 2 phân tử nước khá chặt chẽ
7. Ứng Dụng Của Liên Kết Hydro Trong Đời Sống Và Công Nghiệp
Liên kết hydro có nhiều ứng dụng quan trọng trong đời sống và công nghiệp:
- Sinh học: Liên kết hydro đóng vai trò quan trọng trong cấu trúc và chức năng của protein, DNA và các phân tử sinh học khác. Ví dụ, liên kết hydro giúp giữ hai mạch của DNA xoắn kép lại với nhau.
- Hóa học: Liên kết hydro ảnh hưởng đến tính chất của nhiều hợp chất hóa học, bao gồm độ tan, nhiệt độ sôi và khả năng phản ứng.
- Công nghiệp: Liên kết hydro được sử dụng trong nhiều ứng dụng công nghiệp, chẳng hạn như sản xuất giấy, dệt may và chất kết dính.
8. Các Hợp Chất Khác Có Khả Năng Tạo Liên Kết Hydro
Ngoài nước, nhiều hợp chất khác có khả năng tạo liên kết hydro, bao gồm:
- Alcol (R-OH): Alcol có nhóm hydroxyl (-OH) có thể tạo liên kết hydro với các phân tử alcol khác hoặc với nước. Ví dụ, etanol (C2H5OH) tan tốt trong nước do có khả năng tạo liên kết hydro với nước.
- Axit cacboxylic (R-COOH): Axit cacboxylic có nhóm cacboxyl (-COOH) có thể tạo liên kết hydro với các phân tử axit cacboxylic khác hoặc với nước.
- Amin (R-NH2, R2-NH, R3-N): Amin có nhóm amino (-NH2, -NH, -N) có thể tạo liên kết hydro với các phân tử amin khác hoặc với nước.
- Amoniac (NH3): Amoniac có khả năng tạo liên kết hydro mạnh mẽ, tương tự như nước, do có ba nguyên tử hydro liên kết với một nguyên tử nitơ có độ âm điện cao.
9. So Sánh Liên Kết Hydro Với Các Loại Liên Kết Khác
Để hiểu rõ hơn về liên kết hydro, chúng ta hãy so sánh nó với các loại liên kết khác:
| Loại liên kết | Độ mạnh | Bản chất | Ví dụ |
|---|---|---|---|
| Liên kết cộng hóa trị | Mạnh | Chia sẻ electron giữa các nguyên tử | H2, CH4 |
| Liên kết ion | Mạnh | Lực hút tĩnh điện giữa các ion trái dấu | NaCl, MgO |
| Liên kết kim loại | Mạnh | Chia sẻ electron giữa các nguyên tử kim loại | Cu, Fe |
| Liên kết hydro | Yếu | Lực hút tĩnh điện giữa H và nguyên tử âm điện | H2O, NH3 |
| Tương tác Van der Waals | Rất yếu | Lực hút tạm thời do biến động điện tích | He, Ne |
10. FAQ – Các Câu Hỏi Thường Gặp Về Liên Kết Hydro
Dưới đây là một số câu hỏi thường gặp về liên kết hydro:
10.1. Liên kết hydro mạnh hay yếu?
Liên kết hydro là một loại liên kết yếu, yếu hơn nhiều so với liên kết cộng hóa trị, liên kết ion và liên kết kim loại. Tuy nhiên, nó mạnh hơn tương tác Van der Waals.
10.2. Những yếu tố nào ảnh hưởng đến độ mạnh của liên kết hydro?
Độ mạnh của liên kết hydro phụ thuộc vào độ âm điện của các nguyên tử tham gia, khoảng cách giữa các nguyên tử và góc giữa các liên kết.
10.3. Liên kết hydro có vai trò gì trong sinh học?
Liên kết hydro đóng vai trò quan trọng trong cấu trúc và chức năng của protein, DNA và các phân tử sinh học khác.
10.4. Tại sao nước có nhiệt độ sôi cao bất thường?
Nước có nhiệt độ sôi cao bất thường do các phân tử nước liên kết với nhau bằng liên kết hydro mạnh mẽ.
10.5. Tại sao nước đá lại nổi trên mặt nước?
Nước đá nổi trên mặt nước vì nước đá có cấu trúc tinh thể mở, trong đó các phân tử nước được liên kết với nhau bằng liên kết hydro, tạo ra một cấu trúc ít đặc hơn nước lỏng.
10.6. Liên kết hydro có trong những hợp chất nào khác ngoài nước?
Liên kết hydro có trong nhiều hợp chất khác, bao gồm alcol, axit cacboxylic, amin và amoniac.
10.7. Liên kết hydro có ứng dụng gì trong công nghiệp?
Liên kết hydro được sử dụng trong nhiều ứng dụng công nghiệp, chẳng hạn như sản xuất giấy, dệt may và chất kết dính.
10.8. Làm thế nào để phân biệt liên kết hydro với các loại liên kết khác?
Liên kết hydro có thể được phân biệt với các loại liên kết khác bằng độ mạnh của nó, bản chất của lực hút và các tính chất vật lý mà nó ảnh hưởng.
10.9. Tại sao HCl không tạo liên kết hydro mạnh?
HCl không tạo liên kết hydro mạnh do độ âm điện của clo không đủ cao, kích thước của nguyên tử clo lớn và liên kết H-Cl không phân cực mạnh như liên kết H-F, H-O hoặc H-N.
10.10. Liên kết hydro có ảnh hưởng đến độ tan của các chất không?
Có, liên kết hydro ảnh hưởng đến độ tan của các chất. Các chất có khả năng tạo liên kết hydro với nước thường tan tốt trong nước.
Kết Luận
Mặc dù HCl có tính phân cực, nhưng không thể tạo ra liên kết hydro mạnh mẽ như các hợp chất chứa F, O, N. Điều này là do độ âm điện và kích thước của nguyên tử clo không đủ để tạo ra lực hút mạnh. Tuy nhiên, liên kết hydro vẫn là một chủ đề quan trọng trong hóa học, ảnh hưởng đến nhiều tính chất của vật chất và có nhiều ứng dụng trong đời sống và công nghiệp.
Nếu bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình, hãy truy cập XETAIMYDINH.EDU.VN. Chúng tôi cung cấp thông tin cập nhật về các loại xe tải, so sánh giá cả và thông số kỹ thuật, tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách, giải đáp các thắc mắc liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải.
Liên hệ ngay với Xe Tải Mỹ Đình để được tư vấn và giải đáp mọi thắc mắc!
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
Hãy để Xe Tải Mỹ Đình đồng hành cùng bạn trên mọi nẻo đường!
