H2so4 Hno3 đóng vai trò quan trọng trong nhiều ngành công nghiệp, từ sản xuất phân bón đến tổng hợp hóa học. Hãy cùng XETAIMYDINH.EDU.VN khám phá chi tiết về ứng dụng và các lưu ý quan trọng khi sử dụng hai hợp chất này để đảm bảo an toàn và hiệu quả nhé!
1. Axit H2SO4 HNO3 Là Gì Và Tính Chất Của Chúng Ra Sao?
Axit sulfuric (H2SO4) và axit nitric (HNO3) là hai hóa chất quan trọng với nhiều ứng dụng trong công nghiệp và đời sống. Vậy, tính chất đặc trưng của từng loại axit này là gì?
Axit sulfuric (H2SO4) và axit nitric (HNO3) đều là những hóa chất quan trọng với nhiều ứng dụng, nhưng chúng có những tính chất và đặc điểm khác biệt cần lưu ý.
1.1. Axit Sunfuric (H2SO4)
- Định nghĩa: Axit sunfuric là một axit vô cơ mạnh, có công thức hóa học là H2SO4.
- Tính chất vật lý:
- Chất lỏng sánh như dầu, không màu hoặc hơi vàng.
- Không bay hơi, hút ẩm mạnh.
- Tan vô hạn trong nước và tỏa nhiệt lớn khi tan.
- Tính chất hóa học:
- Tính axit mạnh: Tác dụng với kim loại, oxit bazơ, bazơ và muối.
- Tính oxi hóa mạnh: Đặc biệt khi ở trạng thái đậm đặc và nóng, có thể oxi hóa nhiều kim loại (kể cả Ag, Au) và phi kim.
- Tính háo nước: Hút nước từ môi trường xung quanh, gây cháy các chất hữu cơ như giấy, vải…
1.2. Axit Nitric (HNO3)
- Định nghĩa: Axit nitric là một axit vô cơ mạnh, có công thức hóa học là HNO3.
- Tính chất vật lý:
- Chất lỏng không màu, bốc khói mạnh trong không khí ẩm.
- Có mùi đặc trưng, gây ngạt.
- Kém bền, dễ bị phân hủy bởi ánh sáng và nhiệt.
- Tính chất hóa học:
- Tính axit mạnh: Tác dụng với kim loại, oxit bazơ, bazơ và muối.
- Tính oxi hóa cực mạnh: Oxi hóa hầu hết các kim loại (trừ Au, Pt), nhiều phi kim và hợp chất hữu cơ.
- Khả năng tạo phức: Tạo phức với một số kim loại chuyển tiếp.
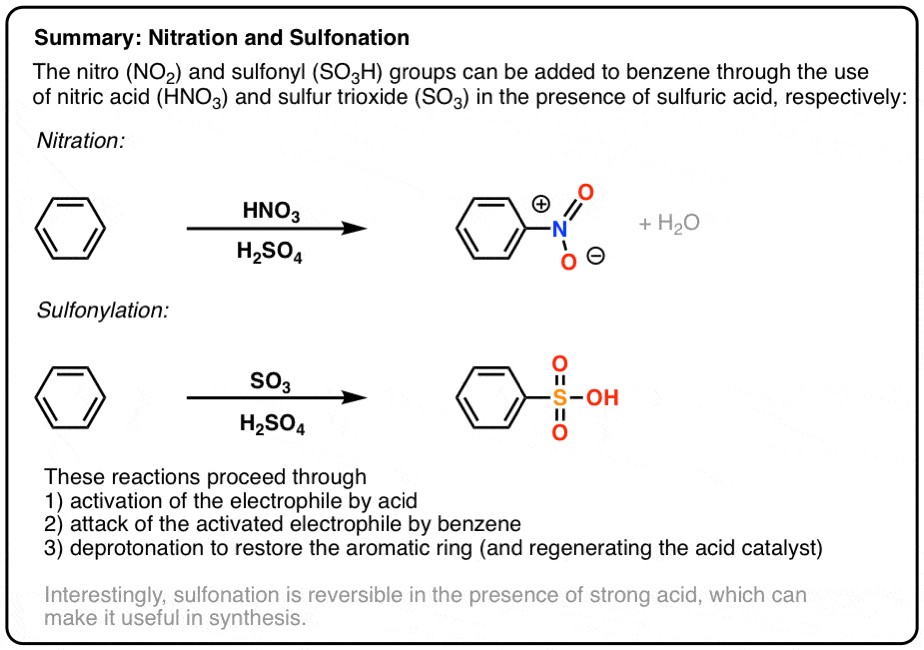 Axit Sunfuric H2SO4 và Axit Nitric HNO3: Các phản ứng và ứng dụng quan trọng trong công nghiệp và phòng thí nghiệm
Axit Sunfuric H2SO4 và Axit Nitric HNO3: Các phản ứng và ứng dụng quan trọng trong công nghiệp và phòng thí nghiệm
2. Ứng Dụng Quan Trọng Của H2SO4 HNO3 Trong Đời Sống Và Sản Xuất?
Axit sulfuric (H2SO4) và axit nitric (HNO3) là hai hóa chất có vai trò không thể thiếu trong nhiều lĩnh vực của đời sống và sản xuất. Chúng ta hãy cùng điểm qua những ứng dụng quan trọng nhất của chúng.
2.1. Ứng Dụng Của Axit Sunfuric (H2SO4)
- Sản xuất phân bón: H2SO4 là nguyên liệu chính để sản xuất các loại phân bón như super lân, amoni sunfat, giúp cung cấp dinh dưỡng cho cây trồng. Theo số liệu từ Tổng cục Thống kê, năm 2023, Việt Nam đã sản xuất hơn 2 triệu tấn phân bón các loại, trong đó H2SO4 đóng vai trò quan trọng.
- Sản xuất hóa chất: Được sử dụng để sản xuất nhiều loại hóa chất khác như axit clohydric (HCl), natri sunfat (Na2SO4), các loại thuốc trừ sâu, chất tẩy rửa…
- Công nghiệp luyện kim: Dùng để xử lý bề mặt kim loại, loại bỏ tạp chất, tăng độ bền và tính thẩm mỹ.
- Sản xuất chất dẻo, tơ sợi: Tham gia vào quá trình sản xuất nhiều loại polymer, sợi tổng hợp như rayon, nylon.
- Ắc quy: Dung dịch H2SO4 loãng được sử dụng làm chất điện ly trong ắc quy chì, cung cấp năng lượng cho các thiết bị điện.
- Xử lý nước thải: Sử dụng để điều chỉnh độ pH của nước thải, giúp loại bỏ các chất ô nhiễm.
2.2. Ứng Dụng Của Axit Nitric (HNO3)
- Sản xuất phân bón: HNO3 là nguyên liệu quan trọng để sản xuất phân đạm (như amoni nitrat, canxi nitrat), cung cấp nitơ cho cây trồng.
- Sản xuất thuốc nổ: HNO3 là thành phần chính trong nhiều loại thuốc nổ như TNT (trinitrotoluen), nitroglycerin, được sử dụng trong quân sự và khai thác mỏ.
- Sản xuất hóa chất: Dùng để sản xuất các hợp chất hữu cơ như nitrobenzen, anilin, các loại thuốc nhuộm, dược phẩm…
- Công nghiệp luyện kim: Sử dụng để khắc kim loại, làm sạch bề mặt và tách các kim loại quý.
- Tẩy rửa và khử trùng: Dung dịch HNO3 loãng được sử dụng để tẩy rửa các thiết bị y tế, khử trùng trong công nghiệp thực phẩm.
- Sản xuất nhựa và sợi tổng hợp: HNO3 tham gia vào quá trình sản xuất một số loại nhựa và sợi tổng hợp như nylon.
3. Cơ Chế Phản Ứng Nitrat Hóa Benzen Với HNO3/H2SO4 Diễn Ra Như Thế Nào?
Nitrat hóa benzen là một phản ứng quan trọng trong hóa học hữu cơ, trong đó một nhóm nitro (-NO2) được gắn vào vòng benzen. Phản ứng này thường được thực hiện bằng cách sử dụng axit nitric (HNO3) làm chất nitrat hóa và axit sulfuric (H2SO4) làm chất xúc tác.
Cơ chế phản ứng nitrat hóa benzen với HNO3/H2SO4 diễn ra qua các giai đoạn sau:
3.1. Tạo ra tác nhân electrophile (ion nitroni, NO2+)
- Axit nitric (HNO3) phản ứng với axit sulfuric (H2SO4) để tạo ra ion nitroni (NO2+), một tác nhân electrophile mạnh.
- H2SO4 đóng vai trò là chất xúc tác, giúp tăng tốc độ phản ứng bằng cách proton hóa HNO3, tạo điều kiện cho sự hình thành NO2+.
- HNO3 + H2SO4 ⇌ H2NO3+ + HSO4-
- H2NO3+ ⇌ NO2+ + H2O
3.2. Tấn công electrophile vào vòng benzen
- Ion nitroni (NO2+) tấn công vào vòng benzen, tạo thành một phức chất π (pi complex).
- Phức chất π này chuyển thành một ion arenium (carbocation trung gian), trong đó nguyên tử carbon mang nhóm nitro trở thành trung tâm tứ diện.
3.3. Loại bỏ proton và tái tạo tính thơm
- Ion arenium mất một proton (H+) từ nguyên tử carbon mang nhóm nitro.
- Quá trình này tái tạo lại liên kết đôi trong vòng benzen, khôi phục tính thơm của vòng và tạo thành nitrobenzen.
- HSO4- (từ giai đoạn 1) đóng vai trò là base, lấy proton từ ion arenium.
Tóm tắt cơ chế:
- Tạo NO2+: HNO3 + 2H2SO4 → NO2+ + H3O+ + 2HSO4-
- Tấn công vòng benzen: Benzen + NO2+ → [C6H6NO2]+ (phức sigma)
- Tái tạo tính thơm: [C6H6NO2]+ + HSO4- → C6H5NO2 + H2SO4
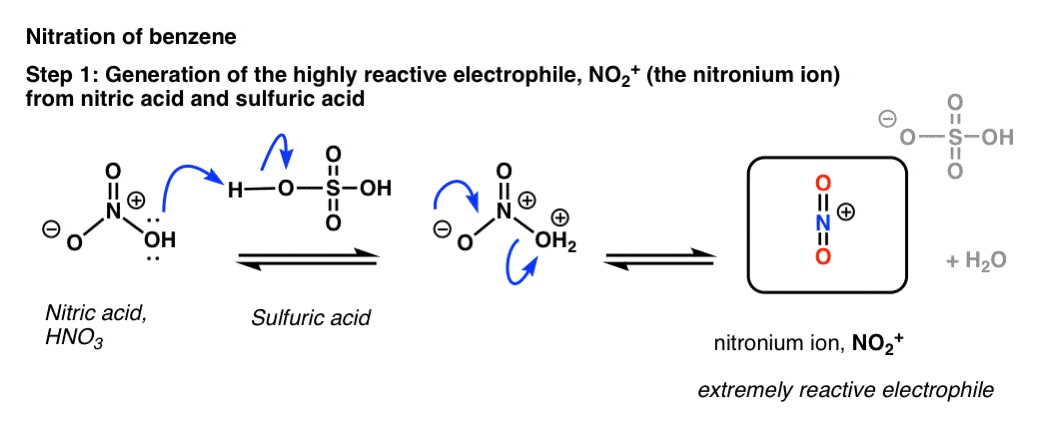 Cơ chế chi tiết phản ứng nitrat hóa benzen sử dụng H2SO4 và HNO3, tạo ra nitrobenzen
Cơ chế chi tiết phản ứng nitrat hóa benzen sử dụng H2SO4 và HNO3, tạo ra nitrobenzen
4. Sulfonat Hóa Benzen Với SO3/H2SO4: Cơ Chế Và Ứng Dụng Thực Tế?
Sulfonat hóa benzen là một phản ứng quan trọng trong hóa học hữu cơ, trong đó một nhóm axit sulfonic (-SO3H) được gắn vào vòng benzen. Phản ứng này thường được thực hiện bằng cách sử dụng lưu huỳnh trioxit (SO3) làm chất sulfonat hóa và axit sulfuric (H2SO4) làm chất xúc tác.
Cơ chế phản ứng sulfonat hóa benzen với SO3/H2SO4 diễn ra qua các giai đoạn sau:
4.1. Tạo ra tác nhân electrophile (SO3H+)
- Lưu huỳnh trioxit (SO3) phản ứng với axit sulfuric (H2SO4) để tạo ra tác nhân electrophile mạnh hơn, có thể là HSO3+ hoặc proton hóa SO3.
- H2SO4 đóng vai trò là chất xúc tác, giúp tăng tốc độ phản ứng bằng cách hoạt hóa SO3.
- SO3 + H2SO4 ⇌ HSO3+ + HSO4-
4.2. Tấn công electrophile vào vòng benzen
- Tác nhân electrophile (HSO3+) tấn công vào vòng benzen, tạo thành một phức chất π (pi complex).
- Phức chất π này chuyển thành một ion arenium (carbocation trung gian), trong đó nguyên tử carbon mang nhóm axit sulfonic trở thành trung tâm tứ diện.
4.3. Loại bỏ proton và tái tạo tính thơm
- Ion arenium mất một proton (H+) từ nguyên tử carbon mang nhóm axit sulfonic.
- Quá trình này tái tạo lại liên kết đôi trong vòng benzen, khôi phục tính thơm của vòng và tạo thành axit benzenesulfonic.
- HSO4- (từ giai đoạn 1) đóng vai trò là base, lấy proton từ ion arenium.
Tóm tắt cơ chế:
- Tạo HSO3+: SO3 + H2SO4 ⇌ HSO3+ + HSO4-
- Tấn công vòng benzen: Benzen + HSO3+ → [C6H6SO3H]+ (phức sigma)
- Tái tạo tính thơm: [C6H6SO3H]+ + HSO4- → C6H5SO3H + H2SO4
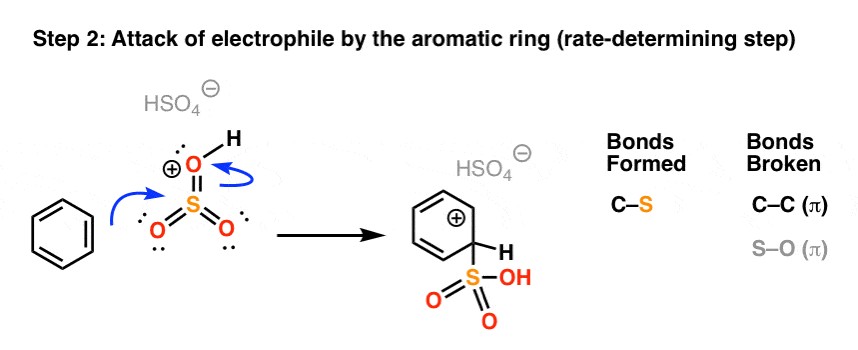 Phản ứng sulfon hóa benzen bằng SO3 và H2SO4: Cơ chế, ứng dụng và các yếu tố ảnh hưởng đến hiệu suất
Phản ứng sulfon hóa benzen bằng SO3 và H2SO4: Cơ chế, ứng dụng và các yếu tố ảnh hưởng đến hiệu suất
Ứng dụng thực tế của phản ứng sulfonat hóa benzen:
- Sản xuất chất tẩy rửa: Axit benzenesulfonic và các dẫn xuất của nó được sử dụng rộng rãi trong sản xuất chất tẩy rửa và chất hoạt động bề mặt.
- Sản xuất thuốc nhuộm: Các hợp chất sulfonat hóa là thành phần quan trọng trong nhiều loại thuốc nhuộm.
- Tổng hợp hữu cơ: Phản ứng sulfonat hóa được sử dụng để bảo vệ một vị trí trên vòng benzen trong quá trình tổng hợp hữu cơ phức tạp.
- Sản xuất nhựa trao đổi ion: Các polyme chứa nhóm axit sulfonic được sử dụng làm nhựa trao đổi ion trong xử lý nước và các ứng dụng khác.
5. Lưu Ý An Toàn Khi Sử Dụng Và Bảo Quản H2SO4 HNO3?
H2SO4 và HNO3 là những hóa chất nguy hiểm, có thể gây bỏng nặng, tổn thương mắt và hệ hô hấp nếu không được sử dụng và bảo quản đúng cách.
Dưới đây là những lưu ý an toàn quan trọng khi làm việc với H2SO4 và HNO3:
5.1. Trang Bị Bảo Hộ Cá Nhân (PPE)
- Kính bảo hộ: Đeo kính bảo hộ kín để bảo vệ mắt khỏi bị bắn hóa chất.
- Găng tay bảo hộ: Sử dụng găng tay chịu hóa chất (như nitrile, neoprene) để bảo vệ da tay.
- Áo choàng hoặc quần áo bảo hộ: Mặc áo choàng hoặc quần áo bảo hộ dài tay để tránh hóa chất tiếp xúc với da.
- Mặt nạ phòng độc: Nếu làm việc trong môi trường có nồng độ hơi axit cao, cần sử dụng mặt nạ phòng độc phù hợp.
5.2. Làm Việc Trong Khu Vực Thông Thoáng
- Luôn làm việc trong khu vực có hệ thống thông gió tốt để giảm thiểu hít phải hơi axit.
- Nếu không có hệ thống thông gió, hãy sử dụng quạt để đẩy hơi axit ra khỏi khu vực làm việc.
5.3. Pha Loãng Axit Đúng Cách
- Luôn thêm từ từ axit vào nước, không làm ngược lại.
- Sử dụng cốc thủy tinh chịu nhiệt hoặc bình pha loãng chuyên dụng.
- Khuấy đều dung dịch trong quá trình pha loãng để tránh nhiệt độ tăng đột ngột.
5.4. Xử Lý Sự Cố
- Tiếp xúc với da: Rửa ngay lập tức vùng da bị tiếp xúc với nhiều nước trong ít nhất 15 phút. Cởi bỏ quần áo bị nhiễm hóa chất. Tìm kiếm sự chăm sóc y tế nếu bị bỏng nặng.
- Tiếp xúc với mắt: Rửa mắt ngay lập tức với nhiều nước trong ít nhất 15 phút, giữ cho mí mắt mở. Tìm kiếm sự chăm sóc y tế ngay lập tức.
- Hít phải hơi axit: Di chuyển đến nơi thoáng khí. Nếu khó thở, cung cấp oxy và tìm kiếm sự chăm sóc y tế.
- Đổ tràn hóa chất: Sử dụng vật liệu hấp thụ (như cát, đất sét) để thấm hút hóa chất. Thu gom vật liệu đã thấm hút vào thùng chứa chịu hóa chất và xử lý theo quy định.
5.5. Bảo Quản Axit An Toàn
- Lưu trữ trong thùng chứa chịu hóa chất: Sử dụng thùng chứa làm từ vật liệu tương thích với axit (như polyethylene, polypropylene).
- Bảo quản ở nơi khô ráo, thoáng mát: Tránh ánh nắng trực tiếp và nhiệt độ cao.
- Để xa các chất không tương thích: Tránh xa các chất oxy hóa mạnh, chất khử, kim loại và vật liệu hữu cơ.
- Dán nhãn rõ ràng: Ghi rõ tên hóa chất, nồng độ và cảnh báo nguy hiểm trên thùng chứa.
- Kiểm tra định kỳ: Kiểm tra thùng chứa để phát hiện rò rỉ hoặc hư hỏng.
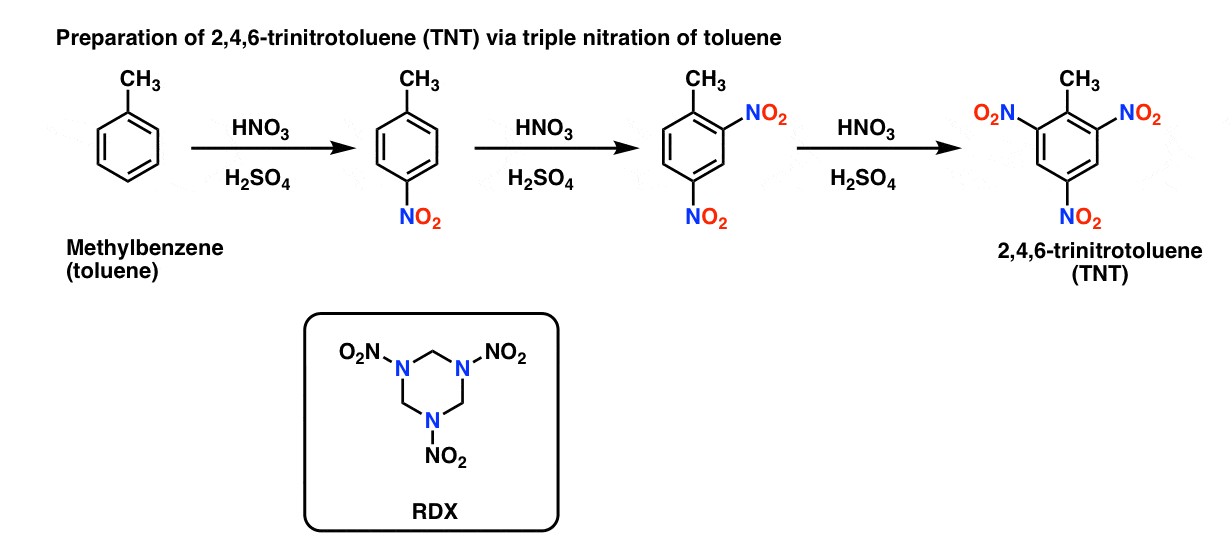 An toàn hóa chất: Hướng dẫn sử dụng và bảo quản H2SO4 và HNO3 trong phòng thí nghiệm và công nghiệp
An toàn hóa chất: Hướng dẫn sử dụng và bảo quản H2SO4 và HNO3 trong phòng thí nghiệm và công nghiệp
6. H2SO4 HNO3 Có Gây Ăn Mòn Xe Tải Không? Biện Pháp Phòng Ngừa?
Axit sulfuric (H2SO4) và axit nitric (HNO3) đều là những chất ăn mòn mạnh, có thể gây hại nghiêm trọng cho xe tải nếu tiếp xúc trực tiếp.
6.1. Mức Độ Ăn Mòn Của H2SO4 Và HNO3 Đối Với Xe Tải
- Axit sulfuric (H2SO4): H2SO4 có khả năng ăn mòn kim loại mạnh mẽ, đặc biệt là thép và nhôm, là những vật liệu chính cấu tạo nên khung gầm và thân xe tải. H2SO4 có thể gây ra hiện tượng gỉ sét, ăn mòn và phá hủy cấu trúc kim loại, làm giảm độ bền và tuổi thọ của xe.
- Axit nitric (HNO3): HNO3 cũng là một chất ăn mòn mạnh, có khả năng oxy hóa kim loại. HNO3 có thể gây ra hiện tượng ăn mòn và làm hỏng các bộ phận kim loại của xe tải, đặc biệt là các chi tiết máy và hệ thống nhiên liệu.
6.2. Các Bộ Phận Xe Tải Dễ Bị Ăn Mòn Nhất
- Khung gầm: Khung gầm là bộ phận chịu lực chính của xe tải, thường xuyên tiếp xúc với môi trường bên ngoài. Nếu tiếp xúc với H2SO4 hoặc HNO3, khung gầm có thể bị ăn mòn, làm giảm khả năng chịu tải và gây nguy hiểm khi vận hành.
- Thân xe: Thân xe tải, đặc biệt là các chi tiết làm từ kim loại, cũng có thể bị ăn mòn bởi H2SO4 và HNO3, ảnh hưởng đến tính thẩm mỹ và độ bền của xe.
- Hệ thống nhiên liệu: Các bộ phận của hệ thống nhiên liệu như bình xăng, ống dẫn nhiên liệu, bơm nhiên liệu… có thể bị ăn mòn bởi HNO3, gây tắc nghẽn, rò rỉ và ảnh hưởng đến hiệu suất động cơ.
- Hệ thống điện: Các đầu nối, dây điện và các thiết bị điện trên xe tải cũng có thể bị ăn mòn, gây chập điện, hư hỏng và ảnh hưởng đến hoạt động của xe.
6.3. Biện Pháp Phòng Ngừa Ăn Mòn
- Tránh để axit tiếp xúc trực tiếp với xe: Khi vận chuyển hoặc sử dụng H2SO4 và HNO3, cần đảm bảo thùng chứa kín, không bị rò rỉ. Nếu có sự cố tràn đổ, cần xử lý ngay lập tức bằng cách trung hòa axit và rửa sạch khu vực bị ảnh hưởng.
- Sử dụng vật liệu chống ăn mòn: Nên sử dụng các vật liệu chống ăn mòn (như thép không gỉ, nhựa composite) cho các bộ phận quan trọng của xe tải, đặc biệt là khung gầm và hệ thống nhiên liệu.
- Sơn phủ bảo vệ: Sơn phủ một lớp sơn chống ăn mòn lên bề mặt kim loại của xe tải có thể giúp bảo vệ khỏi tác động của axit và các yếu tố môi trường khác.
- Vệ sinh xe thường xuyên: Rửa xe thường xuyên bằng nước sạch và chất tẩy rửa trung tính để loại bỏ bụi bẩn, hóa chất và các chất gây ăn mòn khác.
- Kiểm tra định kỳ: Kiểm tra định kỳ các bộ phận của xe tải để phát hiện sớm các dấu hiệu ăn mòn và có biện pháp xử lý kịp thời.
7. Ảnh Hưởng Của H2SO4 HNO3 Đến Môi Trường Và Sức Khỏe Cộng Đồng?
H2SO4 và HNO3 là những hóa chất có thể gây ra những tác động tiêu cực đến môi trường và sức khỏe cộng đồng nếu không được quản lý và sử dụng đúng cách.
7.1. Tác Động Đến Môi Trường
- Ô nhiễm không khí: H2SO4 và HNO3 có thể thải ra môi trường dưới dạng hơi hoặc bụi, gây ô nhiễm không khí. Các chất này có thể gây ra mưa axit, ảnh hưởng đến hệ sinh thái và các công trình xây dựng.
- Ô nhiễm nguồn nước: Nếu H2SO4 và HNO3 rò rỉ hoặc tràn đổ vào nguồn nước, chúng có thể làm giảm độ pH, gây ô nhiễm và ảnh hưởng đến đời sống của các sinh vật thủy sinh.
- Ô nhiễm đất: H2SO4 và HNO3 có thể làm thay đổi tính chất của đất, gây ảnh hưởng đến sự sinh trưởng của cây trồng và các vi sinh vật có lợi trong đất.
7.2. Tác Động Đến Sức Khỏe Cộng Đồng
- Đường hô hấp: Hít phải hơi H2SO4 và HNO3 có thể gây kích ứng đường hô hấp, gây ho, khó thở, viêm phổi và các bệnh về đường hô hấp khác.
- Da và mắt: Tiếp xúc trực tiếp với H2SO4 và HNO3 có thể gây bỏng da, tổn thương mắt, thậm chí gây mù lòa.
- Tiêu hóa: Nuốt phải H2SO4 và HNO3 có thể gây bỏng miệng, thực quản và dạ dày, gây đau đớn và nguy hiểm đến tính mạng.
- Ảnh hưởng lâu dài: Tiếp xúc lâu dài với H2SO4 và HNO3 có thể gây ra các bệnh mãn tính như viêm phế quản, hen suyễn, ung thư phổi và các bệnh về da.
7.3. Biện Pháp Giảm Thiểu Tác Động
- Kiểm soát khí thải: Các nhà máy sản xuất và sử dụng H2SO4 và HNO3 cần trang bị hệ thống xử lý khí thải để giảm thiểu lượng hóa chất thải ra môi trường.
- Quản lý chất thải: Chất thải chứa H2SO4 và HNO3 cần được thu gom, xử lý và tiêu hủy đúng cách theo quy định của pháp luật.
- Sử dụng an toàn: Người lao động làm việc với H2SO4 và HNO3 cần được trang bị đầy đủ bảo hộ cá nhân và tuân thủ nghiêm ngặt các quy trình an toàn.
- Tuyên truyền nâng cao nhận thức: Cần tăng cường tuyên truyền, giáo dục để nâng cao nhận thức của cộng đồng về tác hại của H2SO4 và HNO3 đối với môi trường và sức khỏe, từ đó nâng cao ý thức bảo vệ môi trường và sức khỏe cộng đồng.
8. Mua H2SO4 HNO3 Ở Đâu Uy Tín, Chất Lượng Tại Hà Nội?
Việc lựa chọn nhà cung cấp uy tín, chất lượng là yếu tố quan trọng để đảm bảo an toàn và hiệu quả khi sử dụng H2SO4 và HNO3. Tại Hà Nội, có một số địa chỉ được đánh giá cao về chất lượng sản phẩm và dịch vụ.
Dưới đây là một số gợi ý:
- Các công ty hóa chất lớn:
- Công ty TNHH Hóa chất Việt Trì: Là một trong những nhà sản xuất hóa chất hàng đầu tại Việt Nam, cung cấp H2SO4 và HNO3 với nhiều nồng độ và quy cách đóng gói khác nhau.
- Công ty CP Hóa chất Cơ bản Miền Nam (Sovigaz): Chuyên sản xuất và kinh doanh các loại hóa chất cơ bản, bao gồm H2SO4 và HNO3, đảm bảo chất lượng và giá cả cạnh tranh.
- Các đại lý hóa chất uy tín:
- Công ty TNHH Thương mại và Dịch vụ Hóa chất Hà Nội: Cung cấp đa dạng các loại hóa chất, bao gồm H2SO4 và HNO3, với nguồn gốc rõ ràng và chất lượng đảm bảo.
- Công ty CP Vật tư và Hóa chất Bách Khoa: Là đại lý phân phối của nhiều hãng hóa chất nổi tiếng, cung cấp H2SO4 và HNO3 với đầy đủ chứng từ và kiểm định chất lượng.
- Các sàn thương mại điện tử chuyên về hóa chất:
- Một số sàn thương mại điện tử như Alibaba, Shopee… cũng có bán H2SO4 và HNO3, tuy nhiên cần lựa chọn nhà cung cấp uy tín và kiểm tra kỹ thông tin sản phẩm trước khi mua.
Khi lựa chọn nhà cung cấp, cần lưu ý các yếu tố sau:
- Uy tín và kinh nghiệm: Ưu tiên các nhà cung cấp có uy tín, kinh nghiệm lâu năm trong ngành hóa chất.
- Chất lượng sản phẩm: Yêu cầu nhà cung cấp cung cấp đầy đủ chứng từ, kiểm định chất lượng sản phẩm.
- Giá cả cạnh tranh: So sánh giá cả của nhiều nhà cung cấp để lựa chọn được mức giá tốt nhất.
- Dịch vụ hỗ trợ: Lựa chọn nhà cung cấp có dịch vụ hỗ trợ tốt, sẵn sàng tư vấn và giải đáp thắc mắc của khách hàng.
Lưu ý:
- Khi mua H2SO4 và HNO3, cần có đầy đủ giấy tờ chứng minh mục đích sử dụng hợp pháp.
- Tuân thủ các quy định về vận chuyển, bảo quản và sử dụng hóa chất nguy hiểm.
9. Giá H2SO4 HNO3 Hiện Nay Trên Thị Trường Là Bao Nhiêu?
Giá H2SO4 và HNO3 trên thị trường có thể biến động tùy thuộc vào nhiều yếu tố như nồng độ, quy cách đóng gói, số lượng mua, nhà cung cấp và thời điểm mua.
Dưới đây là thông tin tham khảo về giá H2SO4 và HNO3 trên thị trường Hà Nội (tháng 5/2024):
- Axit sulfuric (H2SO4):
- H2SO4 98%: Giá dao động từ 5.000 – 8.000 VNĐ/kg (tùy thuộc vào số lượng mua và nhà cung cấp).
- H2SO4 loãng (10-30%): Giá dao động từ 2.000 – 4.000 VNĐ/kg.
- Axit nitric (HNO3):
- HNO3 68%: Giá dao động từ 8.000 – 12.000 VNĐ/kg (tùy thuộc vào số lượng mua và nhà cung cấp).
- HNO3 đậm đặc (>90%): Giá có thể cao hơn, dao động từ 15.000 – 20.000 VNĐ/kg.
Lưu ý:
- Đây chỉ là giá tham khảo, giá thực tế có thể khác biệt tùy thuộc vào các yếu tố đã nêu trên.
- Nên liên hệ trực tiếp với các nhà cung cấp để có thông tin giá chính xác nhất.
- Khi mua số lượng lớn, có thể được hưởng chiết khấu và ưu đãi về giá.
Lời khuyên:
- Nên so sánh giá của nhiều nhà cung cấp trước khi quyết định mua.
- Lựa chọn nhà cung cấp uy tín, có chất lượng sản phẩm đảm bảo.
- Mua với số lượng phù hợp với nhu cầu sử dụng để tránh lãng phí và giảm thiểu rủi ro.
10. FAQ: Câu Hỏi Thường Gặp Về H2SO4 HNO3
Dưới đây là một số câu hỏi thường gặp về H2SO4 và HNO3, cùng với câu trả lời chi tiết để giúp bạn hiểu rõ hơn về hai loại hóa chất này:
1. H2SO4 và HNO3 có tác dụng gì trong sản xuất phân bón?
H2SO4 được sử dụng để sản xuất phân lân (super lân) và amoni sunfat, cung cấp photpho và nitơ cho cây trồng. HNO3 được sử dụng để sản xuất phân đạm (amoni nitrat, canxi nitrat), cung cấp nitơ cho cây trồng.
2. Tại sao phải pha loãng axit sulfuric trước khi sử dụng?
Pha loãng axit sulfuric giúp giảm nồng độ axit, giảm nguy cơ bỏng và ăn mòn. Quá trình pha loãng cũng tỏa nhiệt, vì vậy cần thực hiện từ từ và khuấy đều để tránh nhiệt độ tăng đột ngột.
3. Làm thế nào để nhận biết axit nitric bị phân hủy?
Axit nitric bị phân hủy sẽ có màu vàng hoặc nâu do tạo thành khí NO2. Axit đã bị phân hủy không nên sử dụng vì có thể gây ra các phản ứng phụ không mong muốn.
4. Có thể sử dụng H2SO4 và HNO3 để làm sạch cống bị tắc không?
Không nên sử dụng H2SO4 và HNO3 để làm sạch cống bị tắc vì chúng có thể gây ăn mòn đường ống, tạo ra khí độc và gây nguy hiểm cho người sử dụng.
5. H2SO4 và HNO3 có thể tác dụng với kim loại nào?
H2SO4 đặc nóng có thể tác dụng với hầu hết các kim loại (trừ Au, Pt). HNO3 có thể tác dụng với hầu hết các kim loại (trừ Au, Pt), tạo ra muối nitrat, nước và các sản phẩm khử khác (NO2, NO, N2O, NH4NO3).
6. Tại sao khi làm thí nghiệm với HNO3 đặc thường có khí màu nâu bay ra?
Khí màu nâu bay ra là khí NO2, sản phẩm của phản ứng HNO3 đặc với kim loại hoặc các chất hữu cơ. Khí NO2 rất độc, cần tránh hít phải.
7. H2SO4 và HNO3 có thể bảo quản trong thùng chứa bằng vật liệu gì?
H2SO4 và HNO3 nên được bảo quản trong thùng chứa làm từ vật liệu chịu axit như polyethylene (PE), polypropylene (PP), thủy tinh hoặc thép không gỉ.
8. Làm thế nào để xử lý H2SO4 và HNO3 bị đổ tràn?
Sử dụng vật liệu hấp thụ (cát, đất sét) để thấm hút axit, sau đó thu gom vào thùng chứa chịu hóa chất và xử lý theo quy định. Trung hòa axit bằng dung dịch kiềm yếu (như natri cacbonat) trước khi thải bỏ.
9. H2SO4 và HNO3 có thể gây cháy nổ không?
H2SO4 đậm đặc có thể gây cháy các chất hữu cơ do tính háo nước mạnh. HNO3 có thể gây nổ khi tiếp xúc với một số chất hữu cơ dễ cháy.
10. Có quy định nào về việc vận chuyển H2SO4 và HNO3 không?
Việc vận chuyển H2SO4 và HNO3 phải tuân thủ các quy định về vận chuyển hàng nguy hiểm của Bộ Giao thông Vận tải và các cơ quan chức năng liên quan.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Hãy truy cập ngay XETAIMYDINH.EDU.VN để được tư vấn và giải đáp mọi thắc mắc! Đội ngũ chuyên gia của chúng tôi luôn sẵn sàng hỗ trợ bạn lựa chọn chiếc xe tải phù hợp nhất với nhu cầu và ngân sách của bạn. Liên hệ ngay hotline 0247 309 9988 hoặc đến trực tiếp địa chỉ Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội để trải nghiệm dịch vụ chuyên nghiệp và tận tâm nhất!