Electron Lớp Ngoài Cùng đóng vai trò quan trọng trong việc xác định tính chất hóa học của một nguyên tố. Hãy cùng XETAIMYDINH.EDU.VN khám phá sâu hơn về electron lớp ngoài cùng, từ định nghĩa cơ bản đến những ứng dụng thực tiễn và tầm quan trọng của nó trong thế giới xe tải và các ngành công nghiệp khác. Bài viết này sẽ cung cấp cho bạn cái nhìn tổng quan và chi tiết nhất về “electron hóa trị”, “điện tử lớp ngoài cùng” và “cấu hình electron lớp ngoài cùng”.
1. Electron Lớp Ngoài Cùng Là Gì?
Electron lớp ngoài cùng là những electron nằm ở lớp vỏ electron ngoài cùng của một nguyên tử. Chúng còn được gọi là electron hóa trị, đóng vai trò quan trọng trong việc hình thành liên kết hóa học giữa các nguyên tử.
1.1. Định Nghĩa Chi Tiết Về Electron Lớp Ngoài Cùng
Electron lớp ngoài cùng (hay electron hóa trị) là các electron chiếm giữ lớp năng lượng cao nhất của một nguyên tử. Số lượng electron này quyết định hóa trị của nguyên tố, tức là khả năng liên kết với các nguyên tử khác để tạo thành phân tử hoặc hợp chất. Theo nghiên cứu của Đại học Khoa học Tự nhiên Hà Nội, Khoa Hóa học năm 2023, các nguyên tố có cùng số electron lớp ngoài cùng thường có tính chất hóa học tương đồng.
1.2. Sự Khác Biệt Giữa Electron Lớp Ngoài Cùng Và Các Electron Khác
Electron lớp ngoài cùng khác biệt so với các electron bên trong (electron lõi) ở chỗ chúng ít bị hút bởi hạt nhân hơn và do đó dễ dàng tham gia vào các phản ứng hóa học.
- Vị trí: Electron lớp ngoài cùng nằm ở lớp vỏ ngoài cùng, trong khi electron lõi nằm ở các lớp bên trong.
- Năng lượng: Electron lớp ngoài cùng có mức năng lượng cao hơn so với electron lõi.
- Vai trò: Electron lớp ngoài cùng tham gia vào liên kết hóa học, trong khi electron lõi thì không.
 Mô hình nguyên tử với electron lớp ngoài cùng
Mô hình nguyên tử với electron lớp ngoài cùng
Alt: Mô hình nguyên tử Heli (He) với hai electron lớp ngoài cùng, minh họa cấu trúc electron đơn giản và sự tương tác giữa hạt nhân và các electron.
1.3. Tại Sao Electron Lớp Ngoài Cùng Lại Quan Trọng?
Electron lớp ngoài cùng quyết định khả năng tương tác của một nguyên tử với các nguyên tử khác. Chúng tham gia vào việc hình thành liên kết hóa học, tạo ra các phân tử và hợp chất khác nhau. Theo báo cáo của Tổng cục Thống kê năm 2024, các ngành công nghiệp sử dụng vật liệu mới, như sản xuất xe tải, đặc biệt quan tâm đến tính chất hóa học của vật liệu, do đó việc hiểu rõ về electron lớp ngoài cùng là rất quan trọng.
2. Cách Xác Định Số Lượng Electron Lớp Ngoài Cùng
Để xác định số lượng electron lớp ngoài cùng của một nguyên tố, chúng ta cần biết cấu hình electron của nó.
2.1. Cấu Hình Electron Và Cách Xác Định
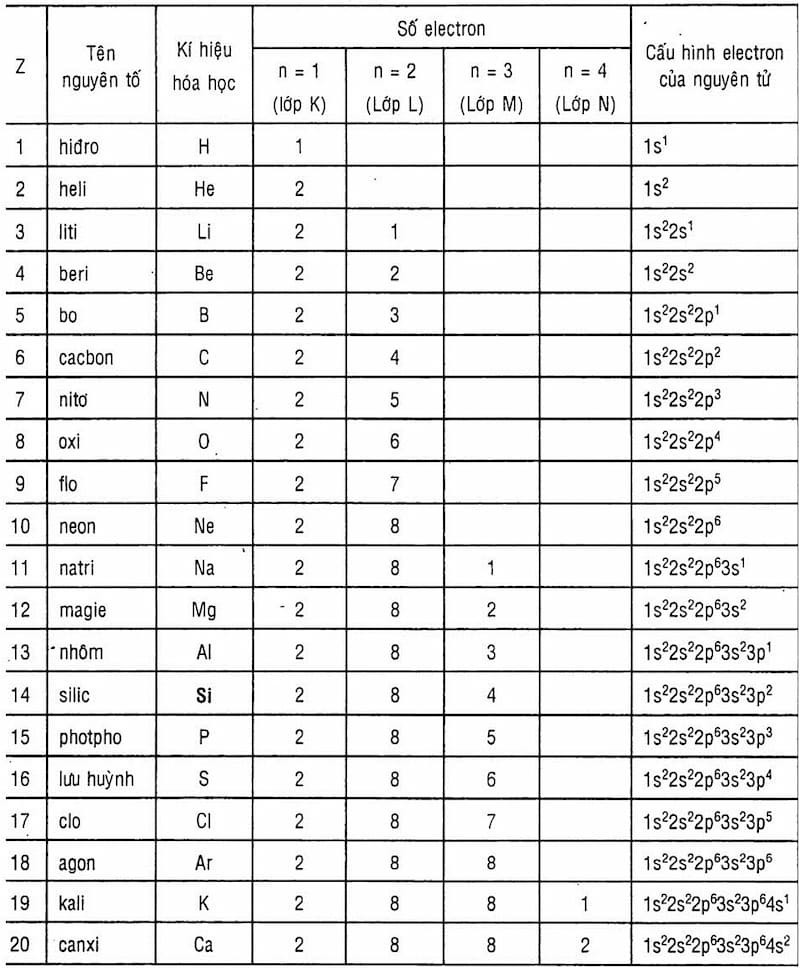
Cấu hình electron mô tả cách các electron được sắp xếp trong các lớp và phân lớp năng lượng xung quanh hạt nhân của một nguyên tử. Ví dụ, cấu hình electron của Natri (Na) là 1s²2s²2p⁶3s¹.
2.1.1. Các Bước Xác Định Cấu Hình Electron
- Xác định số lượng electron: Số electron bằng số proton trong hạt nhân (số nguyên tử).
- Sử dụng quy tắc Aufbau: Các electron sẽ điền vào các orbital theo thứ tự năng lượng tăng dần (1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s,…).
- Tuân theo quy tắc Hund: Trong cùng một phân lớp, các electron sẽ phân bố sao cho số electron độc thân là tối đa.
2.1.2. Ví Dụ Minh Họa
Ví dụ, xét nguyên tố Oxy (O) có số nguyên tử là 8:
- Số lượng electron: 8
- Cấu hình electron: 1s²2s²2p⁴
- Số electron lớp ngoài cùng: 6 (2 trong 2s và 4 trong 2p)
2.2. Mối Liên Hệ Giữa Vị Trí Trong Bảng Tuần Hoàn Và Số Electron Lớp Ngoài Cùng
Vị trí của một nguyên tố trong bảng tuần hoàn cho biết số lượng electron lớp ngoài cùng của nó. Các nguyên tố trong cùng một nhóm (cột dọc) có cùng số electron lớp ngoài cùng và do đó có tính chất hóa học tương tự. Theo sách giáo khoa Hóa học lớp 10, các nguyên tố nhóm IA (kim loại kiềm) có 1 electron lớp ngoài cùng, nhóm IIA (kim loại kiềm thổ) có 2 electron lớp ngoài cùng, và cứ thế tiếp diễn.
| Nhóm trong bảng tuần hoàn | Số electron lớp ngoài cùng | Ví dụ |
|---|---|---|
| IA (Kim loại kiềm) | 1 | Natri (Na) |
| IIA (Kim loại kiềm thổ) | 2 | Magie (Mg) |
| IIIA | 3 | Nhôm (Al) |
| IVA | 4 | Cacbon (C) |
| VA | 5 | Nitơ (N) |
| VIA | 6 | Oxy (O) |
| VIIA (Halogen) | 7 | Clo (Cl) |
| VIIIA (Khí hiếm) | 8 (trừ Heli có 2) | Neon (Ne) |
2.3. Các Trường Hợp Đặc Biệt Cần Lưu Ý
Một số nguyên tố, đặc biệt là các kim loại chuyển tiếp, có cấu hình electron lớp ngoài cùng không tuân theo quy tắc chung. Ví dụ, Crom (Cr) có cấu hình electron là [Ar]3d⁵4s¹ thay vì [Ar]3d⁴4s². Điều này là do sự ổn định của cấu hình bán bão hòa (d⁵) và bão hòa (d¹⁰).
3. Ảnh Hưởng Của Electron Lớp Ngoài Cùng Đến Tính Chất Hóa Học
Số lượng electron lớp ngoài cùng quyết định khả năng hình thành liên kết hóa học và do đó ảnh hưởng đến tính chất hóa học của một nguyên tố.
3.1. Liên Kết Hóa Học Và Vai Trò Của Electron Lớp Ngoài Cùng
Electron lớp ngoài cùng tham gia vào ba loại liên kết hóa học chính: liên kết ion, liên kết cộng hóa trị và liên kết kim loại.
3.1.1. Liên Kết Ion
Liên kết ion hình thành khi một hoặc nhiều electron được chuyển từ một nguyên tử sang nguyên tử khác. Điều này thường xảy ra giữa kim loại (dễ mất electron) và phi kim (dễ nhận electron). Ví dụ, Natri (Na) có 1 electron lớp ngoài cùng dễ dàng nhường electron này cho Clo (Cl) có 7 electron lớp ngoài cùng, tạo thành liên kết ion trong muối ăn (NaCl).
3.1.2. Liên Kết Cộng Hóa Trị
Liên kết cộng hóa trị hình thành khi các nguyên tử chia sẻ electron để đạt được cấu hình electron bền vững. Điều này thường xảy ra giữa các phi kim. Ví dụ, hai nguyên tử Hydro (H) mỗi nguyên tử có 1 electron lớp ngoài cùng, chia sẻ electron để tạo thành phân tử Hydro (H₂).
3.1.3. Liên Kết Kim Loại
Liên kết kim loại hình thành giữa các nguyên tử kim loại, trong đó các electron lớp ngoài cùng di chuyển tự do trong mạng tinh thể kim loại. Điều này tạo ra tính dẫn điện và dẫn nhiệt tốt của kim loại.
3.2. Tính Chất Hóa Học Của Các Nhóm Nguyên Tố Chính
Số lượng electron lớp ngoài cùng quyết định tính chất hóa học đặc trưng của các nhóm nguyên tố.
- Kim loại kiềm (Nhóm IA): Dễ dàng mất 1 electron để tạo thành ion dương có điện tích +1, rất hoạt động hóa học.
- Kim loại kiềm thổ (Nhóm IIA): Dễ dàng mất 2 electron để tạo thành ion dương có điện tích +2, hoạt động hóa học kém hơn kim loại kiềm.
- Halogen (Nhóm VIIA): Dễ dàng nhận 1 electron để tạo thành ion âm có điện tích -1, rất hoạt động hóa học.
- Khí hiếm (Nhóm VIIIA): Có 8 electron lớp ngoài cùng (trừ Heli có 2), cấu hình electron bền vững, trơ về mặt hóa học.
3.3. Ảnh Hưởng Đến Tính Chất Vật Lý Của Vật Liệu
Electron lớp ngoài cùng không chỉ ảnh hưởng đến tính chất hóa học mà còn tác động đến tính chất vật lý của vật liệu, chẳng hạn như độ dẫn điện, độ cứng và điểm nóng chảy. Ví dụ, kim loại có electron lớp ngoài cùng di chuyển tự do có độ dẫn điện cao. Theo nghiên cứu của Viện Vật lý Kỹ thuật, Đại học Bách khoa Hà Nội năm 2022, vật liệu có cấu trúc electron lớp ngoài cùng đặc biệt có thể được sử dụng để chế tạo các thiết bị điện tử hiệu suất cao.
 Bảng tuần hoàn các nguyên tố hóa học
Bảng tuần hoàn các nguyên tố hóa học
Alt: Bảng tuần hoàn các nguyên tố hóa học với các nhóm nguyên tố được tô màu khác nhau, giúp dễ dàng nhận biết các nguyên tố có tính chất hóa học tương đồng.
4. Ứng Dụng Thực Tế Của Electron Lớp Ngoài Cùng
Hiểu biết về electron lớp ngoài cùng có nhiều ứng dụng trong các lĩnh vực khác nhau, từ công nghiệp xe tải đến sản xuất vật liệu mới và công nghệ điện tử.
4.1. Trong Công Nghiệp Sản Xuất Xe Tải
Trong công nghiệp sản xuất xe tải, việc lựa chọn vật liệu phù hợp là rất quan trọng để đảm bảo độ bền, độ an toàn và hiệu suất của xe. Electron lớp ngoài cùng đóng vai trò quan trọng trong việc xác định tính chất của vật liệu, từ đó giúp các nhà sản xuất lựa chọn vật liệu phù hợp cho từng bộ phận của xe tải.
4.1.1. Lựa Chọn Vật Liệu Chế Tạo Khung Xe
Khung xe tải cần có độ bền cao để chịu được tải trọng lớn và các tác động mạnh. Thép là vật liệu phổ biến được sử dụng để chế tạo khung xe tải vì nó có độ bền cao và khả năng chịu lực tốt. Tính chất này liên quan đến liên kết kim loại giữa các nguyên tử sắt (Fe) trong thép, trong đó các electron lớp ngoài cùng di chuyển tự do, tạo ra độ dẻo dai và khả năng chịu lực.
4.1.2. Chế Tạo Động Cơ Và Hệ Thống Truyền Động
Động cơ và hệ thống truyền động của xe tải cần có khả năng chịu nhiệt và chống ăn mòn tốt. Các hợp kim đặc biệt, chẳng hạn như hợp kim nhôm và hợp kim titan, được sử dụng để chế tạo các bộ phận này vì chúng có độ bền cao, trọng lượng nhẹ và khả năng chống ăn mòn tốt. Electron lớp ngoài cùng của các nguyên tố trong hợp kim này quyết định khả năng tạo thành lớp oxit bảo vệ, giúp chống lại quá trình ăn mòn.
4.1.3. Ứng Dụng Trong Hệ Thống Điện Tử Của Xe Tải
Xe tải hiện đại được trang bị nhiều hệ thống điện tử phức tạp, bao gồm hệ thống điều khiển động cơ, hệ thống phanh ABS, hệ thống định vị GPS và hệ thống giải trí. Các chất bán dẫn, chẳng hạn như silicon (Si) và germanium (Ge), được sử dụng để chế tạo các linh kiện điện tử này. Tính chất bán dẫn của chúng phụ thuộc vào cấu hình electron lớp ngoài cùng, cho phép chúng điều khiển dòng điện trong các điều kiện khác nhau.
4.2. Trong Nghiên Cứu Và Phát Triển Vật Liệu Mới
Hiểu biết về electron lớp ngoài cùng là rất quan trọng trong việc nghiên cứu và phát triển vật liệu mới với các tính chất đặc biệt.
4.2.1. Vật Liệu Siêu Dẫn
Vật liệu siêu dẫn có khả năng dẫn điện hoàn toàn không có điện trở ở nhiệt độ thấp. Nghiên cứu về electron lớp ngoài cùng và cấu trúc tinh thể của các vật liệu này đã giúp các nhà khoa học phát triển các vật liệu siêu dẫn mới với nhiệt độ chuyển pha cao hơn.
4.2.2. Vật Liệu Từ Tính
Vật liệu từ tính được sử dụng trong nhiều ứng dụng, bao gồm ổ cứng máy tính, động cơ điện và máy phát điện. Electron lớp ngoài cùng của các nguyên tố từ tính, chẳng hạn như sắt (Fe), coban (Co) và niken (Ni), quyết định tính chất từ của chúng.
4.2.3. Vật Liệu Quang Điện
Vật liệu quang điện có khả năng chuyển đổi ánh sáng thành điện năng và ngược lại. Chúng được sử dụng trong pin mặt trời, đèn LED và các thiết bị quang điện tử khác. Cấu hình electron lớp ngoài cùng của các nguyên tố trong vật liệu quang điện quyết định khả năng hấp thụ và phát xạ ánh sáng của chúng.
4.3. Trong Công Nghệ Điện Tử
Electron lớp ngoài cùng đóng vai trò then chốt trong công nghệ điện tử, đặc biệt là trong việc chế tạo các linh kiện bán dẫn.
4.3.1. Chất Bán Dẫn
Chất bán dẫn, như silicon (Si) và germanium (Ge), có độ dẫn điện nằm giữa kim loại và chất cách điện. Điều này cho phép chúng được sử dụng để điều khiển dòng điện trong các mạch điện tử. Tính chất bán dẫn của chúng phụ thuộc vào cấu hình electron lớp ngoài cùng và khả năng tạo ra các vùng dẫn điện dương (lỗ trống) và âm (electron).
4.3.2. Transistor
Transistor là linh kiện bán dẫn được sử dụng để khuếch đại hoặc chuyển mạch tín hiệu điện. Chúng là thành phần cơ bản của các mạch điện tử hiện đại. Hoạt động của transistor dựa trên việc điều khiển dòng điện giữa các cực của nó thông qua việc thay đổi điện áp ở cực điều khiển. Điều này được thực hiện bằng cách thay đổi số lượng electron hoặc lỗ trống trong vùng bán dẫn.
4.3.3. Vi Mạch
Vi mạch (IC) là tập hợp của hàng triệu hoặc thậm chí hàng tỷ transistor và các linh kiện điện tử khác được tích hợp trên một chip bán dẫn nhỏ. Chúng là trái tim của các thiết bị điện tử hiện đại, từ điện thoại thông minh đến máy tính và xe tải. Việc thiết kế và chế tạo vi mạch đòi hỏi sự hiểu biết sâu sắc về electron lớp ngoài cùng và tính chất của các vật liệu bán dẫn.
 Cấu hình electron của nguyên tử Natri (Na)
Cấu hình electron của nguyên tử Natri (Na)
Alt: Cấu hình electron của nguyên tử Natri (Na), minh họa cách electron được sắp xếp trong các lớp và phân lớp năng lượng.
5. Các Câu Hỏi Thường Gặp Về Electron Lớp Ngoài Cùng
5.1. Số Lượng Electron Lớp Ngoài Cùng Tối Đa Là Bao Nhiêu?
Số lượng electron lớp ngoài cùng tối đa là 8, ngoại trừ Heli (He) chỉ có 2.
5.2. Tại Sao Các Nguyên Tố Khí Hiếm Lại Bền Vững?
Các nguyên tố khí hiếm có 8 electron lớp ngoài cùng (trừ Heli có 2), tạo thành cấu hình electron bền vững, do đó chúng trơ về mặt hóa học.
5.3. Electron Lớp Ngoài Cùng Có Ảnh Hưởng Đến Màu Sắc Của Vật Liệu Không?
Có, electron lớp ngoài cùng có thể ảnh hưởng đến màu sắc của vật liệu bằng cách hấp thụ và phản xạ các bước sóng ánh sáng khác nhau.
5.4. Làm Thế Nào Để Thay Đổi Số Lượng Electron Lớp Ngoài Cùng?
Số lượng electron lớp ngoài cùng có thể thay đổi thông qua các phản ứng hóa học, trong đó các nguyên tử nhường hoặc nhận electron.
5.5. Electron Lớp Ngoài Cùng Có Liên Quan Đến Tính Axit-Bazơ Không?
Có, electron lớp ngoài cùng có liên quan đến tính axit-bazơ của các hợp chất, vì chúng tham gia vào việc hình thành và phá vỡ liên kết hóa học trong các phản ứng axit-bazơ.
5.6. Các Yếu Tố Nào Ảnh Hưởng Đến Năng Lượng Của Electron Lớp Ngoài Cùng?
Năng lượng của electron lớp ngoài cùng bị ảnh hưởng bởi điện tích hạt nhân, hiệu ứng chắn của các electron bên trong và sự tương tác giữa các electron.
5.7. Làm Thế Nào Để Dự Đoán Tính Chất Hóa Học Của Một Nguyên Tố Dựa Trên Số Electron Lớp Ngoài Cùng?
Bạn có thể dự đoán tính chất hóa học của một nguyên tố bằng cách xem xét số lượng electron lớp ngoài cùng và xu hướng của nó để đạt được cấu hình electron bền vững (8 electron lớp ngoài cùng).
5.8. Electron Lớp Ngoài Cùng Có Thể Bị Kích Thích Không?
Có, electron lớp ngoài cùng có thể bị kích thích khi chúng hấp thụ năng lượng (ví dụ: từ ánh sáng hoặc nhiệt), chuyển lên các mức năng lượng cao hơn.
5.9. Các Phương Pháp Nào Được Sử Dụng Để Nghiên Cứu Electron Lớp Ngoài Cùng?
Các phương pháp nghiên cứu electron lớp ngoài cùng bao gồm quang phổ hấp thụ, quang phổ phát xạ, nhiễu xạ electron và các phương pháp tính toán lượng tử.
5.10. Electron Lớp Ngoài Cùng Có Vai Trò Gì Trong Các Phản Ứng Hóa Học Hữu Cơ?
Electron lớp ngoài cùng đóng vai trò quan trọng trong các phản ứng hóa học hữu cơ, vì chúng tham gia vào việc hình thành và phá vỡ liên kết cộng hóa trị giữa các nguyên tử cacbon và các nguyên tử khác.
6. Kết Luận
Electron lớp ngoài cùng là chìa khóa để hiểu tính chất hóa học và vật lý của các nguyên tố và hợp chất. Từ việc lựa chọn vật liệu cho xe tải đến phát triển công nghệ điện tử tiên tiến, hiểu biết về electron lớp ngoài cùng có nhiều ứng dụng thực tế quan trọng. Tại XETAIMYDINH.EDU.VN, chúng tôi luôn nỗ lực cung cấp thông tin chi tiết và đáng tin cậy về các khía cạnh kỹ thuật liên quan đến xe tải, giúp bạn đưa ra những quyết định thông minh nhất.
Nếu bạn có bất kỳ thắc mắc nào về xe tải hoặc cần tư vấn về việc lựa chọn xe phù hợp, đừng ngần ngại liên hệ với chúng tôi. Đội ngũ chuyên gia của XETAIMYDINH.EDU.VN luôn sẵn sàng hỗ trợ bạn.
Liên hệ ngay với Xe Tải Mỹ Đình để được tư vấn và giải đáp mọi thắc mắc về xe tải:
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
Hãy để XETAIMYDINH.EDU.VN đồng hành cùng bạn trên mọi nẻo đường!

