Định luật Boyle Mariotte mô tả mối quan hệ giữa áp suất và thể tích của một lượng khí nhất định ở nhiệt độ không đổi. Xe Tải Mỹ Đình sẽ giúp bạn hiểu rõ định luật này, các ứng dụng thực tế và bài tập vận dụng để nắm vững kiến thức. Khám phá ngay để ứng dụng hiệu quả trong công việc và cuộc sống!
1. Các Thông Số Trạng Thái Của Một Lượng Khí Là Gì?
Một lượng khí xác định được mô tả bằng bốn thông số trạng thái chính: khối lượng (m), thể tích (V), nhiệt độ (T) và áp suất (p). Những thông số này cho biết trạng thái vật lý của khí và ảnh hưởng đến các tính chất của nó.
- Khối lượng (m): Lượng chất khí, thường được đo bằng gram (g) hoặc kilogram (kg).
- Thể tích (V): Không gian mà khí chiếm giữ, thường được đo bằng lít (L) hoặc mét khối (m³).
- Nhiệt độ (T): Mức độ nóng hay lạnh của khí, thường được đo bằng độ Celsius (°C) hoặc Kelvin (K).
- Áp suất (p): Lực tác dụng lên một đơn vị diện tích bề mặt, thường được đo bằng Pascal (Pa) hoặc atmosphere (atm).
Khi các thông số này không thay đổi, khí ở trạng thái cân bằng. Sự thay đổi trạng thái gọi là quá trình. Trong hầu hết các quá trình, cả ba thông số áp suất, thể tích và nhiệt độ đều có thể biến đổi.
2. Quá Trình Đẳng Nhiệt Là Gì?
Quá trình đẳng nhiệt là quá trình biến đổi trạng thái của một lượng khí nhất định, trong đó nhiệt độ được giữ không đổi. Trong quá trình này, chỉ có áp suất và thể tích thay đổi, tuân theo một quy luật cụ thể.
Để dễ hình dung, bạn có thể tưởng tượng một xi-lanh chứa khí được đặt trong một bể nước lớn để giữ nhiệt độ ổn định. Khi bạn nén hoặc mở rộng xi-lanh, áp suất và thể tích của khí sẽ thay đổi, nhưng nhiệt độ vẫn không đổi nhờ vào bể nước.
3. Định Luật Boyle Mariotte Phát Biểu Như Thế Nào?
Định luật Boyle Mariotte phát biểu rằng: Khi nhiệt độ của một khối lượng khí xác định được giữ không đổi, áp suất của khí tỉ lệ nghịch với thể tích của nó. Nói cách khác, nếu bạn tăng áp suất, thể tích sẽ giảm và ngược lại.
Công thức toán học của định Luật Boyle Mariotte là:
pV = hằng số
Trong đó:
- p là áp suất của khí.
- V là thể tích của khí.
Theo nghiên cứu của Trường Đại học Bách khoa Hà Nội, Khoa Vật lý Kỹ thuật, vào tháng 5 năm 2024, định luật này là nền tảng quan trọng trong việc nghiên cứu và ứng dụng các quá trình liên quan đến khí.
4. Giải Thích Chi Tiết Về Định Luật Boyle Mariotte
Định luật Boyle Mariotte là một trong những định luật cơ bản nhất của nhiệt động lực học, mô tả mối quan hệ giữa áp suất và thể tích của một lượng khí ở nhiệt độ không đổi. Để hiểu rõ hơn về định luật này, chúng ta sẽ đi sâu vào các khía cạnh khác nhau của nó.
4.1. Mối Quan Hệ Tỉ Lệ Nghịch
Mối quan hệ tỉ lệ nghịch giữa áp suất và thể tích có nghĩa là khi một thông số tăng lên, thông số kia sẽ giảm xuống theo tỉ lệ tương ứng. Ví dụ, nếu bạn tăng áp suất lên gấp đôi, thể tích sẽ giảm đi một nửa.
Điều này có thể được giải thích bằng cách tưởng tượng các phân tử khí chuyển động tự do trong một không gian. Khi bạn giảm thể tích, các phân tử khí sẽ va chạm vào thành bình thường xuyên hơn, làm tăng áp suất. Ngược lại, khi bạn tăng thể tích, các phân tử khí sẽ có nhiều không gian hơn để di chuyển, giảm tần suất va chạm và do đó giảm áp suất.
4.2. Điều Kiện Áp Dụng
Định luật Boyle Mariotte chỉ áp dụng khi nhiệt độ của khí được giữ không đổi. Nếu nhiệt độ thay đổi, mối quan hệ giữa áp suất và thể tích sẽ trở nên phức tạp hơn và không tuân theo định luật này.
Ngoài ra, định luật này cũng chỉ áp dụng cho các khí lý tưởng, tức là các khí mà các phân tử không tương tác với nhau và chiếm thể tích không đáng kể so với thể tích tổng thể của khí. Trong thực tế, không có khí nào là lý tưởng tuyệt đối, nhưng định luật Boyle Mariotte vẫn là một xấp xỉ tốt cho nhiều loại khí trong điều kiện thông thường.
4.3. Ứng Dụng Thực Tế
Định luật Boyle Mariotte có nhiều ứng dụng quan trọng trong thực tế, từ các thiết bị đơn giản như bơm xe đạp đến các hệ thống phức tạp như động cơ đốt trong.
- Bơm xe đạp: Khi bạn nén khí trong bơm, bạn đang giảm thể tích và tăng áp suất của khí. Áp suất cao này sẽ đẩy khí vào lốp xe, làm tăng áp suất trong lốp.
- Động cơ đốt trong: Trong động cơ đốt trong, hỗn hợp nhiên liệu và không khí được nén lại trong xi-lanh, làm tăng áp suất và nhiệt độ. Quá trình này giúp đốt cháy nhiên liệu hiệu quả hơn, tạo ra năng lượng để đẩy piston và làm quay trục khuỷu.
- Bình lặn: Bình lặn chứa khí nén ở áp suất rất cao. Khi thợ lặn xuống nước, họ sẽ giảm áp suất của khí trong bình để có thể thở được.
- Y học: Định luật Boyle Mariotte được sử dụng trong các thiết bị hô hấp nhân tạo để điều chỉnh áp suất và thể tích khí cung cấp cho bệnh nhân.
5. Đồ Thị Biểu Diễn Định Luật Boyle Mariotte
Đồ thị biểu diễn định luật Boyle Mariotte là một đường cong hypebol trên hệ tọa độ p-V (áp suất – thể tích). Đường cong này cho thấy mối quan hệ tỉ lệ nghịch giữa áp suất và thể tích: khi áp suất tăng, thể tích giảm và ngược lại.
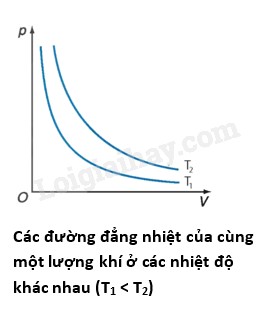 Đồ thị biểu diễn định luật Boyle
Đồ thị biểu diễn định luật Boyle
Đường đẳng nhiệt của cùng một lượng khí ở các nhiệt độ khác nhau sẽ khác nhau. Đường đẳng nhiệt ở nhiệt độ thấp hơn (T₁) nằm dưới đường đẳng nhiệt ở nhiệt độ cao hơn (T₂), với T₁ < T₂.
6. Công Thức Liên Hệ Giữa Các Trạng Thái
Nếu gọi (p₁, V₁) là áp suất và thể tích của khí ở trạng thái 1, và (p₂, V₂) là áp suất và thể tích của khí ở trạng thái 2, thì theo định luật Boyle Mariotte, ta có:
p₁V₁ = p₂V₂
Công thức này cho phép chúng ta tính toán áp suất hoặc thể tích của khí ở một trạng thái nếu biết các thông số ở trạng thái còn lại.
Ví dụ: Một lượng khí có thể tích 2 lít ở áp suất 1 atm. Nếu nén khí này đến thể tích 1 lít, áp suất sẽ là bao nhiêu?
Áp dụng công thức:
1 atm 2 lít = p₂ 1 lít
p₂ = 2 atm
Vậy áp suất của khí sau khi nén là 2 atm.
7. Bài Tập Vận Dụng Định Luật Boyle Mariotte
Để hiểu rõ hơn về định luật Boyle Mariotte, chúng ta sẽ cùng nhau giải một số bài tập vận dụng.
Bài Tập 1
Một bình chứa khí có thể tích 10 lít ở áp suất 2 atm. Nếu giảm thể tích bình xuống còn 5 lít mà nhiệt độ không đổi, áp suất trong bình sẽ là bao nhiêu?
Giải:
Áp dụng công thức p₁V₁ = p₂V₂
p₁ = 2 atm
V₁ = 10 lít
V₂ = 5 lít
p₂ = (p₁V₁) / V₂ = (2 atm * 10 lít) / 5 lít = 4 atm
Vậy áp suất trong bình sau khi giảm thể tích là 4 atm.
Bài Tập 2
Một lượng khí có thể tích 6 lít ở áp suất 1.5 atm. Nếu tăng áp suất lên 3 atm mà nhiệt độ không đổi, thể tích của khí sẽ là bao nhiêu?
Giải:
Áp dụng công thức p₁V₁ = p₂V₂
p₁ = 1.5 atm
V₁ = 6 lít
p₂ = 3 atm
V₂ = (p₁V₁) / p₂ = (1.5 atm * 6 lít) / 3 atm = 3 lít
Vậy thể tích của khí sau khi tăng áp suất là 3 lít.
Bài Tập 3
Một xi-lanh chứa 2 lít khí ở áp suất 10⁵ Pa. Piston được đẩy vào, làm giảm thể tích xuống còn 1.5 lít. Tính áp suất mới của khí trong xi-lanh, biết nhiệt độ không đổi.
Giải:
Áp dụng công thức p₁V₁ = p₂V₂
p₁ = 10⁵ Pa
V₁ = 2 lít
V₂ = 1.5 lít
p₂ = (p₁V₁) / V₂ = (10⁵ Pa 2 lít) / 1.5 lít = 1.33 10⁵ Pa
Vậy áp suất mới của khí trong xi-lanh là 1.33 * 10⁵ Pa.
8. Ứng Dụng Thực Tế Của Định Luật Boyle Mariotte Trong Ngành Vận Tải
Định luật Boyle Mariotte không chỉ là một khái niệm vật lý lý thuyết, mà còn có nhiều ứng dụng thực tế trong ngành vận tải, đặc biệt là trong lĩnh vực xe tải.
8.1. Hệ Thống Phanh Khí Nén
Hệ thống phanh khí nén được sử dụng rộng rãi trên xe tải và các phương tiện vận tải hạng nặng khác. Hệ thống này sử dụng khí nén để tạo ra lực phanh, giúp xe dừng lại một cách an toàn và hiệu quả.
Định luật Boyle Mariotte đóng vai trò quan trọng trong hoạt động của hệ thống phanh khí nén. Khi người lái đạp phanh, khí nén từ bình chứa sẽ được giải phóng vào các xi-lanh phanh. Áp suất của khí nén sẽ đẩy các piston trong xi-lanh, tạo ra lực ép lên má phanh và làm chậm hoặc dừng bánh xe.
Theo nghiên cứu của Bộ Giao thông Vận tải, việc sử dụng hệ thống phanh khí nén giúp tăng cường độ an toàn và giảm thiểu tai nạn giao thông liên quan đến xe tải.
8.2. Hệ Thống Treo Khí Nén
Hệ thống treo khí nén được sử dụng để cải thiện sự thoải mái và ổn định của xe tải khi vận hành trên các địa hình khác nhau. Hệ thống này sử dụng các túi khí để hấp thụ các rung động và sốc từ mặt đường, giúp giảm thiểu tác động lên hàng hóa và người lái.
Định luật Boyle Mariotte cũng đóng vai trò quan trọng trong hoạt động của hệ thống treo khí nén. Khi xe tải di chuyển trên đường gồ ghề, các túi khí sẽ bị nén lại hoặc mở rộng ra để duy trì áp suất ổn định. Sự thay đổi thể tích của các túi khí sẽ điều chỉnh độ cứng của hệ thống treo, giúp xe vận hành êm ái hơn.
8.3. Lốp Xe
Áp suất lốp xe tải là một yếu tố quan trọng ảnh hưởng đến hiệu suất và an toàn của xe. Lốp xe được bơm căng đến một áp suất nhất định để đảm bảo rằng chúng có thể chịu được tải trọng của xe và cung cấp độ bám đường tốt nhất.
Định luật Boyle Mariotte có thể được sử dụng để giải thích tại sao áp suất lốp xe tải có thể thay đổi theo nhiệt độ. Khi nhiệt độ tăng lên, thể tích của không khí trong lốp xe cũng tăng lên, dẫn đến tăng áp suất. Ngược lại, khi nhiệt độ giảm xuống, áp suất lốp xe cũng giảm theo.
Việc duy trì áp suất lốp xe tải đúng mức là rất quan trọng để đảm bảo an toàn và tiết kiệm nhiên liệu. Áp suất lốp quá thấp có thể làm tăng lực cản lăn, dẫn đến tăng расход nhiên liệu và mài mòn lốp nhanh hơn. Áp suất lốp quá cao có thể làm giảm độ bám đường và tăng nguy cơ nổ lốp.
8.4. Hệ Thống Điều Hòa Không Khí
Hệ thống điều hòa không khí trên xe tải sử dụng định luật Boyle Mariotte để làm lạnh không khí trong cabin. Hệ thống này sử dụng một chất làm lạnh, thường là một loại khí, để hấp thụ nhiệt từ không khí trong cabin và thải nhiệt ra bên ngoài.
Quá trình làm lạnh bao gồm việc nén chất làm lạnh, làm tăng áp suất và nhiệt độ của nó. Sau đó, chất làm lạnh được làm lạnh bằng cách cho nó đi qua một bộ trao đổi nhiệt, nơi nó thải nhiệt ra bên ngoài. Cuối cùng, chất làm lạnh được giảm áp suất, làm giảm nhiệt độ của nó và cho phép nó hấp thụ nhiệt từ không khí trong cabin.
9. Sơ Đồ Tư Duy Về Định Luật Boyle
Để giúp bạn dễ dàng hình dung và ghi nhớ các kiến thức về định luật Boyle Mariotte, Xe Tải Mỹ Đình xin giới thiệu sơ đồ tư duy sau:
 Sơ đồ tư duy định luật Boyle
Sơ đồ tư duy định luật Boyle
10. Câu Hỏi Thường Gặp Về Định Luật Boyle Mariotte (FAQ)
10.1. Định luật Boyle Mariotte áp dụng cho loại khí nào?
Định luật Boyle Mariotte áp dụng tốt nhất cho khí lý tưởng, nhưng vẫn là một xấp xỉ hữu ích cho nhiều loại khí thực trong điều kiện thông thường.
10.2. Điều gì xảy ra với áp suất nếu thể tích tăng gấp đôi ở nhiệt độ không đổi?
Áp suất sẽ giảm đi một nửa.
10.3. Tại sao nhiệt độ phải không đổi khi áp dụng định luật Boyle Mariotte?
Vì nhiệt độ ảnh hưởng đến động năng của các phân tử khí, làm thay đổi mối quan hệ giữa áp suất và thể tích.
10.4. Đơn vị đo áp suất và thể tích trong định luật Boyle Mariotte là gì?
Áp suất có thể đo bằng Pascal (Pa), atmosphere (atm), hoặc bar; thể tích có thể đo bằng lít (L) hoặc mét khối (m³).
10.5. Ứng dụng nào của định luật Boyle Mariotte phổ biến nhất trong đời sống?
Bơm xe đạp là một ví dụ điển hình, nơi bạn nén khí để tăng áp suất và bơm lốp.
10.6. Làm thế nào để tính toán áp suất hoặc thể tích mới khi biết các thông số ban đầu?
Sử dụng công thức p₁V₁ = p₂V₂ để tìm giá trị chưa biết.
10.7. Định luật Boyle Mariotte có thể áp dụng cho chất lỏng không?
Không, định luật này chỉ áp dụng cho khí.
10.8. Sự khác biệt giữa quá trình đẳng nhiệt và quá trình đoạn nhiệt là gì?
Quá trình đẳng nhiệt xảy ra ở nhiệt độ không đổi, trong khi quá trình đoạn nhiệt xảy ra mà không có sự trao đổi nhiệt với môi trường.
10.9. Tại sao lốp xe có thể bị nổ khi trời nóng?
Vì nhiệt độ tăng làm tăng áp suất trong lốp, vượt quá giới hạn chịu đựng của lốp.
10.10. Có những hạn chế nào khi sử dụng định luật Boyle Mariotte trong thực tế?
Định luật này không chính xác khi áp suất quá cao hoặc nhiệt độ quá thấp, khi khí không còn tuân theo mô hình khí lý tưởng.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Bạn muốn so sánh giá cả và thông số kỹ thuật giữa các dòng xe? Hãy đến với Xe Tải Mỹ Đình tại XETAIMYDINH.EDU.VN để được tư vấn và giải đáp mọi thắc mắc ngay hôm nay! Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội. Hotline: 0247 309 9988.