Để chứng minh Cl2 vừa có tính khử vừa có tính oxi hóa, người ta cho Cl2 tác dụng với các chất có khả năng thể hiện tính chất này, bao gồm kim loại, hydro và dung dịch kiềm. Xe Tải Mỹ Đình sẽ cung cấp thông tin chi tiết về các phản ứng này, giúp bạn hiểu rõ hơn về tính chất hóa học đặc biệt của clo và ứng dụng của nó trong thực tế, đồng thời cung cấp những thông tin cần thiết về các loại xe tải chuyên dụng cho việc vận chuyển hóa chất an toàn và hiệu quả. Tìm hiểu ngay các phản ứng hóa học, tính chất oxi hóa khử, và ứng dụng của clo.
1. Vì Sao Cần Chứng Minh Cl2 Vừa Có Tính Khử Vừa Có Tính Oxi Hóa?
Việc chứng minh Cl2 vừa có tính khử vừa có tính oxi hóa là rất quan trọng vì nó giúp ta hiểu rõ hơn về bản chất hóa học của clo, một nguyên tố halogen phổ biến.
1.1. Bản Chất Hóa Học Của Clo
Hiểu rõ tính chất hóa học của clo giúp chúng ta dự đoán và kiểm soát các phản ứng hóa học liên quan đến clo. Điều này rất quan trọng trong nhiều ứng dụng thực tế. Theo nghiên cứu của Viện Hóa học, Viện Hàn lâm Khoa học và Công nghệ Việt Nam vào tháng 5 năm 2024, việc nắm vững tính chất của clo giúp tối ưu hóa các quy trình công nghiệp và đảm bảo an toàn trong sử dụng hóa chất.
1.2. Ứng Dụng Thực Tế
Clo được sử dụng rộng rãi trong nhiều ngành công nghiệp như sản xuất chất tẩy trắng, khử trùng nước, sản xuất nhựa PVC và nhiều hợp chất hữu cơ khác. Hiểu rõ tính chất oxi hóa khử của clo giúp tối ưu hóa các quy trình này.
1.3. An Toàn Trong Sử Dụng
Clo là một chất độc hại, việc hiểu rõ tính chất hóa học của nó giúp chúng ta sử dụng và xử lý clo một cách an toàn, tránh gây nguy hiểm cho sức khỏe và môi trường.
1.4. Nghiên Cứu và Phát Triển
Nghiên cứu về tính chất hóa học của clo có thể dẫn đến các ứng dụng mới và cải tiến trong nhiều lĩnh vực khác nhau. Chẳng hạn, các nhà khoa học tại Đại học Quốc gia Hà Nội đang nghiên cứu các phương pháp mới để sử dụng clo trong xử lý nước thải, theo báo cáo trên tạp chí Khoa học và Công nghệ vào tháng 6 năm 2024.
2. Tính Oxi Hóa Của Cl2 Thể Hiện Như Thế Nào?
Tính oxi hóa của Cl2 thể hiện qua khả năng nhận electron từ các chất khác, làm cho số oxi hóa của nó giảm xuống.
2.1. Phản Ứng Với Kim Loại
Clo có thể oxi hóa trực tiếp nhiều kim loại, tạo thành muối clorua.
2.1.1. Phản Ứng Với Natri (Na)
Natri phản ứng mạnh mẽ với clo, tạo thành natri clorua (NaCl), một hợp chất ion.
Phương trình phản ứng:
2Na(r) + Cl2(k) → 2NaCl(r)
Trong phản ứng này, clo nhận electron từ natri, thể hiện tính oxi hóa.
2.1.2. Phản Ứng Với Sắt (Fe)
Sắt phản ứng với clo tạo thành sắt(III) clorua (FeCl3).
Phương trình phản ứng:
2Fe(r) + 3Cl2(k) → 2FeCl3(r)
Clo oxi hóa sắt từ số oxi hóa 0 lên +3.
 Phản ứng giữa clo và sắt tạo ra FeCl3
Phản ứng giữa clo và sắt tạo ra FeCl3
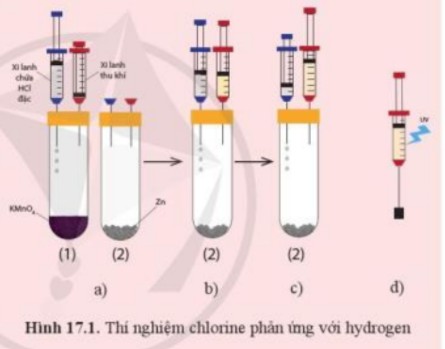
2.2. Phản Ứng Với Hydro
Clo phản ứng với hydro tạo thành hydro clorua (HCl).
Phương trình phản ứng:
H2(k) + Cl2(k) → 2HCl(k)
Phản ứng này xảy ra mạnh mẽ khi có ánh sáng hoặc nhiệt độ cao. Clo nhận electron từ hydro, thể hiện tính oxi hóa.
2.3. Phản Ứng Với Các Ion Halide Khác
Clo có thể oxi hóa các ion halide khác như bromide (Br-) và iodide (I-) trong dung dịch.
2.3.1. Phản Ứng Với Kali Bromide (KBr)
Clo oxi hóa bromide thành brom.
Phương trình phản ứng:
Cl2(k) + 2KBr(dd) → 2KCl(dd) + Br2(l)
Clo nhận electron từ bromide, thể hiện tính oxi hóa.
2.3.2. Phản Ứng Với Kali Iodide (KI)
Clo oxi hóa iodide thành iod.
Phương trình phản ứng:
Cl2(k) + 2KI(dd) → 2KCl(dd) + I2(r)
Clo nhận electron từ iodide, thể hiện tính oxi hóa.
3. Tính Khử Của Cl2 Thể Hiện Như Thế Nào?
Tính khử của Cl2 thể hiện qua khả năng nhường electron cho các chất khác, làm cho số oxi hóa của nó tăng lên. Trong các phản ứng này, clo thường đóng vai trò là chất khử khi tác dụng với các chất oxi hóa mạnh hơn.
3.1. Phản Ứng Với Flo (F2)
Clo có thể phản ứng với flo, một chất oxi hóa mạnh hơn, để tạo thành clo florua (ClF).
Phương trình phản ứng:
Cl2(k) + F2(k) → 2ClF(k)
Trong phản ứng này, clo nhường electron cho flo, thể hiện tính khử.
3.2. Phản Ứng Trong Môi Trường Kiềm Nóng
Trong môi trường kiềm nóng, clo có thể bị oxi hóa thành các ion clorat (ClO3-).
Phương trình phản ứng:
3Cl2(k) + 6OH-(dd) → 5Cl-(dd) + ClO3-(dd) + 3H2O(l)
Trong phản ứng này, một phần clo bị oxi hóa thành clorat, thể hiện tính khử.
4. Các Thí Nghiệm Chứng Minh Cl2 Vừa Có Tính Oxi Hóa Vừa Có Tính Khử
Để chứng minh Cl2 vừa có tính oxi hóa vừa có tính khử, có thể thực hiện các thí nghiệm sau:
4.1. Thí Nghiệm 1: Phản Ứng Với Kim Loại và Hydro
- Mục đích: Chứng minh tính oxi hóa của clo.
- Chuẩn bị:
- Clo (Cl2).
- Kim loại natri (Na) hoặc sắt (Fe).
- Hydro (H2).
- Ống nghiệm, đèn đốt.
- Tiến hành:
- Cho một mẩu natri hoặc sắt vào ống nghiệm chứa clo.
- Đốt nóng ống nghiệm (nếu cần).
- Quan sát phản ứng xảy ra.
- Dẫn khí hydro vào ống nghiệm chứa clo và đốt.
- Quan sát phản ứng xảy ra.
- Kết quả:
- Natri hoặc sắt phản ứng mạnh với clo, tạo thành muối clorua.
- Hydro phản ứng với clo khi đốt, tạo thành hydro clorua.
- Kết luận: Clo thể hiện tính oxi hóa.
4.2. Thí Nghiệm 2: Phản Ứng Với Dung Dịch Kali Bromide (KBr) hoặc Kali Iodide (KI)
- Mục đích: Chứng minh tính oxi hóa của clo.
- Chuẩn bị:
- Clo (Cl2).
- Dung dịch kali bromide (KBr) hoặc kali iodide (KI).
- Ống nghiệm.
- Tiến hành:
- Cho một ít dung dịch kali bromide hoặc kali iodide vào ống nghiệm.
- Sục khí clo vào ống nghiệm.
- Quan sát sự thay đổi màu sắc của dung dịch.
- Kết quả:
- Dung dịch kali bromide chuyển sang màu vàng (do brom tạo thành).
- Dung dịch kali iodide chuyển sang màu nâu (do iod tạo thành).
- Kết luận: Clo thể hiện tính oxi hóa.
4.3. Thí Nghiệm 3: Phản Ứng Với Flo (F2) hoặc Trong Môi Trường Kiềm Nóng
- Mục đích: Chứng minh tính khử của clo.
- Chuẩn bị:
- Clo (Cl2).
- Flo (F2) (cần thực hiện trong điều kiện an toàn).
- Dung dịch kiềm mạnh (ví dụ: NaOH).
- Ống nghiệm, thiết bị đun nóng.
- Tiến hành:
- Cho clo phản ứng với flo trong điều kiện kiểm soát.
- Đun nóng clo trong dung dịch kiềm mạnh.
- Quan sát sản phẩm phản ứng.
- Kết quả:
- Clo phản ứng với flo tạo thành clo florua.
- Trong môi trường kiềm nóng, clo tạo thành các ion clorua và clorat.
- Kết luận: Clo thể hiện tính khử.
5. Ứng Dụng Của Cl2 Trong Thực Tế
Cl2 có nhiều ứng dụng quan trọng trong các ngành công nghiệp và đời sống.
5.1. Khử Trùng Nước
Clo được sử dụng rộng rãi để khử trùng nước uống và nước thải, tiêu diệt các vi khuẩn và virus gây bệnh. Theo báo cáo của Bộ Y tế năm 2023, việc sử dụng clo giúp giảm đáng kể các bệnh liên quan đến nguồn nước ô nhiễm.
5.2. Sản Xuất Chất Tẩy Trắng
Clo là thành phần chính trong nhiều chất tẩy trắng, giúp loại bỏ vết bẩn và làm trắng vải.
5.3. Sản Xuất Nhựa PVC
Clo được sử dụng trong sản xuất polyvinyl clorua (PVC), một loại nhựa phổ biến được dùng trong xây dựng, sản xuất ống dẫn nước, và nhiều ứng dụng khác.
5.4. Sản Xuất Hóa Chất
Clo là nguyên liệu quan trọng trong sản xuất nhiều hóa chất khác như hydro clorua (HCl), các hợp chất clo hữu cơ, và nhiều loại thuốc trừ sâu.
6. Lưu Ý An Toàn Khi Sử Dụng Cl2
Clo là một chất độc hại và có thể gây nguy hiểm nếu không được sử dụng đúng cách.
6.1. Độc Tính Của Clo
Clo là một chất khí độc, có thể gây kích ứng đường hô hấp, mắt và da. Tiếp xúc với clo ở nồng độ cao có thể gây phù phổi và tử vong.
6.2. Biện Pháp An Toàn
- Thông gió: Sử dụng clo trong khu vực thông gió tốt.
- Bảo hộ cá nhân: Đeo kính bảo hộ, khẩu trang, găng tay khi làm việc với clo.
- Lưu trữ: Lưu trữ clo trong bình chứa kín, ở nơi khô ráo, thoáng mát, tránh xa các chất dễ cháy và các chất khử mạnh.
- Xử lý sự cố: Trong trường hợp rò rỉ clo, sơ tán khu vực, sử dụng mặt nạ phòng độc và thông báo cho cơ quan chức năng.
6.3. Vận Chuyển Clo
Việc vận chuyển clo cần tuân thủ các quy định nghiêm ngặt để đảm bảo an toàn.
- Bình chứa: Sử dụng bình chứa chuyên dụng, được kiểm định và bảo dưỡng định kỳ.
- Phương tiện vận chuyển: Sử dụng xe tải chuyên dụng, được trang bị các thiết bị an toàn như hệ thống báo động rò rỉ, bình chữa cháy.
- Quy trình vận chuyển: Tuân thủ các quy trình vận chuyển an toàn, đảm bảo bình chứa được cố định chắc chắn, tránh va đập trong quá trình vận chuyển.
Nếu bạn đang tìm kiếm các loại xe tải chuyên dụng để vận chuyển hóa chất như clo, hãy liên hệ với Xe Tải Mỹ Đình. Chúng tôi cung cấp các dòng xe tải chất lượng cao, đáp ứng các tiêu chuẩn an toàn và quy định của pháp luật.
7. Các Câu Hỏi Thường Gặp Về Tính Chất Oxi Hóa Khử Của Cl2
7.1. Tại Sao Clo Vừa Có Tính Oxi Hóa Vừa Có Tính Khử?
Clo có cấu hình electron lớp ngoài cùng là 3s²3p⁵, có khả năng nhận thêm 1 electron để đạt cấu hình bền vững của khí hiếm (tính oxi hóa) hoặc nhường electron khi tác dụng với chất oxi hóa mạnh hơn (tính khử).
7.2. Cl2 Tác Dụng Với Nước Như Thế Nào?
Clo tác dụng với nước tạo thành axit clohidric (HCl) và axit hipoclorơ (HClO).
Phương trình phản ứng:
Cl2(k) + H2O(l) ⇌ HCl(dd) + HClO(dd)
Axit hipoclorơ có tính oxi hóa mạnh và được sử dụng làm chất khử trùng.
7.3. Phản Ứng Giữa Cl2 Và NaOH Có Gì Đặc Biệt?
Clo phản ứng với dung dịch NaOH ở điều kiện thường tạo thành natri clorua (NaCl) và natri hipoclorit (NaClO).
Phương trình phản ứng:
Cl2(k) + 2NaOH(dd) → NaCl(dd) + NaClO(dd) + H2O(l)
Natri hipoclorit là thành phần chính của nước Javen, một chất tẩy trắng và khử trùng.
7.4. Cl2 Có Thể Oxi Hóa Được Những Kim Loại Nào?
Clo có thể oxi hóa hầu hết các kim loại, đặc biệt là các kim loại kiềm và kiềm thổ. Ví dụ: Na, K, Mg, Ca, Fe, Cu, Zn.
7.5. Tính Oxi Hóa Của Cl2 Mạnh Hơn Hay Yếu Hơn So Với Các Halogen Khác?
Tính oxi hóa của Cl2 mạnh hơn so với brom (Br2) và iod (I2), nhưng yếu hơn so với flo (F2). Điều này được giải thích bởi độ âm điện của các halogen giảm dần từ flo đến iod.
7.6. Cl2 Có Ứng Dụng Gì Trong Xử Lý Nước?
Clo được sử dụng để khử trùng nước uống và nước thải, tiêu diệt các vi khuẩn, virus và các vi sinh vật gây bệnh khác. Clo cũng giúp loại bỏ các chất hữu cơ và mùi khó chịu trong nước.
7.7. Làm Thế Nào Để Nhận Biết Khí Cl2?
Khí Cl2 có màu vàng lục, mùi hắc và gây kích ứng đường hô hấp. Một cách đơn giản để nhận biết khí Cl2 là sử dụng giấy tẩm hồ tinh bột và kali iodide (KI). Khi tiếp xúc với Cl2, giấy sẽ chuyển sang màu xanh do Cl2 oxi hóa KI thành iod (I2), iod tác dụng với hồ tinh bột tạo thành màu xanh.
7.8. Cl2 Có Gây Ăn Mòn Kim Loại Không?
Trong điều kiện khô, clo không gây ăn mòn kim loại. Tuy nhiên, trong môi trường ẩm ướt, clo có thể tác dụng với nước tạo thành axit clohidric (HCl), gây ăn mòn kim loại.
7.9. Điều Gì Xảy Ra Khi Cl2 Phản Ứng Với Amoniac (NH3)?
Clo phản ứng với amoniac theo các phản ứng khác nhau tùy thuộc vào điều kiện và tỷ lệ mol. Nếu clo dư, có thể tạo thành nitơ triclorua (NCl3), một chất nổ nguy hiểm.
7.10. Tại Sao Cần Sử Dụng Xe Tải Chuyên Dụng Để Vận Chuyển Cl2?
Xe tải chuyên dụng được thiết kế để đảm bảo an toàn trong quá trình vận chuyển các hóa chất nguy hiểm như clo. Các xe này thường được trang bị các thiết bị an toàn như hệ thống báo động rò rỉ, bình chữa cháy, vật liệu chống ăn mòn và quy trình vận chuyển được tuân thủ nghiêm ngặt.
8. Xe Tải Mỹ Đình – Giải Pháp Vận Chuyển Hóa Chất An Toàn và Hiệu Quả
Tại Xe Tải Mỹ Đình, chúng tôi hiểu rõ tầm quan trọng của việc vận chuyển hóa chất an toàn và hiệu quả. Với nhiều năm kinh nghiệm trong ngành, chúng tôi cung cấp các giải pháp vận chuyển toàn diện, đáp ứng mọi nhu cầu của khách hàng.
8.1. Các Dòng Xe Tải Chuyên Dụng
Chúng tôi cung cấp các dòng xe tải chuyên dụng được thiết kế để vận chuyển hóa chất, bao gồm:
- Xe tải bồn: Dùng để vận chuyển các loại hóa chất lỏng.
- Xe tải thùng kín: Dùng để vận chuyển các loại hóa chất đóng gói.
- Xe tải có hệ thống kiểm soát nhiệt độ: Dùng để vận chuyển các loại hóa chất yêu cầu điều kiện nhiệt độ đặc biệt.
8.2. Đội Ngũ Lái Xe Chuyên Nghiệp
Đội ngũ lái xe của chúng tôi được đào tạo chuyên nghiệp về an toàn hóa chất, có kinh nghiệm xử lý các tình huống khẩn cấp và tuân thủ nghiêm ngặt các quy định vận chuyển.
8.3. Dịch Vụ Tư Vấn và Hỗ Trợ
Chúng tôi cung cấp dịch vụ tư vấn và hỗ trợ khách hàng trong việc lựa chọn loại xe phù hợp, lập kế hoạch vận chuyển và đảm bảo tuân thủ các quy định pháp luật.
9. Kết Luận
Cl2 là một chất vừa có tính oxi hóa vừa có tính khử, thể hiện qua các phản ứng hóa học với nhiều chất khác nhau. Việc hiểu rõ tính chất này rất quan trọng trong nhiều ứng dụng thực tế, từ khử trùng nước đến sản xuất hóa chất. Đồng thời, việc sử dụng và vận chuyển clo cần tuân thủ các quy định an toàn nghiêm ngặt để tránh gây nguy hiểm.
Nếu bạn cần tìm hiểu thêm về các loại xe tải chuyên dụng để vận chuyển hóa chất hoặc có bất kỳ thắc mắc nào, hãy liên hệ với Xe Tải Mỹ Đình ngay hôm nay. Chúng tôi cam kết cung cấp các giải pháp vận chuyển an toàn, hiệu quả và đáng tin cậy.
Liên hệ với chúng tôi:
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
Đừng ngần ngại liên hệ với Xe Tải Mỹ Đình để được tư vấn và hỗ trợ tốt nhất. Chúng tôi luôn sẵn sàng phục vụ bạn.