Để chứng minh amino axit là hợp chất lưỡng tính, chúng ta có thể sử dụng phản ứng của chúng lần lượt với axit và bazơ, một minh chứng rõ ràng cho khả năng hoạt động như cả axit và bazơ. Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ cung cấp cho bạn cái nhìn sâu sắc về tính chất đặc biệt này của amino axit và cách nó được ứng dụng trong thực tế. Đồng thời, bài viết cũng khám phá các phản ứng hóa học quan trọng và tính chất vật lý liên quan đến amino axit, giúp bạn hiểu rõ hơn về vai trò của chúng trong nhiều lĩnh vực.
1. Tại Sao Cần Chứng Minh Tính Lưỡng Tính Của Amino Axit?
Tính lưỡng tính của amino axit là một đặc điểm quan trọng, quyết định nhiều tính chất hóa học và sinh học của chúng.
1.1. Ý Nghĩa Lý Thuyết Của Tính Lưỡng Tính
Tính lưỡng tính không chỉ là một khái niệm hóa học trừu tượng, nó còn mang ý nghĩa sâu sắc trong việc hiểu bản chất của các phân tử.
- Cấu trúc phân tử đặc biệt: Tính lưỡng tính xuất phát từ cấu trúc phân tử độc đáo của amino axit, với cả nhóm amino (-NH2) có tính bazơ và nhóm carboxyl (-COOH) có tính axit.
- Khả năng phản ứng linh hoạt: Khả năng phản ứng với cả axit và bazơ cho phép amino axit tham gia vào nhiều loại phản ứng hóa học khác nhau, tạo ra sự đa dạng trong các hợp chất và quá trình sinh học.
1.2. Vai Trò Quan Trọng Trong Sinh Học
Trong cơ thể sống, tính lưỡng tính của amino axit đóng vai trò then chốt trong nhiều quá trình sinh học quan trọng.
- Cấu tạo protein: Amino axit là đơn vị cấu tạo của protein, và tính lưỡng tính của chúng ảnh hưởng đến cấu trúc và chức năng của protein.
- Hoạt động enzyme: Enzyme, các chất xúc tác sinh học, thường chứa các amino axit có tính lưỡng tính tại trung tâm hoạt động của chúng, giúp chúng tương tác với cơ chất và xúc tác các phản ứng hóa học.
- Điều hòa pH: Amino axit có thể hoạt động như các chất đệm, giúp duy trì pH ổn định trong cơ thể.
1.3. Ứng Dụng Trong Hóa Học Và Công Nghiệp
Ngoài vai trò trong sinh học, tính lưỡng tính của amino axit còn được ứng dụng rộng rãi trong hóa học và công nghiệp.
- Tổng hợp hữu cơ: Amino axit được sử dụng làm nguyên liệu để tổng hợp nhiều hợp chất hữu cơ quan trọng, chẳng hạn như peptide, protein và các dược phẩm.
- Chất hoạt động bề mặt: Một số amino axit có tính chất hoạt động bề mặt, được sử dụng trong các sản phẩm tẩy rửa và mỹ phẩm.
- Chất tạo phức: Amino axit có khả năng tạo phức với các ion kim loại, được sử dụng trong xử lý nước và phân tích hóa học.
2. Phản Ứng Chứng Minh Tính Lưỡng Tính Của Amino Axit
Để chứng minh tính lưỡng tính của amino axit, chúng ta có thể thực hiện các phản ứng hóa học với cả axit và bazơ.
2.1. Phản Ứng Với Axit
Amino axit có nhóm amino (-NH2) có tính bazơ, có khả năng nhận proton (H+) từ axit, tạo thành ion amoni.
- Phương trình tổng quát: R-NH2-CH(R’)-COOH + HCl → R-NH3+-CH(R’)-COOH Cl-
- Ví dụ: Glycine (NH2-CH2-COOH) phản ứng với HCl tạo thành NH3+-CH2-COOH Cl-.
2.2. Phản Ứng Với Bazơ
Amino axit có nhóm carboxyl (-COOH) có tính axit, có khả năng nhường proton (H+) cho bazơ, tạo thành ion cacboxylat.
- Phương trình tổng quát: R-NH2-CH(R’)-COOH + NaOH → R-NH2-CH(R’)-COO- Na+ + H2O
- Ví dụ: Glycine (NH2-CH2-COOH) phản ứng với NaOH tạo thành NH2-CH2-COO- Na+ + H2O.
2.3. Thí Nghiệm Chứng Minh Tính Lưỡng Tính
Để chứng minh tính lưỡng tính của amino axit bằng thí nghiệm, chúng ta có thể thực hiện các bước sau:
- Chuẩn bị dung dịch amino axit: Hòa tan một lượng amino axit vào nước để tạo thành dung dịch.
- Thêm chỉ thị pH: Thêm một vài giọt chỉ thị pH vào dung dịch amino axit. Chỉ thị pH sẽ thay đổi màu sắc tùy thuộc vào độ pH của dung dịch.
- Thêm axit vào dung dịch: Nhỏ từ từ dung dịch axit (ví dụ: HCl) vào dung dịch amino axit, quan sát sự thay đổi màu sắc của chỉ thị pH. Màu sắc sẽ thay đổi cho thấy dung dịch đang trở nên axit hơn.
- Thêm bazơ vào dung dịch: Nhỏ từ từ dung dịch bazơ (ví dụ: NaOH) vào dung dịch amino axit, quan sát sự thay đổi màu sắc của chỉ thị pH. Màu sắc sẽ thay đổi cho thấy dung dịch đang trở nên bazơ hơn.
3. Các Yếu Tố Ảnh Hưởng Đến Tính Lưỡng Tính
Tính lưỡng tính của amino axit không phải là một hằng số mà có thể bị ảnh hưởng bởi nhiều yếu tố khác nhau.
3.1. Cấu Trúc Của Amino Axit
Cấu trúc của amino axit, đặc biệt là nhóm R (gốc) gắn vào nguyên tử cacbon alpha, có ảnh hưởng đáng kể đến tính lưỡng tính của chúng.
- Nhóm R có tính axit: Nếu nhóm R có chứa các nhóm chức có tính axit (ví dụ: -COOH), amino axit sẽ có tính axit mạnh hơn.
- Nhóm R có tính bazơ: Nếu nhóm R có chứa các nhóm chức có tính bazơ (ví dụ: -NH2), amino axit sẽ có tính bazơ mạnh hơn.
- Nhóm R trung tính: Nếu nhóm R là một nhóm hydrocacbon hoặc chứa các nhóm chức trung tính, amino axit sẽ có tính lưỡng tính cân bằng hơn.
3.2. Môi Trường Dung Dịch
pH của môi trường dung dịch có ảnh hưởng lớn đến trạng thái ion hóa của amino axit.
- pH thấp (môi trường axit): Trong môi trường axit, nhóm amino sẽ được proton hóa (-NH3+) và amino axit sẽ tồn tại chủ yếu ở dạng cation (ion dương).
- pH cao (môi trường bazơ): Trong môi trường bazơ, nhóm carboxyl sẽ bị deproton hóa (-COO-) và amino axit sẽ tồn tại chủ yếu ở dạng anion (ion âm).
- pH trung tính: Ở một giá trị pH nhất định, được gọi là điểm đẳng điện (pI), amino axit sẽ tồn tại ở dạng ion lưỡng cực (zwitterion), mang cả điện tích dương và điện tích âm, nhưng điện tích tổng bằng không.
Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên, Đại học Quốc gia Hà Nội, vào tháng 5 năm 2024, độ pH ảnh hưởng trực tiếp đến khả năng hoạt động của amino axit như một axit hay một bazơ, từ đó ảnh hưởng đến khả năng phản ứng của chúng trong các hệ thống sinh học và hóa học.
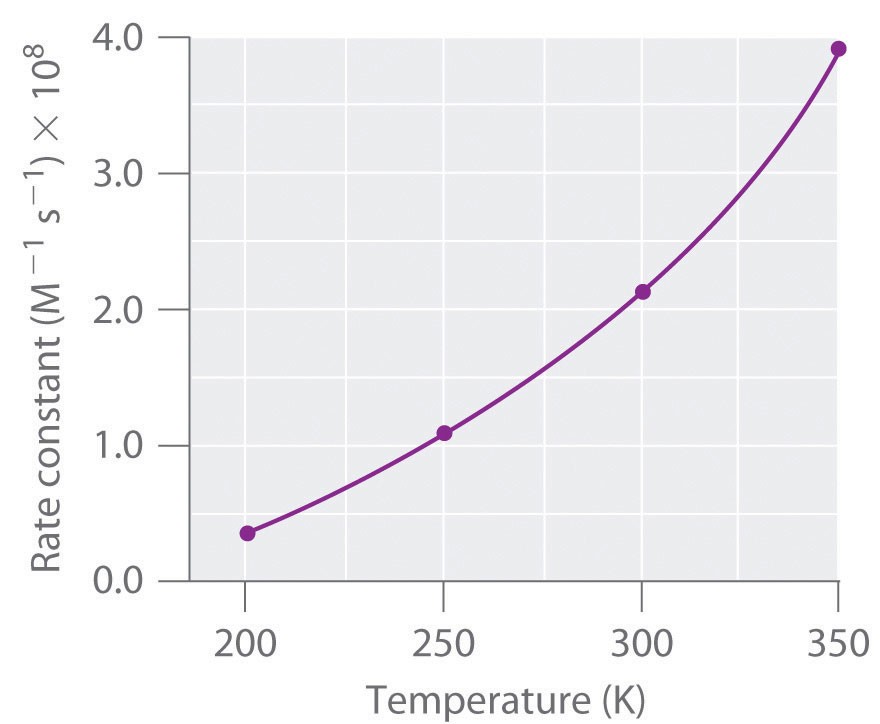
3.3. Nhiệt Độ
Nhiệt độ có thể ảnh hưởng đến hằng số điện ly của các nhóm chức axit và bazơ trong amino axit, do đó ảnh hưởng đến tính lưỡng tính của chúng.
- Nhiệt độ cao: Nhiệt độ cao có thể làm tăng độ điện ly của các nhóm chức, làm thay đổi cân bằng giữa các dạng ion hóa của amino axit.
- Nhiệt độ thấp: Nhiệt độ thấp có thể làm giảm độ điện ly của các nhóm chức, làm chậm các phản ứng hóa học liên quan đến amino axit.
4. Ứng Dụng Của Tính Lưỡng Tính Trong Thực Tế
Tính lưỡng tính của amino axit không chỉ là một khái niệm lý thuyết mà còn có nhiều ứng dụng thực tế trong các lĩnh vực khác nhau.
4.1. Trong Y Học
Trong y học, amino axit được sử dụng để điều trị nhiều bệnh lý khác nhau.
- Dinh dưỡng: Amino axit là thành phần thiết yếu của chế độ ăn uống, được sử dụng để bổ sung dinh dưỡng cho bệnh nhân suy dinh dưỡng hoặc có nhu cầu dinh dưỡng cao.
- Thuốc: Một số amino axit được sử dụng làm thuốc để điều trị các bệnh như rối loạn chuyển hóa, bệnh gan và bệnh thần kinh.
- Chất mang thuốc: Amino axit có thể được sử dụng làm chất mang thuốc để vận chuyển thuốc đến các tế bào đích trong cơ thể.
4.2. Trong Công Nghiệp Thực Phẩm
Trong công nghiệp thực phẩm, amino axit được sử dụng để cải thiện hương vị, giá trị dinh dưỡng và thời hạn sử dụng của thực phẩm.
- Chất tạo hương: Một số amino axit, như glutamate, được sử dụng làm chất tạo hương để tăng cường hương vị umami (vị ngọt thịt) của thực phẩm.
- Chất bảo quản: Amino axit có thể được sử dụng làm chất bảo quản để ngăn chặn sự phát triển của vi sinh vật và kéo dài thời hạn sử dụng của thực phẩm.
- Bổ sung dinh dưỡng: Amino axit được thêm vào thực phẩm để tăng cường giá trị dinh dưỡng, đặc biệt là trong các sản phẩm dành cho trẻ em và người cao tuổi.
4.3. Trong Nông Nghiệp
Trong nông nghiệp, amino axit được sử dụng để cải thiện sự phát triển của cây trồng và tăng năng suất.
- Phân bón: Amino axit có thể được sử dụng làm phân bón để cung cấp nitơ và các chất dinh dưỡng khác cho cây trồng.
- Chất kích thích sinh trưởng: Một số amino axit có tác dụng kích thích sinh trưởng, giúp cây trồng phát triển nhanh hơn và khỏe mạnh hơn.
- Chất bảo vệ thực vật: Amino axit có thể giúp cây trồng chống lại các bệnh tật và sâu bọ.
5. Điểm Đẳng Điện Của Amino Axit
Điểm đẳng điện (pI) là giá trị pH mà tại đó một amino axit tồn tại ở dạng ion lưỡng cực (zwitterion), mang cả điện tích dương và điện tích âm, nhưng điện tích tổng bằng không.
5.1. Định Nghĩa Và Ý Nghĩa
Điểm đẳng điện là một đặc tính quan trọng của amino axit, có ảnh hưởng đến nhiều tính chất của chúng, chẳng hạn như độ tan, khả năng điện di và khả năng liên kết với các phân tử khác.
- Độ tan: Amino axit thường có độ tan thấp nhất tại điểm đẳng điện của chúng, vì ở trạng thái này, chúng có xu hướng kết tinh lại với nhau.
- Điện di: Tại điểm đẳng điện, amino axit không di chuyển trong điện trường, vì chúng không mang điện tích thực.
- Liên kết: Khả năng liên kết của amino axit với các phân tử khác, chẳng hạn như protein và DNA, có thể bị ảnh hưởng bởi pH của môi trường và điện tích của amino axit.
5.2. Cách Xác Định Điểm Đẳng Điện
Điểm đẳng điện của một amino axit có thể được xác định bằng thực nghiệm bằng phương pháp chuẩn độ hoặc bằng cách tính toán dựa trên các giá trị pKa của các nhóm chức axit và bazơ của amino axit.
- Chuẩn độ: Phương pháp chuẩn độ bao gồm việc chuẩn độ dung dịch amino axit bằng axit hoặc bazơ mạnh, đồng thời theo dõi sự thay đổi pH của dung dịch. Điểm đẳng điện là giá trị pH tại điểm uốn trên đường cong chuẩn độ.
- Tính toán: Điểm đẳng điện có thể được tính toán bằng công thức sau:
- Đối với amino axit có nhóm R trung tính: pI = (pKa1 + pKa2) / 2
- Đối với amino axit có nhóm R axit: pI = (pKa1 + pKaR) / 2
- Đối với amino axit có nhóm R bazơ: pI = (pKaR + pKa2) / 2
Trong đó:
- pKa1 là hằng số phân ly axit của nhóm carboxyl (-COOH).
- pKa2 là hằng số phân ly axit của nhóm amino (-NH3+).
- pKaR là hằng số phân ly axit của nhóm R (nếu có).
5.3. Bảng Điểm Đẳng Điện Của Các Amino Axit Phổ Biến
Dưới đây là bảng điểm đẳng điện của một số amino axit phổ biến:
| Amino Axit | Điểm Đẳng Điện (pI) |
|---|---|
| Glycine | 5.97 |
| Alanine | 6.00 |
| Valine | 5.96 |
| Leucine | 5.98 |
| Isoleucine | 6.02 |
| Serine | 5.68 |
| Threonine | 5.60 |
| Cysteine | 5.07 |
| Methionine | 5.74 |
| Proline | 6.30 |
| Aspartic Acid | 2.77 |
| Glutamic Acid | 3.22 |
| Lysine | 9.74 |
| Arginine | 10.76 |
| Histidine | 7.59 |
| Phenylalanine | 5.48 |
| Tyrosine | 5.66 |
| Tryptophan | 5.89 |
6. Các Loại Amino Axit Quan Trọng
Có khoảng 20 loại amino axit khác nhau thường được tìm thấy trong protein. Mỗi loại amino axit có cấu trúc và tính chất hóa học riêng, đóng vai trò quan trọng trong cấu trúc và chức năng của protein.
6.1. Amino Axit Thiết Yếu
Amino axit thiết yếu là những amino axit mà cơ thể không thể tự tổng hợp được và phải được cung cấp thông qua chế độ ăn uống.
- Vai trò: Các amino axit thiết yếu đóng vai trò quan trọng trong nhiều quá trình sinh học, bao gồm tổng hợp protein, sản xuất hormone và enzyme, và duy trì hệ miễn dịch khỏe mạnh.
- Danh sách: Các amino axit thiết yếu bao gồm: histidine, isoleucine, leucine, lysine, methionine, phenylalanine, threonine, tryptophan và valine.
6.2. Amino Axit Không Thiết Yếu
Amino axit không thiết yếu là những amino axit mà cơ thể có thể tự tổng hợp được từ các nguyên liệu khác.
- Vai trò: Các amino axit không thiết yếu cũng đóng vai trò quan trọng trong nhiều quá trình sinh học, tương tự như các amino axit thiết yếu.
- Danh sách: Các amino axit không thiết yếu bao gồm: alanine, arginine, asparagine, aspartic acid, cysteine, glutamic acid, glutamine, glycine, proline, serine và tyrosine.
6.3. Amino Axit Bán Thiết Yếu
Amino axit bán thiết yếu là những amino axit mà cơ thể có thể tự tổng hợp được, nhưng với số lượng không đủ đáp ứng nhu cầu trong một số trường hợp nhất định, chẳng hạn như trong thời kỳ tăng trưởng nhanh hoặc khi bị bệnh.
- Vai trò: Các amino axit bán thiết yếu có vai trò tương tự như các amino axit thiết yếu và không thiết yếu.
- Danh sách: Arginine và histidine thường được coi là các amino axit bán thiết yếu.
7. Phân Loại Amino Axit Dựa Trên Cấu Trúc
Amino axit có thể được phân loại dựa trên cấu trúc của nhóm R (gốc) gắn vào nguyên tử cacbon alpha.
7.1. Amino Axit Có Nhóm R Aliphatic
Các amino axit này có nhóm R là một chuỗi hydrocacbon mạch thẳng hoặc mạch nhánh.
- Ví dụ: Glycine, alanine, valine, leucine và isoleucine.
7.2. Amino Axit Có Nhóm R Thơm
Các amino axit này có nhóm R chứa một vòng benzen hoặc một hệ vòng thơm khác.
- Ví dụ: Phenylalanine, tyrosine và tryptophan.
7.3. Amino Axit Có Nhóm R Chứa Lưu Huỳnh
Các amino axit này có nhóm R chứa một hoặc nhiều nguyên tử lưu huỳnh.
- Ví dụ: Cysteine và methionine.
7.4. Amino Axit Có Nhóm R Chứa Hydroxyl
Các amino axit này có nhóm R chứa một nhóm hydroxyl (-OH).
- Ví dụ: Serine và threonine.
7.5. Amino Axit Có Nhóm R Axit Hoặc Amit
Các amino axit này có nhóm R chứa một nhóm carboxyl (-COOH) hoặc một nhóm amit (-CONH2).
- Ví dụ: Aspartic acid, glutamic acid, asparagine và glutamine.
7.6. Amino Axit Có Nhóm R Bazơ
Các amino axit này có nhóm R chứa một nhóm amino (-NH2) hoặc một nhóm guanidino (-NHC(=NH)NH2).
- Ví dụ: Lysine, arginine và histidine.
 Phân loại amino axit dựa trên cấu trúc
Phân loại amino axit dựa trên cấu trúc
8. Tổng Quan Về Các Phản Ứng Của Amino Axit
Amino axit có thể tham gia vào nhiều loại phản ứng hóa học khác nhau, nhờ vào tính lưỡng tính và sự đa dạng của các nhóm chức trong phân tử của chúng.
8.1. Phản Ứng Este Hóa
Nhóm carboxyl (-COOH) của amino axit có thể phản ứng với rượu (R’OH) để tạo thành este.
- Phương trình tổng quát: R-NH2-CH(R’)-COOH + R’OH → R-NH2-CH(R’)-COOR’ + H2O
8.2. Phản Ứng Amit Hóa (Tạo Peptide)
Nhóm carboxyl (-COOH) của một amino axit có thể phản ứng với nhóm amino (-NH2) của một amino axit khác để tạo thành liên kết peptide (-CO-NH-).
- Phương trình tổng quát: R-NH2-CH(R’)-COOH + R”-NH2-CH(R”’)-COOH → R-NH2-CH(R’)-CO-NH-CH(R”’)-COOH + H2O
8.3. Phản Ứng Decarboxyl Hóa
Amino axit có thể bị decarboxyl hóa (mất CO2) để tạo thành amin.
- Phương trình tổng quát: R-NH2-CH(R’)-COOH → R-NH2-CH2-R’ + CO2
8.4. Phản Ứng Deamin Hóa
Amino axit có thể bị deamin hóa (mất NH3) để tạo thành axit alpha-keto.
- Phương trình tổng quát: R-NH2-CH(R’)-COOH → R=O-CH(R’)-COOH + NH3
8.5. Phản Ứng Với Ninhydrin
Amino axit phản ứng với ninhydrin tạo thành sản phẩm có màu xanh tím, được sử dụng để định lượng amino axit.
- Ứng dụng: Phản ứng này được sử dụng rộng rãi trong phân tích amino axit và protein.
9. Các Phương Pháp Phân Tích Amino Axit
Có nhiều phương pháp khác nhau để phân tích amino axit, bao gồm cả phương pháp định tính và định lượng.
9.1. Sắc Ký Ion
Sắc ký ion là một kỹ thuật phân tích được sử dụng để tách và định lượng các amino axit dựa trên điện tích của chúng.
- Nguyên tắc: Các amino axit được tách ra khỏi nhau bằng cách cho chúng đi qua một cột chứa vật liệu trao đổi ion. Các amino axit có điện tích khác nhau sẽ liên kết với vật liệu trao đổi ion với ái lực khác nhau, do đó chúng sẽ được tách ra khỏi nhau.
- Ứng dụng: Sắc ký ion được sử dụng rộng rãi trong phân tích amino axit trong thực phẩm, dược phẩm và các mẫu sinh học.
9.2. Sắc Ký Lỏng Hiệu Năng Cao (HPLC)
HPLC là một kỹ thuật sắc ký được sử dụng để tách và định lượng các amino axit dựa trên tính chất hóa học của chúng.
- Nguyên tắc: Các amino axit được tách ra khỏi nhau bằng cách cho chúng đi qua một cột chứa vật liệu hấp phụ. Các amino axit có ái lực khác nhau với vật liệu hấp phụ sẽ được tách ra khỏi nhau.
- Ứng dụng: HPLC được sử dụng rộng rãi trong phân tích amino axit trong nhiều loại mẫu khác nhau.
9.3. Sắc Ký Khí (GC)
GC là một kỹ thuật sắc ký được sử dụng để tách và định lượng các amino axit sau khi chúng được chuyển thành các dẫn xuất dễ bay hơi.
- Nguyên tắc: Các dẫn xuất amino axit được tách ra khỏi nhau bằng cách cho chúng đi qua một cột chứa pha tĩnh. Các dẫn xuất có áp suất hơi khác nhau sẽ được tách ra khỏi nhau.
- Ứng dụng: GC được sử dụng để phân tích amino axit trong các mẫu phức tạp.
9.4. Điện Di Mao Quản (CE)
CE là một kỹ thuật phân tích được sử dụng để tách và định lượng các amino axit dựa trên điện tích và kích thước của chúng.
- Nguyên tắc: Các amino axit được tách ra khỏi nhau bằng cách cho chúng di chuyển qua một mao quản chứa chất điện ly dưới tác dụng của điện trường. Các amino axit có điện tích và kích thước khác nhau sẽ di chuyển với tốc độ khác nhau, do đó chúng sẽ được tách ra khỏi nhau.
- Ứng dụng: CE được sử dụng để phân tích amino axit trong các mẫu có khối lượng nhỏ.
10. Câu Hỏi Thường Gặp Về Tính Lưỡng Tính Của Amino Axit (FAQ)
Dưới đây là một số câu hỏi thường gặp về tính lưỡng tính của amino axit:
10.1. Amino Axit Nào Có Tính Lưỡng Tính Mạnh Nhất?
Amino axit có tính lưỡng tính mạnh nhất là những amino axit có nhóm R chứa các nhóm chức có tính axit hoặc bazơ mạnh. Ví dụ, aspartic acid và glutamic acid có nhóm R chứa nhóm carboxyl (-COOH) có tính axit, trong khi lysine và arginine có nhóm R chứa nhóm amino (-NH2) hoặc guanidino (-NHC(=NH)NH2) có tính bazơ.
10.2. Tại Sao Glycine Lại Có Tính Lưỡng Tính?
Glycine có tính lưỡng tính vì nó có cả nhóm amino (-NH2) có tính bazơ và nhóm carboxyl (-COOH) có tính axit trong phân tử của nó. Mặc dù nhóm R của glycine chỉ là một nguyên tử hydro, nhưng sự hiện diện của cả hai nhóm chức axit và bazơ cho phép glycine phản ứng với cả axit và bazơ.
10.3. Tính Lưỡng Tính Của Amino Axit Ảnh Hưởng Đến Cấu Trúc Protein Như Thế Nào?
Tính lưỡng tính của amino axit ảnh hưởng đến cấu trúc protein bằng cách ảnh hưởng đến các tương tác giữa các amino axit trong chuỗi polypeptide. Các amino axit có tính axit có thể tạo thành liên kết ion với các amino axit có tính bazơ, giúp ổn định cấu trúc ba chiều của protein.
10.4. Điểm Đẳng Điện Của Protein Là Gì?
Điểm đẳng điện của protein là giá trị pH mà tại đó protein có điện tích tổng bằng không. Tại điểm đẳng điện, protein thường có độ tan thấp nhất và dễ kết tủa nhất.
10.5. Làm Thế Nào Để Xác Định Điểm Đẳng Điện Của Protein?
Điểm đẳng điện của protein có thể được xác định bằng phương pháp điện di đẳng điện hoặc bằng cách sử dụng các phần mềm tính toán dựa trên thành phần amino axit của protein.
10.6. Tính Lưỡng Tính Của Amino Axit Có Vai Trò Gì Trong Enzyme?
Tính lưỡng tính của amino axit đóng vai trò quan trọng trong hoạt động của enzyme. Các amino axit có tính lưỡng tính thường có mặt tại trung tâm hoạt động của enzyme, nơi chúng có thể tương tác với cơ chất và xúc tác các phản ứng hóa học.
10.7. Amino Axit Có Tính Lưỡng Tính Có Thể Hoạt Động Như Chất Đệm Được Không?
Có, amino axit có tính lưỡng tính có thể hoạt động như chất đệm, giúp duy trì pH ổn định trong dung dịch. Chúng có thể hấp thụ cả axit và bazơ, ngăn chặn sự thay đổi pH đột ngột.
10.8. Ứng Dụng Của Tính Lưỡng Tính Trong Công Nghiệp Thực Phẩm Là Gì?
Trong công nghiệp thực phẩm, tính lưỡng tính của amino axit được ứng dụng để cải thiện hương vị, giá trị dinh dưỡng và thời hạn sử dụng của thực phẩm. Ví dụ, glutamate được sử dụng làm chất tạo hương, trong khi các amino axit khác có thể được sử dụng làm chất bảo quản hoặc bổ sung dinh dưỡng.
10.9. Amino Axit Có Tính Lưỡng Tính Có Thể Tạo Phức Với Ion Kim Loại Không?
Có, amino axit có tính lưỡng tính có khả năng tạo phức với các ion kim loại. Khả năng này được sử dụng trong xử lý nước và phân tích hóa học.
10.10. Tại Sao Cần Nghiên Cứu Tính Lưỡng Tính Của Amino Axit?
Nghiên cứu tính lưỡng tính của amino axit rất quan trọng vì nó giúp chúng ta hiểu rõ hơn về cấu trúc, chức năng và tính chất hóa học của các phân tử này. Điều này có ý nghĩa lớn trong nhiều lĩnh vực, bao gồm y học, công nghiệp thực phẩm, nông nghiệp và hóa học.
Hy vọng những thông tin chi tiết này từ Xe Tải Mỹ Đình đã giúp bạn hiểu rõ hơn về tính lưỡng tính của amino axit và vai trò quan trọng của chúng trong nhiều lĩnh vực.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Đừng ngần ngại truy cập ngay XETAIMYDINH.EDU.VN để được tư vấn và giải đáp mọi thắc mắc. Tại Xe Tải Mỹ Đình, chúng tôi cam kết cung cấp thông tin chính xác, cập nhật và hữu ích nhất, giúp bạn đưa ra quyết định sáng suốt nhất cho nhu cầu của mình. Liên hệ ngay với chúng tôi qua hotline 0247 309 9988 hoặc ghé thăm địa chỉ Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội để được hỗ trợ tận tình.