Công Thức Phân Tử Của Benzen Là C6H6. Bạn đang tìm hiểu về benzen, từ công thức hóa học đến ứng dụng thực tế và những lưu ý an toàn? Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ cung cấp cho bạn một cái nhìn toàn diện, giúp bạn hiểu rõ về hợp chất quan trọng này trong công nghiệp và đời sống. Bài viết này sẽ đi sâu vào cấu trúc, tính chất, ứng dụng và những cảnh báo quan trọng về benzen, đi kèm các thông tin về an toàn và sức khỏe liên quan.
1. Benzen Là Gì?
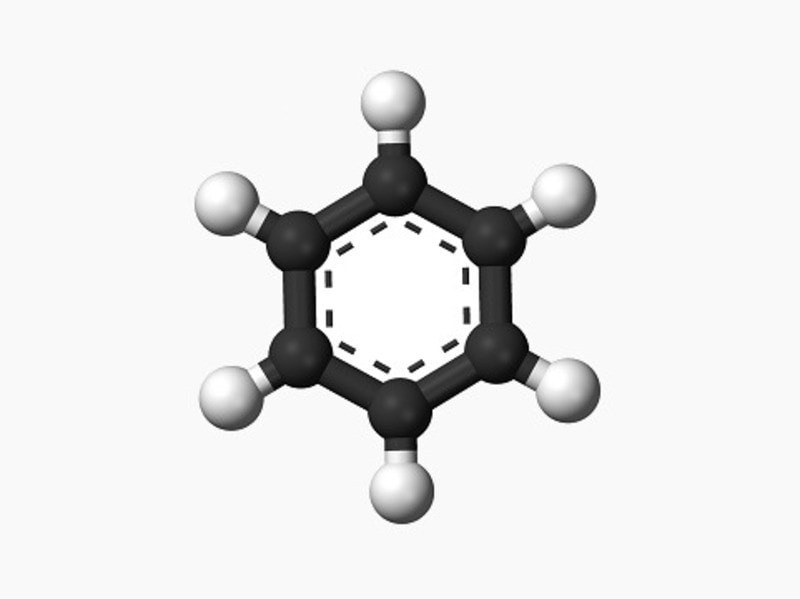 Công thức cấu tạo benzen vòng 6 cạnh
Công thức cấu tạo benzen vòng 6 cạnh
Benzen là một hợp chất hữu cơ, một hydrocacbon thơm với công thức phân tử là C6H6. Đó là một chất lỏng không màu, dễ bay hơi và có mùi thơm đặc trưng. Benzen ít tan trong nước nhưng tan tốt trong các dung môi hữu cơ như etanol, dietyl ete và đặc biệt là trong các chất béo. Benzen là một nguyên liệu quan trọng trong nhiều ngành công nghiệp hóa chất.
1.1. Cấu Trúc Phân Tử Đặc Biệt Của Benzen
Benzen có cấu trúc vòng với sáu nguyên tử carbon liên kết với nhau, tạo thành một lục giác đều. Mỗi nguyên tử carbon liên kết với một nguyên tử hydro. Điều đặc biệt là các liên kết giữa các nguyên tử carbon không phải là liên kết đơn hay liên kết đôi xen kẽ như công thức cổ điển của Kekulé, mà là các liên kết pi (π) được giải tỏa trên toàn vòng. Điều này mang lại cho benzen tính ổn định cao và các tính chất hóa học đặc trưng.
1.2. Đặc Điểm Nhận Dạng Benzen
Benzen có một số đặc điểm giúp nhận dạng nó:
- Trạng thái vật lý: Chất lỏng không màu ở nhiệt độ phòng.
- Mùi: Mùi thơm đặc trưng, dễ nhận biết.
- Tính tan: Ít tan trong nước, tan tốt trong dung môi hữu cơ.
- Tính cháy: Dễ cháy, tạo ra ngọn lửa có nhiều khói đen.
- Độc tính: Độc hại, có thể gây ảnh hưởng đến sức khỏe.
1.3. Ứng Dụng Rộng Rãi Của Benzen Trong Công Nghiệp
Trong công nghiệp, benzen được sử dụng rộng rãi làm nguyên liệu để sản xuất nhiều hợp chất hữu cơ quan trọng khác, bao gồm:
- Styrene: Sản xuất nhựa polystyrene, được sử dụng trong sản xuất vật liệu cách nhiệt, bao bì thực phẩm và nhiều sản phẩm khác.
- Phenol: Sản xuất nhựa phenolic, được sử dụng trong sản xuất chất kết dính, vật liệu composite và các sản phẩm khác.
- Cyclohexane: Sản xuất nylon, một loại polyme quan trọng được sử dụng trong sản xuất sợi, vải và các sản phẩm khác.
- Aniline: Sản xuất thuốc nhuộm, dược phẩm và các hóa chất khác.
- Cumene: Sản xuất phenol và acetone.
Theo thống kê của Bộ Công Thương năm 2023, ngành công nghiệp hóa chất Việt Nam tiêu thụ hàng chục ngàn tấn benzen mỗi năm, chủ yếu cho sản xuất các sản phẩm nhựa và hóa chất cơ bản.
2. Công Thức Phân Tử và Cấu Tạo Chi Tiết Của Benzen
2.1. Công Thức Phân Tử C6H6: Ý Nghĩa và Giải Thích
Công thức phân tử C6H6 cho biết mỗi phân tử benzen chứa 6 nguyên tử carbon (C) và 6 nguyên tử hydro (H). Tỷ lệ này rất quan trọng vì nó cho thấy benzen là một hydrocacbon không no cao, nghĩa là nó có ít nguyên tử hydro hơn so với một ankan mạch hở có cùng số lượng nguyên tử carbon.
2.2. Công Thức Cấu Tạo Của Benzen: Từ Kekulé Đến Mô Hình Hiện Đại
Công thức cấu tạo của benzen đã trải qua nhiều thay đổi và cải tiến theo thời gian.
- Công thức Kekulé: Vào thế kỷ 19, nhà hóa học Friedrich August Kekulé đề xuất công thức cấu tạo của benzen là một vòng sáu cạnh với các liên kết đơn và liên kết đôi xen kẽ. Tuy nhiên, công thức này không giải thích được tính ổn định cao và tính chất hóa học đặc biệt của benzen.
- Mô hình hiện đại: Mô hình hiện đại mô tả benzen là một vòng sáu cạnh với các liên kết pi (π) được giải tỏa trên toàn vòng. Điều này có nghĩa là các electron pi không cố định giữa hai nguyên tử carbon cụ thể, mà chúng di chuyển tự do trên toàn vòng. Sự giải tỏa electron này tạo ra một hệ thống electron ổn định, giải thích cho tính ổn định cao của benzen.
2.3. Các Dạng Biểu Diễn Cấu Trúc Benzen Thường Gặp
Có nhiều cách để biểu diễn cấu trúc của benzen, bao gồm:
- Công thức cấu tạo khai triển: Hiển thị tất cả các liên kết giữa các nguyên tử.
- Công thức cấu tạo rút gọn: Chỉ hiển thị các liên kết chính, bỏ qua các liên kết C-H.
- Công thức vòng benzen: Chỉ hiển thị vòng sáu cạnh, thường có một vòng tròn bên trong để biểu thị sự giải tỏa electron.
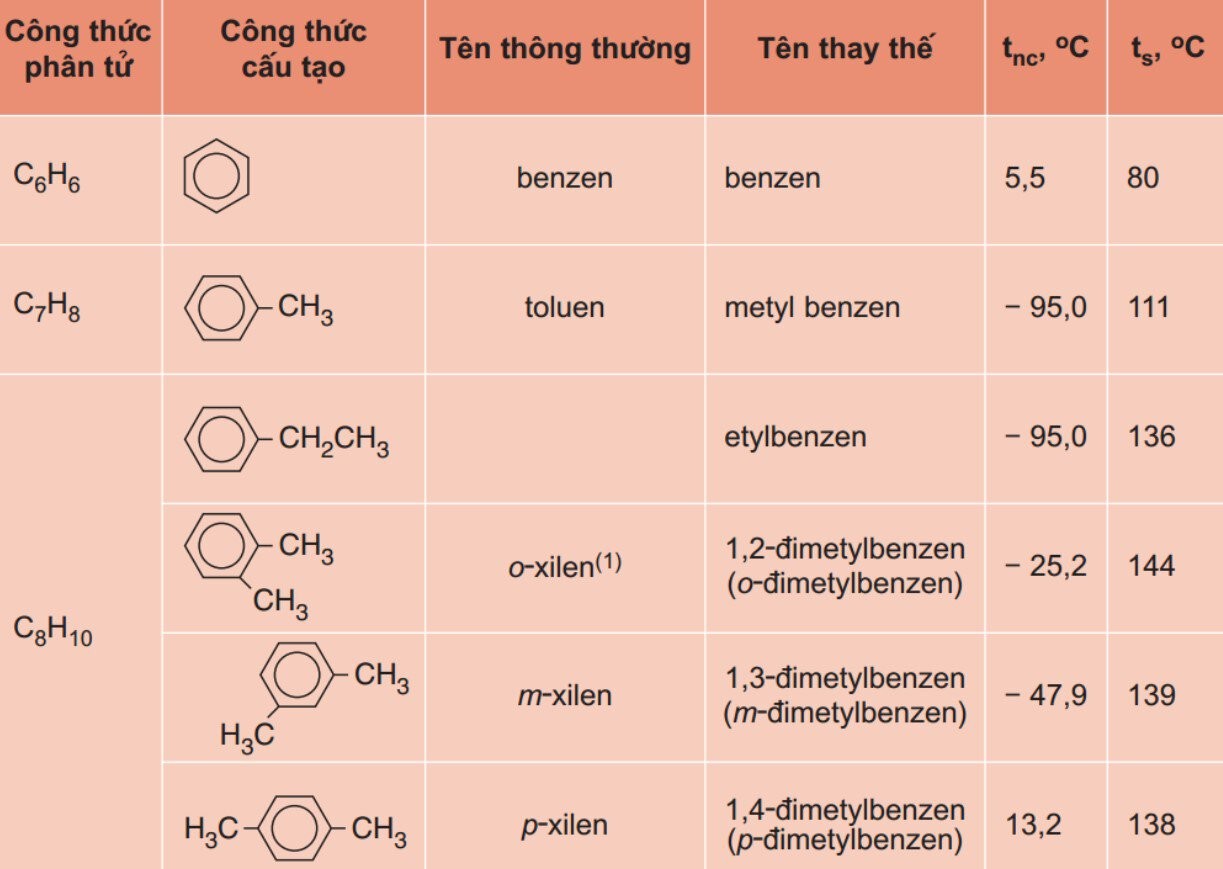 Công thức cấu tạo Benzen
Công thức cấu tạo Benzen
2.4. So Sánh Cấu Trúc Benzen Với Các Hydrocacbon Thơm Khác
Benzen là hydrocacbon thơm đơn giản nhất. Các hydrocacbon thơm khác có thể có thêm các nhóm thế gắn vào vòng benzen hoặc có nhiều vòng benzen liên kết với nhau. Ví dụ:
- Toluene: Vòng benzen có một nhóm metyl (CH3) gắn vào.
- Xylene: Vòng benzen có hai nhóm metyl gắn vào.
- Naphthalene: Hai vòng benzen liên kết với nhau.
Cấu trúc của các hydrocacbon thơm này ảnh hưởng đến tính chất hóa học và ứng dụng của chúng.
3. Tính Chất Vật Lý Đặc Trưng Của Benzen (C6H6)
3.1. Trạng Thái, Màu Sắc, Mùi Vị Của Benzen
- Trạng thái: Benzen là chất lỏng ở nhiệt độ phòng (khoảng 25°C).
- Màu sắc: Không màu.
- Mùi: Mùi thơm đặc trưng, dễ nhận biết.
- Vị: Không nên nếm thử vì benzen độc hại.
3.2. Điểm Nóng Chảy, Điểm Sôi Và Khối Lượng Riêng Của Benzen
- Điểm nóng chảy: 5.5 °C
- Điểm sôi: 80.1 °C
- Khối lượng riêng: 0.876 g/cm³ (ở 20°C)
Những thông số này cho thấy benzen là một chất lỏng dễ bay hơi, có nghĩa là nó chuyển từ trạng thái lỏng sang trạng thái khí ở nhiệt độ tương đối thấp.
3.3. Độ Tan Của Benzen Trong Nước Và Các Dung Môi Khác
Benzen ít tan trong nước (khoảng 1.8 g/L ở 25°C) nhưng tan tốt trong các dung môi hữu cơ như etanol, dietyl ete, và đặc biệt là trong các chất béo. Điều này là do benzen là một phân tử không phân cực, trong khi nước là một phân tử phân cực.
3.4. Tính Chất Hấp Phụ Ánh Sáng Của Benzen
Benzen có khả năng hấp thụ ánh sáng trong vùng tử ngoại (UV). Điều này được sử dụng trong các phương pháp phân tích quang phổ để xác định và định lượng benzen trong các mẫu.
3.5. Bảng Tổng Hợp Các Tính Chất Vật Lý Của Benzen
| Tính Chất | Giá Trị |
|---|---|
| Trạng thái | Lỏng |
| Màu sắc | Không màu |
| Mùi | Thơm đặc trưng |
| Điểm nóng chảy | 5.5 °C |
| Điểm sôi | 80.1 °C |
| Khối lượng riêng | 0.876 g/cm³ (ở 20°C) |
| Độ tan trong nước | 1.8 g/L (ở 25°C) |
| Hấp thụ ánh sáng | Vùng tử ngoại (UV) |
| Áp suất hơi bão hòa | 10 kPa (ở 20 °C) |
| Độ nhớt | 0.652 cP (ở 20 °C) |
| Chiết suất | 1.5011 (ở 20 °C) |
Nguồn: Tổng hợp từ các tài liệu hóa học uy tín
4. Tính Chất Hóa Học Quan Trọng Của Benzen
4.1. Phản Ứng Thế (Substitution Reactions): Halogen Hóa, Nitro Hóa, Sulfon Hóa
Benzen tham gia vào các phản ứng thế ái điện tử, trong đó một nguyên tử hydro trên vòng benzen được thay thế bằng một nhóm thế khác. Các phản ứng thế quan trọng bao gồm:
- Halogen hóa: Thay thế hydro bằng halogen (ví dụ: clo, brom) với xúc tác là FeCl3 hoặc AlCl3.
- Nitro hóa: Thay thế hydro bằng nhóm nitro (NO2) với xúc tác là H2SO4 đặc.
- Sulfon hóa: Thay thế hydro bằng nhóm sulfonic (SO3H) với xúc tác là H2SO4 đặc.
Các phản ứng này tạo ra các dẫn xuất benzen quan trọng trong công nghiệp hóa chất.
4.2. Phản Ứng Cộng (Addition Reactions): Hiđro Hóa, Clo Hóa
Mặc dù benzen có tính ổn định cao, nó vẫn có thể tham gia vào các phản ứng cộng trong điều kiện khắc nghiệt.
- Hiđro hóa: Cộng hydro vào vòng benzen để tạo thành cyclohexane với xúc tác là kim loại (ví dụ: Ni, Pt) và nhiệt độ cao.
- Clo hóa: Cộng clo vào vòng benzen dưới ánh sáng tử ngoại (UV) để tạo thành benzene hexachloride (BHC), một loại thuốc trừ sâu.
4.3. Phản Ứng Oxi Hóa: Cháy Hoàn Toàn, Oxi Hóa Không Hoàn Toàn
- Cháy hoàn toàn: Benzen cháy trong oxy tạo ra CO2 và H2O.
- 2 C6H6 + 15 O2 → 12 CO2 + 6 H2O
- Oxi hóa không hoàn toàn: Oxi hóa benzen với xúc tác V2O5 ở nhiệt độ cao tạo ra maleic anhydride, một nguyên liệu quan trọng trong sản xuất nhựa polyester.
4.4. So Sánh Tính Chất Hóa Học Của Benzen Với Các Hydrocacbon No Và Không No Khác
So với các hydrocacbon no (ankan) và không no (anken, ankin), benzen có tính chất hóa học khác biệt:
- Tính ổn định: Benzen ổn định hơn nhiều so với các hydrocacbon không no mạch hở.
- Phản ứng thế: Benzen dễ tham gia vào các phản ứng thế hơn là phản ứng cộng.
- Phản ứng cộng: Benzen chỉ tham gia vào phản ứng cộng trong điều kiện khắc nghiệt.
Sự khác biệt này là do cấu trúc đặc biệt của benzen với các electron pi được giải tỏa trên toàn vòng.
4.5. Bảng Tóm Tắt Các Phản Ứng Hóa Học Quan Trọng Của Benzen
| Phản Ứng | Tác Nhân và Điều Kiện | Sản Phẩm |
|---|---|---|
| Halogen hóa | Halogen (Cl2, Br2), FeCl3/AlCl3 | Halogenbenzen (ví dụ: Clorobenzen) |
| Nitro hóa | HNO3 đặc, H2SO4 đặc | Nitrobenzen |
| Sulfon hóa | H2SO4 đặc | Benzenesulfonic acid |
| Hiđro hóa | H2, Ni/Pt, nhiệt độ | Cyclohexane |
| Clo hóa (ánh sáng) | Cl2, ánh sáng UV | Benzene hexachloride (BHC) |
| Cháy hoàn toàn | O2, nhiệt độ | CO2 + H2O |
| Oxi hóa không hoàn toàn | O2, V2O5, nhiệt độ | Maleic anhydride |
Nguồn: Tổng hợp từ các tài liệu hóa học uy tín
5. Các Phương Pháp Điều Chế Benzen (C6H6) Trong Công Nghiệp
5.1. Tách Benzen Từ Dầu Mỏ Và Than Đá
- Từ dầu mỏ: Benzen được tách ra từ phân đoạn naphtha của dầu mỏ thông qua quá trình reforming xúc tác. Quá trình này chuyển đổi các hydrocacbon mạch hở thành hydrocacbon thơm, bao gồm benzen.
- Từ than đá: Benzen được tách ra từ nhựa than đá, một sản phẩm phụ của quá trình sản xuất than cốc. Nhựa than đá được chưng cất để tách ra các phân đoạn khác nhau, bao gồm phân đoạn chứa benzen.
5.2. Các Phương Pháp Tổng Hợp Benzen Từ Các Hợp Chất Khác
- Dehydrocyclization của n-hexane: N-hexane được chuyển hóa thành benzen bằng cách sử dụng xúc tác Pt/Al2O3 ở nhiệt độ cao.
- C6H14 → C6H6 + 4 H2
- Trimer hóa của acetylene: Acetylene được trimer hóa thành benzen bằng cách sử dụng xúc tác kim loại (ví dụ: Ni) ở nhiệt độ cao.
- 3 C2H2 → C6H6
- Alkylation và dealkylation của toluene: Toluene có thể được alkyl hóa bằng ethylene để tạo thành xylene, sau đó xylene có thể được dealkyl hóa để tạo thành benzen.
5.3. Quy Trình Sản Xuất Benzen Trong Công Nghiệp Hiện Đại
Quy trình sản xuất benzen trong công nghiệp hiện đại thường bao gồm các bước sau:
- Chuẩn bị nguyên liệu: Lựa chọn và xử lý nguyên liệu đầu vào (ví dụ: naphtha, nhựa than đá).
- Reforming xúc tác: Chuyển đổi các hydrocacbon mạch hở thành hydrocacbon thơm.
- Tách benzen: Tách benzen ra khỏi hỗn hợp các hydrocacbon thơm khác bằng phương pháp chưng cất hoặc chiết ly.
- Tinh chế benzen: Loại bỏ các tạp chất để thu được benzen có độ tinh khiết cao.
5.4. So Sánh Hiệu Quả Và Chi Phí Của Các Phương Pháp Điều Chế Benzen
Hiệu quả và chi phí của các phương pháp điều chế benzen khác nhau tùy thuộc vào nguyên liệu đầu vào, công nghệ sử dụng và quy mô sản xuất.
- Tách benzen từ dầu mỏ: Phương pháp phổ biến nhất, hiệu quả cao và chi phí tương đối thấp.
- Tách benzen từ than đá: Phương pháp ít phổ biến hơn, hiệu quả thấp hơn và chi phí cao hơn.
- Dehydrocyclization của n-hexane: Phương pháp hiệu quả, nhưng chi phí cao do yêu cầu sử dụng xúc tác đắt tiền.
- Trimer hóa của acetylene: Phương pháp ít được sử dụng do acetylene là một nguyên liệu đắt tiền và khó bảo quản.
5.5. Bảng So Sánh Các Phương Pháp Điều Chế Benzen
| Phương Pháp | Nguyên Liệu | Ưu Điểm | Nhược Điểm |
|---|---|---|---|
| Tách từ dầu mỏ | Naphtha | Phổ biến, hiệu quả cao, chi phí tương đối thấp | Phụ thuộc vào nguồn cung dầu mỏ |
| Tách từ than đá | Nhựa than đá | Tận dụng sản phẩm phụ | Hiệu quả thấp, chi phí cao |
| Dehydrocyclization n-hexane | N-hexane | Hiệu quả cao | Chi phí xúc tác cao |
| Trimer hóa acetylene | Acetylene | Nguyên liệu đắt tiền, khó bảo quản |
Nguồn: Tổng hợp từ các tài liệu công nghiệp hóa chất
6. Ứng Dụng Rộng Rãi Của Benzen (C6H6) Trong Đời Sống Và Công Nghiệp
6.1. Benzen Là Nguyên Liệu Quan Trọng Trong Sản Xuất Polyme (Nhựa, Cao Su, Sợi)
Benzen là một nguyên liệu quan trọng để sản xuất nhiều loại polyme, bao gồm:
- Polystyrene: Được sử dụng trong sản xuất vật liệu cách nhiệt, bao bì thực phẩm, đồ chơi và nhiều sản phẩm khác.
- Nylon: Được sử dụng trong sản xuất sợi, vải, thảm, dây thừng và các sản phẩm khác.
- Cao su tổng hợp: Được sử dụng trong sản xuất lốp xe, ống dẫn, gioăng và các sản phẩm khác.
6.2. Benzen Được Sử Dụng Làm Dung Môi Trong Nhiều Ngành Công Nghiệp
Benzen là một dung môi tốt cho nhiều chất hữu cơ, do đó nó được sử dụng rộng rãi trong các ngành công nghiệp như:
- Sản xuất sơn và mực in: Benzen giúp hòa tan các chất màu và nhựa trong sơn và mực in.
- Sản xuất chất tẩy rửa: Benzen giúp hòa tan các chất béo và dầu mỡ trong chất tẩy rửa.
- Sản xuất dược phẩm: Benzen được sử dụng để chiết xuất và tinh chế các hợp chất dược phẩm.
6.3. Benzen Trong Sản Xuất Dược Phẩm, Thuốc Nhuộm, Thuốc Trừ Sâu
Benzen là một nguyên liệu quan trọng để sản xuất nhiều loại dược phẩm, thuốc nhuộm và thuốc trừ sâu. Ví dụ:
- Aspirin: Một loại thuốc giảm đau và hạ sốt phổ biến.
- Paracetamol: Một loại thuốc giảm đau và hạ sốt khác.
- Aniline dyes: Một loại thuốc nhuộm được sử dụng rộng rãi trong ngành dệt may.
- DDT: Một loại thuốc trừ sâu đã từng được sử dụng rộng rãi (hiện nay đã bị cấm ở nhiều quốc gia).
6.4. Các Ứng Dụng Khác Của Benzen Trong Đời Sống Hàng Ngày
Ngoài các ứng dụng trên, benzen còn được sử dụng trong một số ứng dụng khác trong đời sống hàng ngày, chẳng hạn như:
- Sản xuất chất nổ: Benzen là một thành phần của một số loại chất nổ.
- Sản xuất xăng: Benzen được thêm vào xăng để tăng chỉ số octane và cải thiện hiệu suất động cơ.
6.5. Bảng Tổng Hợp Các Ứng Dụng Quan Trọng Của Benzen
| Ứng Dụng | Sản Phẩm/Ngành Công Nghiệp |
|---|---|
| Sản xuất polyme | Nhựa (polystyrene, nylon), cao su tổng hợp |
| Dung môi | Sơn, mực in, chất tẩy rửa, dược phẩm |
| Dược phẩm | Aspirin, paracetamol |
| Thuốc nhuộm | Aniline dyes |
| Thuốc trừ sâu | (Một số loại, đã bị hạn chế) |
| Chất nổ | (Một số loại) |
| Xăng | Tăng chỉ số octane |
Nguồn: Tổng hợp từ các tài liệu công nghiệp và hóa học
7. Độc Tính Của Benzen (C6H6) Và Các Biện Pháp Phòng Ngừa
7.1. Các Đường Xâm Nhập Của Benzen Vào Cơ Thể (Hô Hấp, Da, Tiêu Hóa)
Benzen có thể xâm nhập vào cơ thể qua các đường sau:
- Hô hấp: Hít phải hơi benzen trong không khí. Đây là đường xâm nhập phổ biến nhất trong môi trường làm việc.
- Da: Tiếp xúc trực tiếp với benzen lỏng. Benzen có thể hấp thụ qua da và gây kích ứng.
- Tiêu hóa: Uống phải nước hoặc thực phẩm bị nhiễm benzen.
7.2. Các Triệu Chứng Ngộ Độc Benzen Cấp Tính Và Mãn Tính
- Ngộ độc cấp tính: Các triệu chứng bao gồm chóng mặt, nhức đầu, buồn nôn, nôn mửa, khó thở, co giật và mất ý thức. Trong trường hợp nghiêm trọng, có thể dẫn đến tử vong.
- Ngộ độc mãn tính: Các triệu chứng bao gồm mệt mỏi, suy nhược, chán ăn, giảm cân, thiếu máu, giảm bạch cầu, giảm tiểu cầu, và tăng nguy cơ mắc bệnh bạch cầu (ung thư máu).
7.3. Ảnh Hưởng Của Benzen Đến Sức Khỏe (Ung Thư, Tổn Thương Hệ Thần Kinh, Rối Loạn Máu)
Benzen là một chất gây ung thư đã được biết đến. Tiếp xúc lâu dài với benzen có thể làm tăng nguy cơ mắc bệnh bạch cầu và các loại ung thư khác. Ngoài ra, benzen còn có thể gây tổn thương hệ thần kinh, rối loạn máu và các vấn đề sức khỏe khác.
7.4. Các Biện Pháp Phòng Ngừa Khi Tiếp Xúc Với Benzen
- Sử dụng thiết bị bảo hộ cá nhân (PPE): Đeo khẩu trang, găng tay, kính bảo hộ và quần áo bảo hộ khi làm việc với benzen.
- Đảm bảo thông gió tốt: Làm việc trong khu vực thông thoáng hoặc sử dụng hệ thống thông gió cục bộ để giảm nồng độ benzen trong không khí.
- Tránh tiếp xúc trực tiếp với da: Rửa tay kỹ bằng xà phòng và nước sau khi tiếp xúc với benzen.
- Không ăn uống hoặc hút thuốc trong khu vực làm việc: Để tránh nuốt phải benzen.
- Đào tạo và hướng dẫn: Cung cấp đào tạo và hướng dẫn cho người lao động về các nguy cơ và biện pháp phòng ngừa khi làm việc với benzen.
- Kiểm tra sức khỏe định kỳ: Thực hiện kiểm tra sức khỏe định kỳ cho người lao động tiếp xúc với benzen để phát hiện sớm các dấu hiệu ngộ độc.
7.5. Các Quy Định Và Tiêu Chuẩn Về An Toàn Khi Sử Dụng Benzen
Có nhiều quy định và tiêu chuẩn về an toàn khi sử dụng benzen, bao gồm:
- Giới hạn tiếp xúc cho phép (PEL): Quy định nồng độ benzen tối đa cho phép trong không khí tại nơi làm việc.
- Yêu cầu về thông gió: Quy định các yêu cầu về thông gió để giảm nồng độ benzen trong không khí.
- Yêu cầu về PPE: Quy định việc sử dụng các thiết bị bảo hộ cá nhân khi làm việc với benzen.
- Yêu cầu về đào tạo: Quy định việc đào tạo và hướng dẫn cho người lao động về các nguy cơ và biện pháp phòng ngừa khi làm việc với benzen.
Tại Việt Nam, các quy định về an toàn hóa chất được ban hành bởi Bộ Công Thương và Bộ Y tế.
8. Các Câu Hỏi Thường Gặp Về Benzen (FAQ)
8.1. Benzen Có Mùi Gì?
Benzen có mùi thơm đặc trưng, hơi ngọt. Tuy nhiên, không nên cố ý ngửi benzen vì nó độc hại.
8.2. Benzen Có Tan Trong Nước Không?
Benzen ít tan trong nước.
8.3. Benzen Có Gây Ung Thư Không?
Có, benzen là một chất gây ung thư đã được biết đến, đặc biệt là ung thư máu (bạch cầu).
8.4. Làm Thế Nào Để Phát Hiện Benzen Trong Không Khí?
Có thể sử dụng các thiết bị đo nồng độ benzen trong không khí. Các thiết bị này có thể được sử dụng để kiểm tra chất lượng không khí trong nhà và ngoài trời.
8.5. Benzen Được Sử Dụng Để Làm Gì?
Benzen được sử dụng làm nguyên liệu để sản xuất nhiều loại sản phẩm, bao gồm nhựa, cao su, sợi, sơn, mực in, chất tẩy rửa, dược phẩm và thuốc trừ sâu.
8.6. Benzen Có Tồn Tại Trong Xăng Không?
Có, benzen có thể tồn tại trong xăng với một lượng nhỏ. Tuy nhiên, hàm lượng benzen trong xăng đã được giới hạn ở mức thấp để giảm nguy cơ tiếp xúc.
8.7. Tiếp Xúc Với Benzen Có Nguy Hiểm Không?
Có, tiếp xúc với benzen có thể gây nguy hiểm cho sức khỏe. Tiếp xúc lâu dài với benzen có thể làm tăng nguy cơ mắc bệnh ung thư và các vấn đề sức khỏe khác.
8.8. Làm Thế Nào Để Giảm Thiểu Tiếp Xúc Với Benzen?
Có thể giảm thiểu tiếp xúc với benzen bằng cách sử dụng các thiết bị bảo hộ cá nhân, đảm bảo thông gió tốt và tránh tiếp xúc trực tiếp với da.
8.9. Benzen Có Thể Tìm Thấy Ở Đâu Trong Đời Sống Hàng Ngày?
Benzen có thể tìm thấy trong khói thuốc lá, khí thải ô tô, một số sản phẩm gia dụng (như sơn, chất tẩy rửa) và nước uống bị ô nhiễm.
8.10. Benzen Ảnh Hưởng Đến Môi Trường Như Thế Nào?
Benzen có thể gây ô nhiễm không khí và nước. Nó có thể gây hại cho các sinh vật sống trong môi trường.
9. Xe Tải Mỹ Đình: Đối Tác Tin Cậy Của Bạn Trong Lĩnh Vực Vận Tải
Tại Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN), chúng tôi hiểu rõ tầm quan trọng của việc lựa chọn xe tải phù hợp với nhu cầu kinh doanh của bạn. Chúng tôi cung cấp thông tin chi tiết và cập nhật về các loại xe tải có sẵn ở Mỹ Đình, Hà Nội, so sánh giá cả và thông số kỹ thuật giữa các dòng xe, tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách, và giải đáp các thắc mắc liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải.
Bạn đang tìm kiếm một chiếc xe tải bền bỉ, tiết kiệm nhiên liệu và phù hợp với ngân sách của mình?
Hãy đến với Xe Tải Mỹ Đình!
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
Đừng ngần ngại liên hệ với chúng tôi để được tư vấn và hỗ trợ tốt nhất!
10. Kết Luận
Benzen là một hợp chất hóa học quan trọng với nhiều ứng dụng trong công nghiệp và đời sống. Tuy nhiên, nó cũng là một chất độc hại và có thể gây nguy hiểm cho sức khỏe. Việc hiểu rõ về công thức, tính chất, ứng dụng và độc tính của benzen là rất quan trọng để sử dụng nó một cách an toàn và hiệu quả. Xe Tải Mỹ Đình hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích về benzen.