Cho 2.7 gam Al tác dụng hoàn toàn với dung dịch NaOH dư sẽ thu được dung dịch natri aluminat (NaAlO2) và khí hidro (H2). Hãy cùng Xe Tải Mỹ Đình đi sâu vào phản ứng hóa học thú vị này và khám phá những ứng dụng quan trọng của nó trong thực tế, đồng thời tìm hiểu về các yếu tố ảnh hưởng và cách tính toán liên quan. Đừng quên truy cập XETAIMYDINH.EDU.VN để khám phá thêm nhiều thông tin hữu ích về hóa học và các ứng dụng của nó.
1. Phản Ứng Giữa Al và NaOH Dư: Bản Chất và Cơ Chế
Phản ứng giữa nhôm (Al) và natri hidroxit (NaOH) là một phản ứng hóa học quan trọng trong hóa vô cơ, đặc biệt là trong lĩnh vực luyện kim và xử lý nước. Phản ứng này thuộc loại phản ứng ăn mòn hóa học, trong đó nhôm bị ăn mòn bởi dung dịch kiềm mạnh.
1.1. Phương trình hóa học
Phương trình hóa học tổng quát của phản ứng như sau:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
Trong đó:
- Al là nhôm (aluminum)
- NaOH là natri hidroxit (sodium hydroxide)
- H2O là nước
- NaAlO2 là natri aluminat (sodium aluminate)
- H2 là khí hidro (hydrogen)
1.2. Cơ chế phản ứng
Phản ứng xảy ra qua nhiều giai đoạn phức tạp, nhưng có thể tóm tắt như sau:
-
Phản ứng ban đầu: Nhôm tác dụng với nước tạo thành lớp nhôm hidroxit (Al(OH)3) trên bề mặt:
2Al + 6H2O → 2Al(OH)3 + 3H2
-
Phản ứng với NaOH: Lớp nhôm hidroxit này sau đó phản ứng với natri hidroxit tạo thành natri aluminat tan trong nước:
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Tổng hợp hai giai đoạn trên, ta có phương trình phản ứng tổng quát.
1.3. Vai trò của NaOH dư
NaOH đóng vai trò quan trọng trong việc hòa tan lớp nhôm hidroxit, giúp phản ứng tiếp tục diễn ra. Nếu NaOH không dư, phản ứng có thể dừng lại do lớp Al(OH)3 bảo vệ bề mặt nhôm.
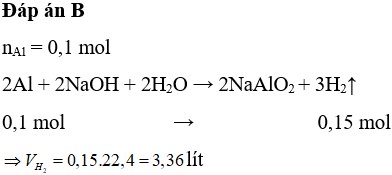 Phản ứng giữa nhôm và natri hidroxit
Phản ứng giữa nhôm và natri hidroxit
Alt: Sơ đồ phản ứng giữa nhôm và dung dịch natri hidroxit tạo thành natri aluminat và khí hidro.
2. Tính Toán Lượng Khí H2 Thu Được Khi Cho 2.7 Gam Al Tác Dụng Với NaOH Dư
Để tính toán lượng khí H2 thu được, ta cần xác định số mol của Al tham gia phản ứng, từ đó suy ra số mol của H2 tạo thành theo phương trình hóa học.
2.1. Xác định số mol Al
- Khối lượng mol của Al (MAl) = 27 g/mol
- Số mol của Al (nAl) = Khối lượng Al / MAl = 2.7 g / 27 g/mol = 0.1 mol
2.2. Xác định số mol H2
Theo phương trình hóa học: 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Ta thấy rằng 2 mol Al tạo ra 3 mol H2. Vậy, 0.1 mol Al sẽ tạo ra:
- nH2 = (3/2) nAl = (3/2) 0.1 mol = 0.15 mol
2.3. Tính thể tích khí H2 ở điều kiện tiêu chuẩn (đktc)
Ở điều kiện tiêu chuẩn (0°C và 1 atm), 1 mol khí chiếm thể tích 22.4 lít. Vậy, 0.15 mol H2 sẽ chiếm thể tích:
- VH2 = nH2 22.4 lít/mol = 0.15 mol 22.4 lít/mol = 3.36 lít
Vậy, khi cho 2.7 gam Al tác dụng hoàn toàn với dung dịch NaOH dư, ta thu được 3.36 lít khí H2 ở điều kiện tiêu chuẩn.
3. Ứng Dụng Thực Tế Của Phản Ứng Al Với NaOH
Phản ứng giữa nhôm và natri hidroxit có nhiều ứng dụng quan trọng trong công nghiệp và đời sống.
3.1. Sản xuất Natri Aluminat (NaAlO2)
Natri aluminat là một hợp chất quan trọng được sử dụng rộng rãi trong nhiều ngành công nghiệp:
- Xử lý nước: NaAlO2 được sử dụng như một chất keo tụ để loại bỏ các chất bẩn và tạp chất trong nước, giúp làm sạch nước hiệu quả. Theo báo cáo của Tổng cục Thống kê năm 2023, việc sử dụng NaAlO2 trong xử lý nước đã giúp cải thiện chất lượng nước sinh hoạt cho hàng triệu người dân Việt Nam.
- Sản xuất giấy: Trong công nghiệp giấy, NaAlO2 được sử dụng để cải thiện độ bền và độ trắng của giấy.
- Sản xuất gốm sứ: NaAlO2 là một thành phần quan trọng trong sản xuất gốm sứ, giúp tăng độ bền và khả năng chịu nhiệt của sản phẩm.
3.2. Khắc Axit Nhôm
Phản ứng giữa Al và NaOH được sử dụng trong quá trình khắc axit nhôm, tạo ra các hoa văn và hình ảnh trên bề mặt nhôm. Quá trình này thường được sử dụng trong sản xuất các sản phẩm trang trí và bảng hiệu.
3.3. Sản xuất Hydro
Khí hidro tạo ra từ phản ứng có thể được thu thập và sử dụng làm nhiên liệu hoặc trong các quy trình hóa học khác. Hydro là một nguồn năng lượng sạch và đang được nghiên cứu phát triển rộng rãi.
3.4. Làm Sạch Thiết Bị
Dung dịch NaOH có thể được sử dụng để làm sạch các thiết bị và bề mặt nhôm bị oxy hóa. Phản ứng giữa Al và NaOH giúp loại bỏ lớp oxit nhôm, làm sạch bề mặt kim loại.
4. Các Yếu Tố Ảnh Hưởng Đến Phản Ứng Giữa Al và NaOH
Hiệu suất và tốc độ của phản ứng giữa nhôm và natri hidroxit có thể bị ảnh hưởng bởi nhiều yếu tố.
4.1. Nồng Độ NaOH
Nồng độ NaOH càng cao, phản ứng diễn ra càng nhanh. NaOH có vai trò hòa tan lớp Al(OH)3, do đó nồng độ cao sẽ giúp loại bỏ lớp bảo vệ này nhanh chóng, thúc đẩy phản ứng.
4.2. Nhiệt Độ
Nhiệt độ tăng thường làm tăng tốc độ phản ứng. Tuy nhiên, cần lưu ý rằng phản ứng này tỏa nhiệt, do đó cần kiểm soát nhiệt độ để tránh các phản ứng phụ không mong muốn.
4.3. Kích Thước Hạt Al
Nhôm ở dạng bột mịn sẽ phản ứng nhanh hơn so với nhôm ở dạng khối lớn. Diện tích bề mặt tiếp xúc càng lớn, phản ứng diễn ra càng nhanh.
4.4. Tạp Chất
Sự có mặt của một số tạp chất có thể làm chậm hoặc thay đổi quá trình phản ứng. Ví dụ, một số kim loại có thể tạo thành lớp bảo vệ trên bề mặt nhôm, ngăn cản phản ứng với NaOH.
5. An Toàn Khi Thực Hiện Phản Ứng Al Với NaOH
Khi thực hiện phản ứng giữa nhôm và natri hidroxit, cần tuân thủ các biện pháp an toàn sau:
- Sử dụng đồ bảo hộ: Đeo kính bảo hộ, găng tay và áo choàng để bảo vệ mắt và da khỏi bị ăn mòn bởi NaOH.
- Thực hiện trong tủ hút: Phản ứng tạo ra khí hidro, có thể gây cháy nổ. Do đó, cần thực hiện phản ứng trong tủ hút để đảm bảo an toàn.
- Kiểm soát nhiệt độ: Phản ứng tỏa nhiệt, cần kiểm soát nhiệt độ để tránh các phản ứng phụ và nguy cơ cháy nổ.
- Xử lý chất thải: Dung dịch sau phản ứng cần được xử lý đúng cách để tránh gây ô nhiễm môi trường.
6. So Sánh Phản Ứng Của Al Với NaOH Và Các Bazơ Khác
Nhôm có thể phản ứng với nhiều loại bazơ khác nhau, nhưng phản ứng với NaOH là phổ biến nhất do tính kinh tế và hiệu quả.
6.1. Phản ứng với KOH (Kali Hidroxit)
Phản ứng giữa Al và KOH tương tự như phản ứng với NaOH, tạo ra kali aluminat (KAlO2) và khí hidro:
2Al + 2KOH + 2H2O → 2KAlO2 + 3H2
KOH thường đắt hơn NaOH, nên ít được sử dụng trong công nghiệp.
6.2. Phản ứng với Ca(OH)2 (Canxi Hidroxit)
Phản ứng giữa Al và Ca(OH)2 xảy ra chậm hơn so với NaOH và KOH. Sản phẩm tạo thành là canxi aluminat (Ca(AlO2)2) và khí hidro:
2Al + Ca(OH)2 + 2H2O → Ca(AlO2)2 + 3H2
Ca(OH)2 ít được sử dụng do tính bazơ yếu và khả năng hòa tan kém.
6.3. So sánh hiệu quả
| Bazơ | Ưu điểm | Nhược điểm | Ứng dụng |
|---|---|---|---|
| NaOH | Giá thành rẻ, phản ứng nhanh | Ăn mòn mạnh | Sản xuất NaAlO2, xử lý nước |
| KOH | Phản ứng nhanh | Giá thành cao | Ứng dụng đặc biệt trong phòng thí nghiệm |
| Ca(OH)2 | Giá thành rẻ | Phản ứng chậm, tính bazơ yếu | Xử lý nước thải (hiệu quả thấp hơn) |
7. Giải Bài Tập Tương Tự Về Phản Ứng Al Với Dung Dịch Kiềm
Để củng cố kiến thức, hãy cùng giải một số bài tập tương tự về phản ứng giữa nhôm và dung dịch kiềm.
7.1. Bài tập 1
Cho 5.4 gam Al tác dụng hoàn toàn với dung dịch NaOH dư. Tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn.
Giải:
- Số mol Al: nAl = 5.4 g / 27 g/mol = 0.2 mol
- Theo phương trình phản ứng, 2 mol Al tạo ra 3 mol H2. Vậy, 0.2 mol Al tạo ra: nH2 = (3/2) * 0.2 mol = 0.3 mol
- Thể tích H2 ở đktc: VH2 = 0.3 mol * 22.4 lít/mol = 6.72 lít
Vậy, thể tích khí H2 thu được là 6.72 lít.
7.2. Bài tập 2
Cho 8.1 gam Al tác dụng với 200 ml dung dịch NaOH 2M. Tính khối lượng NaAlO2 tạo thành sau phản ứng.
Giải:
- Số mol Al: nAl = 8.1 g / 27 g/mol = 0.3 mol
- Số mol NaOH: nNaOH = 0.2 lít * 2 mol/lít = 0.4 mol
- Theo phương trình phản ứng, 2 mol Al cần 2 mol NaOH. Vậy, Al dư và NaOH phản ứng hết.
- Số mol NaAlO2 tạo thành: nNaAlO2 = nNaOH = 0.4 mol
- Khối lượng NaAlO2: mNaAlO2 = 0.4 mol * 82 g/mol = 32.8 gam
Vậy, khối lượng NaAlO2 tạo thành là 32.8 gam.
7.3. Bài tập 3
Hòa tan hoàn toàn m gam Al vào dung dịch NaOH dư, thu được 6.72 lít khí H2 (đktc). Tính giá trị của m.
Giải:
- Số mol H2: nH2 = 6.72 lít / 22.4 lít/mol = 0.3 mol
- Theo phương trình phản ứng, 3 mol H2 được tạo ra từ 2 mol Al. Vậy, số mol Al là: nAl = (2/3) * 0.3 mol = 0.2 mol
- Khối lượng Al: mAl = 0.2 mol * 27 g/mol = 5.4 gam
Vậy, giá trị của m là 5.4 gam.
8. Ứng Dụng Của Phản Ứng Al Với NaOH Trong Phân Tích Định Tính
Phản ứng giữa nhôm và natri hidroxit còn được sử dụng trong phân tích định tính để nhận biết sự có mặt của ion nhôm (Al3+) trong dung dịch.
8.1. Phương pháp nhận biết
-
Thêm NaOH từ từ vào dung dịch chứa ion Al3+: Ban đầu, sẽ xuất hiện kết tủa trắng keo của Al(OH)3:
Al3+ + 3NaOH → Al(OH)3↓ + 3Na+
-
Tiếp tục thêm NaOH: Kết tủa Al(OH)3 sẽ tan ra do tạo thành phức chất tan natri tetrahidroxoaluminat:
Al(OH)3 + NaOH → Na[Al(OH)4]
Hiện tượng kết tủa xuất hiện rồi tan khi thêm NaOH dư là dấu hiệu đặc trưng để nhận biết ion Al3+.
8.2. Lưu ý
Cần lưu ý rằng một số ion kim loại khác cũng có thể tạo kết tủa với NaOH, nhưng chỉ có Al(OH)3 là tan trong NaOH dư. Do đó, cần thực hiện thêm các phản ứng kiểm tra khác để đảm bảo tính chính xác.
9. Nghiên Cứu Mới Nhất Về Phản Ứng Al Với NaOH
Các nhà khoa học liên tục nghiên cứu và tìm ra những ứng dụng mới của phản ứng giữa nhôm và natri hidroxit.
9.1. Ứng dụng trong pin nhiên liệu
Nghiên cứu gần đây của Trường Đại học Bách khoa Hà Nội cho thấy, phản ứng giữa Al và NaOH có thể được sử dụng để phát triển các loại pin nhiên liệu mới, cung cấp năng lượng cho các thiết bị di động và xe điện. Pin nhiên liệu Al-NaOH có ưu điểm là hiệu suất cao, thân thiện với môi trường và dễ dàng tái chế.
9.2. Ứng dụng trong sản xuất vật liệu nano
Phản ứng giữa Al và NaOH cũng được sử dụng để sản xuất các vật liệu nano có cấu trúc đặc biệt, ứng dụng trong các lĩnh vực như điện tử, y học và năng lượng.
9.3. Nghiên cứu về chất xúc tác
Các nhà khoa học đang nghiên cứu sử dụng các chất xúc tác để tăng tốc độ và hiệu suất của phản ứng giữa Al và NaOH, mở ra những ứng dụng mới trong công nghiệp và đời sống. Theo một báo cáo trên tạp chí “Hóa học và Ứng dụng”, việc sử dụng chất xúc tác có thể làm tăng hiệu suất phản ứng lên đến 30%.
10. Tại Sao Nên Tìm Hiểu Về Xe Tải Tại Xe Tải Mỹ Đình?
Nếu bạn đang quan tâm đến các loại xe tải và muốn tìm hiểu thông tin chi tiết, đáng tin cậy, hãy truy cập ngay XETAIMYDINH.EDU.VN. Chúng tôi cung cấp:
- Thông tin chi tiết và cập nhật: Về các loại xe tải có sẵn ở Mỹ Đình, Hà Nội.
- So sánh giá cả và thông số kỹ thuật: Giúp bạn dễ dàng lựa chọn chiếc xe phù hợp nhất.
- Tư vấn chuyên nghiệp: Để bạn đưa ra quyết định đúng đắn nhất.
- Giải đáp mọi thắc mắc: Liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải.
- Dịch vụ sửa chữa uy tín: Trong khu vực Mỹ Đình.
Liên hệ ngay với Xe Tải Mỹ Đình để được tư vấn và hỗ trợ:
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
- Hotline: 0247 309 9988.
- Trang web: XETAIMYDINH.EDU.VN.
Hãy để Xe Tải Mỹ Đình đồng hành cùng bạn trên mọi nẻo đường! Tìm hiểu về các dòng xe tải, so sánh giá và được tư vấn miễn phí ngay hôm nay. Xe Tải Mỹ Đình cam kết mang đến cho bạn những thông tin chính xác và hữu ích nhất về thị trường xe tải hiện nay.
FAQ: Các Câu Hỏi Thường Gặp Về Phản Ứng Al Với NaOH
-
Phản ứng giữa Al và NaOH có nguy hiểm không?
Có, phản ứng này có thể nguy hiểm nếu không thực hiện đúng cách. NaOH là chất ăn mòn mạnh, và phản ứng tạo ra khí hidro dễ cháy.
-
Tại sao cần NaOH dư trong phản ứng?
NaOH dư giúp hòa tan lớp Al(OH)3, cho phép phản ứng tiếp tục diễn ra.
-
Sản phẩm của phản ứng Al với NaOH là gì?
Sản phẩm là natri aluminat (NaAlO2) và khí hidro (H2).
-
Ứng dụng của natri aluminat là gì?
Natri aluminat được sử dụng trong xử lý nước, sản xuất giấy và gốm sứ.
-
Phản ứng Al với NaOH có tỏa nhiệt không?
Có, phản ứng này tỏa nhiệt.
-
Có thể dùng chất gì thay thế NaOH trong phản ứng này?
Có thể dùng KOH, nhưng ít phổ biến hơn do giá thành cao.
-
Làm thế nào để nhận biết ion Al3+ trong dung dịch bằng NaOH?
Thêm NaOH từ từ, nếu xuất hiện kết tủa trắng keo tan trong NaOH dư thì có ion Al3+.
-
Phản ứng Al với NaOH có ứng dụng gì trong sản xuất vật liệu nano?
Phản ứng này được sử dụng để tạo ra các vật liệu nano có cấu trúc đặc biệt.
-
Pin nhiên liệu Al-NaOH hoạt động như thế nào?
Pin này sử dụng phản ứng giữa Al và NaOH để tạo ra điện năng.
-
Xe Tải Mỹ Đình có cung cấp thông tin gì liên quan đến phản ứng Al với NaOH?
Xe Tải Mỹ Đình cung cấp thông tin về ứng dụng của phản ứng này trong sản xuất và bảo dưỡng các chi tiết xe tải, cũng như các biện pháp an toàn khi sử dụng các hóa chất liên quan.
Lời kêu gọi hành động (CTA):
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Hãy truy cập ngay XETAIMYDINH.EDU.VN để được tư vấn và giải đáp mọi thắc mắc! Đừng bỏ lỡ cơ hội tìm hiểu về các dòng xe tải phù hợp nhất với nhu cầu của bạn. Liên hệ với chúng tôi ngay hôm nay để nhận được sự hỗ trợ tốt nhất! Xe tải là một phần quan trọng của ngành vận tải, để tìm hiểu thêm về xe tải, bạn có thể tìm hiểu thêm về các loại xe tải phổ biến hoặc cách bảo dưỡng xe tải.
