Ch3oh H2so4 140 là một chủ đề phức tạp trong hóa học, đặc biệt liên quan đến phản ứng tạo ete. Bài viết này của Xe Tải Mỹ Đình sẽ cung cấp thông tin chi tiết về phản ứng này, các ứng dụng thực tế và những lưu ý quan trọng để đảm bảo an toàn và hiệu quả. Cùng khám phá cách tối ưu hóa quá trình này và những kiến thức chuyên sâu liên quan đến lĩnh vực hóa học hữu cơ nhé.
1. CH3OH H2SO4 140 Là Gì?
CH3OH H2SO4 140 đề cập đến phản ứng hóa học trong đó methanol (CH3OH) được xử lý với axit sulfuric (H2SO4) ở nhiệt độ khoảng 140°C để tạo thành dimethyl ether. Đây là một phản ứng dehydration (loại nước) xúc tác bởi axit.
1.1. Phản Ứng Hóa Học Cơ Bản
Phản ứng tổng quát có thể được biểu diễn như sau:
2 CH3OH → CH3OCH3 + H2O
Trong điều kiện có axit sulfuric (H2SO4) làm chất xúc tác và nhiệt độ được duy trì ở khoảng 140°C, hai phân tử methanol sẽ kết hợp với nhau, loại bỏ một phân tử nước để tạo thành dimethyl ether (DME).
1.2. Vai Trò Của Các Chất Trong Phản Ứng
- Methanol (CH3OH): Là chất phản ứng chính, nguồn cung cấp các nhóm methyl để tạo thành dimethyl ether.
- Axit Sunfuric (H2SO4): Đóng vai trò là chất xúc tác. Axit sulfuric giúp proton hóa nhóm hydroxyl (-OH) của methanol, biến nó thành một nhóm rời tốt hơn (nước), từ đó tạo điều kiện cho phản ứng SN2 xảy ra.
- Nhiệt Độ (140°C): Nhiệt độ này cung cấp năng lượng hoạt hóa cần thiết để phản ứng xảy ra với tốc độ hợp lý. Nếu nhiệt độ quá thấp, phản ứng sẽ diễn ra rất chậm. Nếu nhiệt độ quá cao, có thể xảy ra các phản ứng phụ không mong muốn, như tạo thành các sản phẩm khác hoặc phân hủy chất phản ứng.
1.3. Cơ Chế Phản Ứng Chi Tiết
Phản ứng xảy ra theo ba bước chính:
- Proton Hóa Methanol: Axit sulfuric proton hóa nhóm hydroxyl của một phân tử methanol, tạo thành ion methyl oxonium (CH3OH2+).
- Tấn Công Nucleophile: Một phân tử methanol khác tấn công carbon của ion methyl oxonium, loại bỏ nước và tạo thành một sản phẩm trung gian.
- Deproton Hóa: Sản phẩm trung gian mất một proton để tạo thành dimethyl ether.
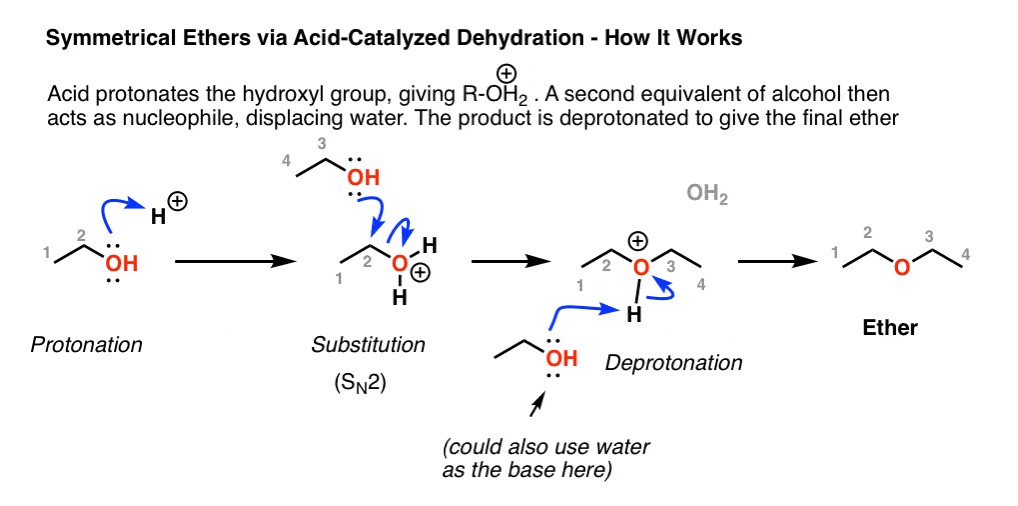 Cơ chế phản ứng tạo dimethyl ether từ methanol và axit sulfuric
Cơ chế phản ứng tạo dimethyl ether từ methanol và axit sulfuric
1.4. Các Yếu Tố Ảnh Hưởng Đến Hiệu Suất Phản Ứng
- Nhiệt Độ: Nhiệt độ tối ưu là khoảng 140°C. Nhiệt độ quá thấp làm chậm phản ứng, trong khi nhiệt độ quá cao có thể dẫn đến các phản ứng phụ.
- Nồng Độ Axit: Nồng độ axit sulfuric cần được kiểm soát cẩn thận. Nồng độ quá cao có thể gây ra sự phân hủy methanol, trong khi nồng độ quá thấp có thể làm giảm tốc độ phản ứng.
- Thời Gian Phản Ứng: Thời gian phản ứng cần đủ để đạt được hiệu suất tối đa, nhưng không quá dài để tránh các phản ứng phụ.
- Tỉ Lệ Mol: Tỉ lệ mol giữa methanol và axit sulfuric cũng ảnh hưởng đến hiệu suất. Tỉ lệ tối ưu cần được xác định để đảm bảo phản ứng diễn ra hiệu quả nhất.
1.5. Ưu Điểm Và Nhược Điểm Của Phương Pháp Này
- Ưu Điểm:
- Nguyên liệu đầu vào (methanol) tương đối rẻ và dễ kiếm.
- Phản ứng đơn giản, dễ thực hiện ở quy mô công nghiệp.
- Nhược Điểm:
- Cần kiểm soát chặt chẽ nhiệt độ và nồng độ axit để tránh các phản ứng phụ.
- Hiệu suất có thể bị ảnh hưởng bởi các yếu tố như thời gian phản ứng và tỉ lệ mol.
1.6. So Sánh Với Các Phương Pháp Điều Chế Ete Khác
So với các phương pháp điều chế ete khác như tổng hợp Williamson, phương pháp sử dụng CH3OH H2SO4 140 có những ưu điểm và nhược điểm riêng. Tổng hợp Williamson cho phép điều chế các ete không đối xứng, trong khi phương pháp này chỉ thích hợp cho việc điều chế ete đối xứng như dimethyl ether. Tuy nhiên, phương pháp sử dụng CH3OH H2SO4 140 thường đơn giản và kinh tế hơn cho việc sản xuất dimethyl ether ở quy mô lớn.
2. Ứng Dụng Quan Trọng Của Dimethyl Ether (DME)
Dimethyl ether (DME) là một hợp chất hóa học có nhiều ứng dụng quan trọng trong các ngành công nghiệp khác nhau. Dưới đây là một số ứng dụng chính của DME:
2.1. Nhiên Liệu
- Nhiên Liệu Thay Thế: DME có thể được sử dụng làm nhiên liệu thay thế cho dầu diesel và LPG (khí dầu mỏ hóa lỏng). DME có số cetane cao, giúp động cơ diesel khởi động dễ dàng và hoạt động êm ái hơn.
- Giảm Phát Thải: Khi sử dụng làm nhiên liệu, DME tạo ra ít khí thải độc hại hơn so với dầu diesel, bao gồm ít hạt vật chất (PM) và oxit nitơ (NOx). Điều này giúp cải thiện chất lượng không khí và giảm tác động tiêu cực đến môi trường. Theo một báo cáo của Bộ Tài nguyên và Môi trường, việc sử dụng DME có thể giảm tới 90% lượng PM và 40% lượng NOx so với dầu diesel thông thường.
- Ứng Dụng Trong Giao Thông Vận Tải: DME có thể được sử dụng trong các phương tiện giao thông như xe buýt, xe tải và tàu thuyền. Một số quốc gia đã bắt đầu thử nghiệm và triển khai sử dụng DME trong giao thông công cộng để giảm ô nhiễm không khí.
2.2. Chất Đẩy Trong Bình Xịt
- Chất Đẩy An Toàn: DME được sử dụng làm chất đẩy trong các bình xịt (aerosol) cho các sản phẩm như keo xịt tóc, sơn xịt và thuốc trừ sâu. DME là một chất đẩy an toàn và không gây hại cho tầng ozone, thay thế cho các chất đẩy chứa CFC (chlorofluorocarbon) đã bị cấm sử dụng.
- Độ Ổn Định Cao: DME có độ ổn định hóa học cao và không phản ứng với các thành phần khác trong bình xịt, đảm bảo chất lượng và hiệu quả của sản phẩm.
2.3. Dung Môi
- Dung Môi Hữu Ích: DME là một dung môi hữu ích trong nhiều ứng dụng công nghiệp và phòng thí nghiệm. Nó có khả năng hòa tan nhiều loại hợp chất hữu cơ và được sử dụng trong các quá trình chiết xuất, phản ứng và làm sạch.
- Ứng Dụng Trong Sản Xuất Polyme: DME được sử dụng trong sản xuất một số loại polyme, chẳng hạn như polyuretan và polyolefin. Nó giúp kiểm soát quá trình trùng hợp và cải thiện tính chất của sản phẩm cuối cùng.
2.4. Hóa Chất Trung Gian
- Sản Xuất Olefin: DME có thể được sử dụng làm nguyên liệu để sản xuất olefin (như ethylene và propylene) thông qua quá trình chuyển hóa DME thành olefin (DTO). Olefin là các hóa chất cơ bản quan trọng trong ngành công nghiệp hóa chất, được sử dụng để sản xuất nhựa, sợi và nhiều sản phẩm khác.
- Sản Xuất Metyl Axetat: DME có thể phản ứng với cacbon monoxit (CO) để tạo thành metyl axetat, một dung môi và hóa chất trung gian quan trọng.
2.5. Ứng Dụng Trong Y Tế
- Chất Làm Lạnh: DME có thể được sử dụng làm chất làm lạnh trong các thiết bị y tế, chẳng hạn như trong các thiết bị làm lạnh nhanh để bảo quản mẫu sinh học.
- Chất Mang Trong Dược Phẩm: DME có thể được sử dụng làm chất mang trong một số loại thuốc xịt, giúp phân tán thuốc đều và nhanh chóng.
2.6. Ứng Dụng Tiềm Năng Khác
- Sản Xuất Điện: DME có thể được sử dụng trong các tuabin khí để sản xuất điện. Nó có thể giúp giảm phát thải và cải thiện hiệu suất của tuabin.
- Chất Tạo Bọt: DME có thể được sử dụng làm chất tạo bọt trong sản xuất vật liệu cách nhiệt và các sản phẩm khác.
3. An Toàn Và Các Lưu Ý Khi Sử Dụng CH3OH H2SO4 140
Khi làm việc với CH3OH H2SO4 140, việc tuân thủ các biện pháp an toàn là vô cùng quan trọng để đảm bảo an toàn cho bản thân và môi trường xung quanh. Dưới đây là những lưu ý quan trọng cần tuân thủ:
3.1. Đeo Trang Bị Bảo Hộ Cá Nhân (PPE)
- Kính Bảo Hộ: Luôn đeo kính bảo hộ để bảo vệ mắt khỏi bị văng hóa chất.
- Găng Tay: Sử dụng găng tay chịu hóa chất để bảo vệ da tay khỏi tiếp xúc trực tiếp với methanol và axit sulfuric.
- Áo Choàng Phòng Thí Nghiệm: Mặc áo choàng phòng thí nghiệm để bảo vệ quần áo và da khỏi bị hóa chất ăn mòn.
- Mặt Nạ Phòng Độc: Nếu làm việc trong môi trường có nồng độ hơi methanol cao, hãy sử dụng mặt nạ phòng độc để tránh hít phải hơi độc.
3.2. Thực Hiện Phản Ứng Trong Tủ Hút
- Thông Gió Tốt: Phản ứng nên được thực hiện trong tủ hút để đảm bảo thông gió tốt và loại bỏ hơi methanol độc hại.
- Kiểm Tra Lưu Lượng Khí: Đảm bảo rằng tủ hút hoạt động hiệu quả và lưu lượng khí đủ để loại bỏ hơi hóa chất.
3.3. Kiểm Soát Nhiệt Độ Cẩn Thận
- Sử Dụng Thiết Bị Kiểm Soát Nhiệt Độ: Sử dụng các thiết bị kiểm soát nhiệt độ chính xác để duy trì nhiệt độ phản ứng ở khoảng 140°C.
- Tránh Quá Nhiệt: Quá nhiệt có thể dẫn đến các phản ứng phụ không mong muốn và tạo ra các sản phẩm phân hủy độc hại.
3.4. Xử Lý Axit Sunfuric Cẩn Thận
- Pha Loãng Axit Đúng Cách: Khi pha loãng axit sulfuric, luôn thêm từ từ axit vào nước, không bao giờ thêm nước vào axit. Quá trình này tỏa nhiệt mạnh và có thể gây bắn axit nếu thực hiện không đúng cách.
- Tránh Tiếp Xúc Với Da Và Mắt: Axit sulfuric là một chất ăn mòn mạnh, có thể gây bỏng nặng nếu tiếp xúc với da và mắt. Nếu bị axit bắn vào, rửa ngay lập tức với nhiều nước và tìm kiếm sự chăm sóc y tế.
3.5. Lưu Trữ Hóa Chất Đúng Cách
- Lưu Trữ Trong Chai Đựng Thích Hợp: Lưu trữ methanol và axit sulfuric trong các chai đựng chịu hóa chất, được dán nhãn rõ ràng.
- Tránh Xa Các Chất Không Tương Thích: Lưu trữ hóa chất ở nơi khô ráo, thoáng mát, tránh xa các chất không tương thích như chất oxy hóa mạnh, kim loại kiềm và các chất dễ cháy.
3.6. Xử Lý Sự Cố
- Tràn Hóa Chất: Nếu hóa chất bị tràn, hãy sử dụng vật liệu thấm hút (như cát hoặc giấy thấm) để lau sạch. Sau đó, xử lý vật liệu thấm hút theo quy định về xử lý chất thải nguy hại.
- Tiếp Xúc Với Da Hoặc Mắt: Nếu hóa chất tiếp xúc với da hoặc mắt, rửa ngay lập tức với nhiều nước trong ít nhất 15 phút và tìm kiếm sự chăm sóc y tế.
- Hỏa Hoạn: Methanol là một chất dễ cháy. Trong trường hợp hỏa hoạn, sử dụng bình chữa cháy chứa bọt, CO2 hoặc bột khô để dập lửa.
3.7. Tuân Thủ Quy Định Về An Toàn Lao Động
- Đọc Và Hiểu MSDS: Đọc và hiểu rõ Bảng Dữ Liệu An Toàn Hóa Chất (MSDS) của methanol và axit sulfuric trước khi làm việc.
- Tuân Thủ Quy Trình An Toàn: Tuân thủ các quy trình an toàn lao động của phòng thí nghiệm hoặc nhà máy.
- Đào Tạo An Toàn: Tham gia các khóa đào tạo về an toàn hóa chất để nắm vững các biện pháp phòng ngừa và ứng phó sự cố.
3.8. Bảo Vệ Môi Trường
- Xử Lý Chất Thải Đúng Quy Định: Xử lý chất thải hóa học theo quy định của pháp luật về bảo vệ môi trường. Không đổ hóa chất xuống cống rãnh hoặc thải ra môi trường.
- Giảm Thiểu Lượng Hóa Chất Sử Dụng: Sử dụng lượng hóa chất vừa đủ để thực hiện phản ứng, tránh lãng phí và giảm thiểu lượng chất thải phát sinh.
3.9. Các Lưu Ý Khác
- Không Ăn Uống Hoặc Hút Thuốc: Không ăn uống hoặc hút thuốc trong khu vực làm việc với hóa chất.
- Giữ Khu Vực Làm Việc Sạch Sẽ: Giữ khu vực làm việc sạch sẽ và gọn gàng để tránh tai nạn.
- Báo Cáo Sự Cố: Báo cáo ngay lập tức mọi sự cố hoặc tai nạn cho người quản lý hoặc người có trách nhiệm.
4. Tối Ưu Hóa Phản Ứng CH3OH H2SO4 140 Để Đạt Hiệu Quả Cao
Để đạt được hiệu quả cao trong phản ứng CH3OH H2SO4 140, việc tối ưu hóa các yếu tố ảnh hưởng đến phản ứng là rất quan trọng. Dưới đây là các bước và yếu tố cần xem xét để tối ưu hóa phản ứng:
4.1. Kiểm Soát Nhiệt Độ Chính Xác
- Sử Dụng Bộ Điều Nhiệt: Sử dụng bộ điều nhiệt chính xác để duy trì nhiệt độ phản ứng ở khoảng 140°C. Nhiệt độ này là tối ưu để cân bằng giữa tốc độ phản ứng và giảm thiểu các phản ứng phụ.
- Theo Dõi Nhiệt Độ Liên Tục: Theo dõi nhiệt độ phản ứng liên tục bằng nhiệt kế hoặc cảm biến nhiệt độ để đảm bảo nhiệt độ luôn ổn định.
- Tránh Dao Động Nhiệt Độ: Tránh dao động nhiệt độ lớn, vì điều này có thể ảnh hưởng đến hiệu suất phản ứng và tạo ra các sản phẩm phụ không mong muốn.
4.2. Điều Chỉnh Nồng Độ Axit Sunfuric
- Xác Định Nồng Độ Tối Ưu: Nồng độ axit sulfuric cần được xác định tối ưu dựa trên quy mô phản ứng và thiết bị sử dụng. Nồng độ quá cao có thể gây phân hủy methanol, trong khi nồng độ quá thấp có thể làm chậm phản ứng.
- Sử Dụng Axit Có Độ Tinh Khiết Cao: Sử dụng axit sulfuric có độ tinh khiết cao để tránh các tạp chất ảnh hưởng đến phản ứng.
- Kiểm Tra Định Kỳ: Kiểm tra nồng độ axit định kỳ để đảm bảo nồng độ không bị thay đổi trong quá trình phản ứng.
4.3. Tối Ưu Hóa Thời Gian Phản Ứng
- Thực Hiện Thử Nghiệm Thời Gian: Thực hiện các thử nghiệm thời gian để xác định thời gian phản ứng tối ưu. Thời gian phản ứng quá ngắn có thể không đủ để đạt được hiệu suất cao, trong khi thời gian quá dài có thể dẫn đến các phản ứng phụ.
- Theo Dõi Tiến Trình Phản Ứng: Theo dõi tiến trình phản ứng bằng các phương pháp phân tích như sắc ký khí (GC) hoặc sắc ký lỏng (HPLC) để xác định thời điểm phản ứng kết thúc.
4.4. Sử Dụng Chất Xúc Tác Hỗ Trợ (Nếu Cần)
- Nghiên Cứu Các Chất Xúc Tác Hỗ Trợ: Nghiên cứu các chất xúc tác hỗ trợ có thể cải thiện hiệu suất phản ứng. Ví dụ, một số loại zeolit hoặc oxit kim loại có thể được sử dụng để tăng cường hoạt tính xúc tác của axit sulfuric.
- Thử Nghiệm Với Các Chất Xúc Tác Khác Nhau: Thử nghiệm với các chất xúc tác hỗ trợ khác nhau để tìm ra chất xúc tác phù hợp nhất với điều kiện phản ứng.
4.5. Kiểm Soát Tỉ Lệ Mol Của Các Chất Phản Ứng
- Xác Định Tỉ Lệ Mol Tối Ưu: Xác định tỉ lệ mol tối ưu giữa methanol và axit sulfuric. Tỉ lệ này có thể ảnh hưởng đến hiệu suất phản ứng và lượng sản phẩm phụ tạo ra.
- Sử Dụng Tỉ Lệ Mol Chính Xác: Sử dụng tỉ lệ mol chính xác trong quá trình phản ứng để đảm bảo hiệu suất cao nhất.
4.6. Loại Bỏ Nước Trong Quá Trình Phản Ứng
- Sử Dụng Chất Hút Ẩm: Sử dụng chất hút ẩm như分子筛 để loại bỏ nước tạo ra trong quá trình phản ứng. Việc loại bỏ nước có thể giúp tăng tốc độ phản ứng và cải thiện hiệu suất.
- Sử Dụng Thiết Bị Tách Nước: Sử dụng thiết bị tách nước như bình Dean-Stark để loại bỏ nước liên tục trong quá trình phản ứng.
4.7. Khuấy Trộn Hiệu Quả
- Đảm Bảo Khuấy Trộn Đều: Đảm bảo khuấy trộn đều các chất phản ứng để tăng cường tiếp xúc giữa methanol và axit sulfuric.
- Sử Dụng Máy Khuấy Phù Hợp: Sử dụng máy khuấy có tốc độ và công suất phù hợp với quy mô phản ứng.
4.8. Sử Dụng Thiết Bị Phản Ứng Phù Hợp
- Chọn Thiết Bị Chịu Hóa Chất: Chọn thiết bị phản ứng được làm từ vật liệu chịu hóa chất, chẳng hạn như thủy tinh borosilicate hoặc thép không gỉ.
- Thiết Kế Thiết Bị Phản Ứng Tối Ưu: Thiết kế thiết bị phản ứng sao cho đảm bảo kiểm soát nhiệt độ tốt, khuấy trộn hiệu quả và dễ dàng thu hồi sản phẩm.
4.9. Thu Hồi Và Tái Sử Dụng Methanol
- Thu Hồi Methanol Dư: Thu hồi methanol dư sau phản ứng để tái sử dụng. Điều này giúp giảm chi phí và bảo vệ môi trường.
- Sử Dụng Phương Pháp Chưng Cất: Sử dụng phương pháp chưng cất để tách methanol khỏi các sản phẩm phụ và tạp chất.
4.10. Phân Tích Và Đánh Giá Hiệu Quả
- Phân Tích Sản Phẩm: Phân tích sản phẩm bằng các phương pháp như GC, HPLC hoặc NMR để xác định thành phần và độ tinh khiết.
- Đánh Giá Hiệu Suất: Đánh giá hiệu suất phản ứng dựa trên lượng sản phẩm thu được và lượng chất phản ứng đã sử dụng.
- Điều Chỉnh Các Yếu Tố Phản Ứng: Dựa trên kết quả phân tích và đánh giá, điều chỉnh các yếu tố phản ứng để đạt được hiệu quả cao nhất.
4.11. Các Nghiên Cứu Và Cải Tiến Liên Tục
- Theo Dõi Các Nghiên Cứu Mới: Theo dõi các nghiên cứu mới về phản ứng CH3OH H2SO4 140 để áp dụng các cải tiến mới nhất.
- Thử Nghiệm Các Điều Kiện Phản Ứng Khác Nhau: Thử nghiệm các điều kiện phản ứng khác nhau để tìm ra điều kiện tối ưu cho từng quy mô và thiết bị phản ứng.
Bằng cách tuân thủ các biện pháp trên, bạn có thể tối ưu hóa phản ứng CH3OH H2SO4 140 để đạt được hiệu quả cao, giảm thiểu chi phí và bảo vệ môi trường.
5. Nghiên Cứu Về Phản Ứng CH3OH H2SO4 140 Trong Công Nghiệp
Phản ứng CH3OH H2SO4 140 được sử dụng rộng rãi trong công nghiệp để sản xuất dimethyl ether (DME). Dưới đây là một số nghiên cứu và ứng dụng thực tế trong công nghiệp:
5.1. Sản Xuất Dimethyl Ether (DME) Quy Mô Lớn
- Ứng Dụng Trong Công Nghiệp Hóa Chất: DME được sản xuất quy mô lớn để sử dụng làm nhiên liệu, chất đẩy trong bình xịt, dung môi và hóa chất trung gian.
- Các Nhà Máy Sản Xuất DME: Nhiều nhà máy hóa chất trên thế giới sử dụng phản ứng CH3OH H2SO4 140 để sản xuất DME. Các nhà máy này thường tối ưu hóa các điều kiện phản ứng để đạt được hiệu suất cao và giảm chi phí sản xuất.
5.2. Nghiên Cứu Về Chất Xúc Tác Heterogeneous
- Sử Dụng Zeolit Làm Chất Xúc Tác: Nhiều nghiên cứu tập trung vào việc sử dụng zeolit làm chất xúc tác heterogeneous cho phản ứng CH3OH H2SO4 140. Zeolit có diện tích bề mặt lớn và khả năng điều chỉnh tính axit, giúp tăng cường hoạt tính xúc tác và hiệu suất phản ứng.
- Ưu Điểm Của Chất Xúc Tác Heterogeneous: Chất xúc tác heterogeneous dễ dàng tách khỏi sản phẩm sau phản ứng, có thể tái sử dụng và giảm thiểu lượng chất thải hóa học.
5.3. Nghiên Cứu Về Các Điều Kiện Phản Ứng Tối Ưu
- Ảnh Hưởng Của Nhiệt Độ Và Áp Suất: Các nghiên cứu đã chỉ ra rằng nhiệt độ và áp suất có ảnh hưởng lớn đến hiệu suất phản ứng CH3OH H2SO4 140. Nhiệt độ tối ưu thường nằm trong khoảng 130-150°C, và áp suất cao có thể giúp tăng tốc độ phản ứng.
- Tối Ưu Hóa Tỉ Lệ Mol: Các nghiên cứu cũng tập trung vào việc tối ưu hóa tỉ lệ mol giữa methanol và axit sulfuric để đạt được hiệu suất cao nhất.
5.4. Nghiên Cứu Về Các Phương Pháp Tách DME
- Chưng Cất: Chưng cất là phương pháp phổ biến để tách DME khỏi các sản phẩm phụ và tạp chất.
- Hấp Thụ: Hấp thụ bằng dung môi thích hợp cũng được sử dụng để tách DME.
- Màng Lọc: Màng lọc có thể được sử dụng để tách DME khỏi các hỗn hợp khí.
5.5. Ứng Dụng Trong Sản Xuất Nhiên Liệu DME
- DME Làm Nhiên Liệu Thay Thế: DME được sử dụng làm nhiên liệu thay thế cho dầu diesel và LPG. Nó có số cetane cao, giúp động cơ diesel khởi động dễ dàng và hoạt động êm ái hơn.
- Giảm Phát Thải: DME tạo ra ít khí thải độc hại hơn so với dầu diesel, bao gồm ít hạt vật chất (PM) và oxit nitơ (NOx).
- Các Dự Án Sản Xuất DME: Nhiều dự án trên thế giới đang tập trung vào việc sản xuất DME từ các nguồn tái tạo như sinh khối và khí sinh học.
5.6. Nghiên Cứu Về Tính Bền Vững Của Quá Trình Sản Xuất DME
- Sử Dụng Nguồn Nguyên Liệu Tái Tạo: Các nghiên cứu tập trung vào việc sử dụng nguồn nguyên liệu tái tạo như sinh khối và khí sinh học để sản xuất methanol, từ đó giảm thiểu tác động tiêu cực đến môi trường.
- Giảm Lượng Chất Thải: Các nghiên cứu cũng tập trung vào việc giảm lượng chất thải và tái sử dụng các chất xúc tác và dung môi để làm cho quá trình sản xuất DME bền vững hơn.
5.7. Các Công Ty Và Tổ Chức Nghiên Cứu
- Các Công Ty Hóa Chất: Nhiều công ty hóa chất lớn trên thế giới đang tiến hành nghiên cứu và phát triển các quy trình sản xuất DME hiệu quả và bền vững.
- Các Trường Đại Học Và Viện Nghiên Cứu: Nhiều trường đại học và viện nghiên cứu cũng tham gia vào các dự án nghiên cứu về phản ứng CH3OH H2SO4 140 và các ứng dụng của DME.
5.8. Các Bằng Sáng Chế Liên Quan
- Bằng Sáng Chế Về Chất Xúc Tác: Có nhiều bằng sáng chế liên quan đến việc sử dụng các chất xúc tác mới và cải tiến cho phản ứng CH3OH H2SO4 140.
- Bằng Sáng Chế Về Quy Trình Sản Xuất DME: Có nhiều bằng sáng chế liên quan đến các quy trình sản xuất DME hiệu quả và bền vững.
6. FAQ Về CH3OH H2SO4 140
6.1. CH3OH H2SO4 140 là gì?
CH3OH H2SO4 140 là phản ứng hóa học giữa methanol (CH3OH) và axit sulfuric (H2SO4) ở nhiệt độ 140°C để tạo ra dimethyl ether (DME).
6.2. Tại sao cần sử dụng axit sulfuric trong phản ứng này?
Axit sulfuric đóng vai trò là chất xúc tác, giúp proton hóa nhóm hydroxyl của methanol, tạo điều kiện cho phản ứng loại nước và hình thành DME.
6.3. Nhiệt độ 140°C có vai trò gì trong phản ứng?
Nhiệt độ 140°C cung cấp năng lượng hoạt hóa cần thiết để phản ứng xảy ra với tốc độ hợp lý, đồng thời giúp cân bằng giữa tốc độ phản ứng và giảm thiểu các phản ứng phụ.
6.4. Dimethyl ether (DME) được ứng dụng để làm gì?
DME được sử dụng làm nhiên liệu thay thế, chất đẩy trong bình xịt, dung môi, hóa chất trung gian và trong một số ứng dụng y tế.
6.5. Làm thế nào để tối ưu hóa phản ứng CH3OH H2SO4 140?
Để tối ưu hóa phản ứng, cần kiểm soát nhiệt độ chính xác, điều chỉnh nồng độ axit sulfuric, tối ưu hóa thời gian phản ứng, sử dụng chất xúc tác hỗ trợ (nếu cần), kiểm soát tỉ lệ mol của các chất phản ứng và loại bỏ nước trong quá trình phản ứng.
6.6. Những biện pháp an toàn nào cần tuân thủ khi làm việc với CH3OH H2SO4 140?
Cần đeo trang bị bảo hộ cá nhân (PPE), thực hiện phản ứng trong tủ hút, kiểm soát nhiệt độ cẩn thận, xử lý axit sulfuric cẩn thận, lưu trữ hóa chất đúng cách, xử lý sự cố và tuân thủ quy định về an toàn lao động.
6.7. Có thể tái sử dụng methanol sau phản ứng không?
Có, methanol dư sau phản ứng có thể được thu hồi và tái sử dụng bằng phương pháp chưng cất.
6.8. Phản ứng CH3OH H2SO4 140 có thân thiện với môi trường không?
Để làm cho phản ứng thân thiện với môi trường hơn, cần sử dụng nguồn nguyên liệu tái tạo, giảm lượng chất thải và tái sử dụng các chất xúc tác và dung môi.
6.9. Chất xúc tác heterogeneous có ưu điểm gì so với chất xúc tác homogeneous trong phản ứng này?
Chất xúc tác heterogeneous dễ dàng tách khỏi sản phẩm sau phản ứng, có thể tái sử dụng và giảm thiểu lượng chất thải hóa học.
6.10. Có những nghiên cứu nào về phản ứng CH3OH H2SO4 140 trong công nghiệp?
Các nghiên cứu tập trung vào việc sử dụng zeolit làm chất xúc tác, tối ưu hóa các điều kiện phản ứng, nghiên cứu các phương pháp tách DME và ứng dụng trong sản xuất nhiên liệu DME.
Mong rằng những thông tin chi tiết trên sẽ giúp bạn hiểu rõ hơn về phản ứng CH3OH H2SO4 140 và các ứng dụng quan trọng của nó. Nếu bạn còn bất kỳ thắc mắc nào hoặc cần tư vấn thêm về các loại xe tải phù hợp với nhu cầu vận chuyển hàng hóa, đừng ngần ngại liên hệ với Xe Tải Mỹ Đình qua số hotline 0247 309 9988 hoặc truy cập trang web XETAIMYDINH.EDU.VN để được hỗ trợ tận tình. Địa chỉ của chúng tôi tại Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội luôn sẵn sàng đón tiếp bạn.
Hãy đến với Xe Tải Mỹ Đình để trải nghiệm dịch vụ tư vấn chuyên nghiệp và tìm được chiếc xe tải ưng ý nhất!
