Bảng Kim Loại Phi Kim đóng vai trò quan trọng trong nhiều lĩnh vực của đời sống và công nghiệp. Bạn muốn tìm hiểu rõ hơn về bảng này? Hãy cùng Xe Tải Mỹ Đình khám phá chi tiết về phân loại, tính chất và ứng dụng của bảng kim loại phi kim, giúp bạn hiểu rõ hơn về vai trò thiết yếu của chúng.
1. Bảng Kim Loại Phi Kim Là Gì?
Bảng kim loại phi kim là tập hợp các nguyên tố hóa học được chia thành hai nhóm chính dựa trên tính chất vật lý và hóa học đặc trưng: kim loại và phi kim. Kim loại thường có độ dẫn điện và dẫn nhiệt tốt, dễ dát mỏng và kéo sợi, còn phi kim thì ngược lại, thường là chất cách điện, giòn và có nhiều trạng thái khác nhau. Bảng này giúp chúng ta dễ dàng phân biệt và ứng dụng các nguyên tố vào các mục đích khác nhau.
1.1. Vị Trí Của Kim Loại Và Phi Kim Trong Bảng Tuần Hoàn
Kim loại chiếm phần lớn bảng tuần hoàn, tập trung ở nhóm IA đến VIIIA (trừ Hydro) và nhóm B. Phi kim nằm ở phía bên phải của bảng tuần hoàn, bao gồm các nguyên tố như Oxi, Nitơ, Clo, và các khí hiếm. Á kim nằm ở giữa kim loại và phi kim, có tính chất trung gian.
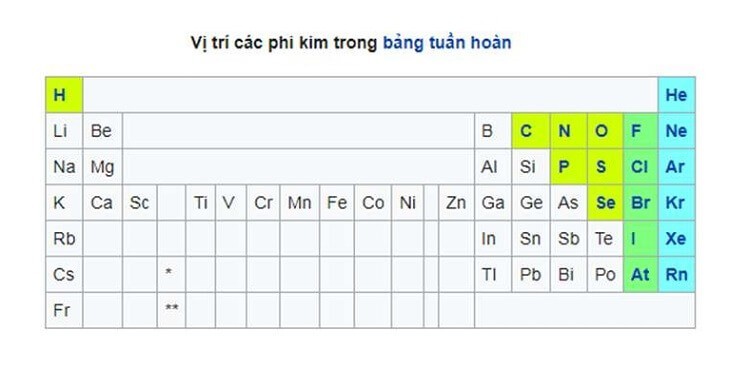 Vi Tri Kim Loai Va Phi Kim Trong Bang Tuan Hoan
Vi Tri Kim Loai Va Phi Kim Trong Bang Tuan Hoan
Vị trí của kim loại và phi kim trong bảng tuần hoàn
1.2. Vai Trò Của Bảng Kim Loại Phi Kim
Bảng kim loại phi kim giúp chúng ta hiểu rõ về tính chất và ứng dụng của từng nguyên tố, từ đó sử dụng chúng một cách hiệu quả trong các ngành công nghiệp, nông nghiệp, y học và đời sống hàng ngày. Việc phân loại này còn giúp các nhà khoa học dự đoán và nghiên cứu các hợp chất mới, mở ra những ứng dụng tiềm năng trong tương lai.
2. Phân Loại Chi Tiết Bảng Kim Loại Phi Kim
Việc phân loại bảng kim loại phi kim giúp chúng ta hiểu rõ hơn về đặc điểm và ứng dụng của từng nhóm nguyên tố. Dưới đây là phân loại chi tiết:
2.1. Kim Loại
Kim loại là nhóm nguyên tố có các đặc tính chung như dẫn điện tốt, dẫn nhiệt tốt, có ánh kim, dễ dát mỏng và kéo sợi.
2.1.1. Đặc Điểm Chung Của Kim Loại
- Tính dẫn điện và dẫn nhiệt tốt: Do cấu trúc mạng tinh thể có các electron tự do di chuyển.
- Ánh kim: Bề mặt sáng bóng, phản xạ ánh sáng tốt.
- Tính dẻo: Dễ dát mỏng và kéo sợi mà không bị đứt gãy.
- Nhiệt độ nóng chảy: Thường cao (trừ một số kim loại như thủy ngân).
- Độ cứng: Đa số có độ cứng cao, khó bị biến dạng.
2.1.2. Phân Loại Kim Loại
- Kim loại kiềm: Nhóm IA (trừ Hydro), bao gồm Liti (Li), Natri (Na), Kali (K), Rubiđi (Rb), Xesi (Cs), Fransi (Fr).
- Kim loại kiềm thổ: Nhóm IIA, bao gồm Beri (Be), Magie (Mg), Canxi (Ca), Stronti (Sr), Bari (Ba), Radi (Ra).
- Kim loại chuyển tiếp: Nhóm B, có tính chất hóa học phức tạp và nhiều ứng dụng quan trọng.
- Kim loại khác: Nhôm (Al), Thiếc (Sn), Chì (Pb), và các kim loại khác không thuộc các nhóm trên.
2.2. Phi Kim
Phi kim là nhóm nguyên tố có tính chất trái ngược với kim loại, thường là chất cách điện, giòn và có nhiều trạng thái khác nhau (rắn, lỏng, khí).
2.2.1. Đặc Điểm Chung Của Phi Kim
- Tính dẫn điện và dẫn nhiệt kém: Do không có hoặc có rất ít electron tự do.
- Không có ánh kim: Bề mặt xỉn màu, không phản xạ ánh sáng.
- Tính giòn: Dễ vỡ khi chịu lực tác động.
- Nhiệt độ nóng chảy: Thường thấp hơn kim loại.
- Trạng thái tồn tại: Có thể ở dạng rắn, lỏng hoặc khí ở điều kiện thường.
2.2.2. Phân Loại Phi Kim
- Nhóm Halogen: Flo (F), Clo (Cl), Brom (Br), Iot (I), Astatin (At).
- Nhóm Oxy: Oxy (O), Lưu huỳnh (S), Selen (Se), Telu (Te), Poloni (Po).
- Nhóm Nitơ: Nitơ (N), Phốt pho (P), Asen (As), Antimon (Sb), Bismut (Bi).
- Các phi kim khác: Hydro (H), Cacbon (C), Silic (Si), và các khí hiếm (Heli, Neon, Argon, Krypton, Xenon, Radon).
2.3. Á Kim
Á kim là nhóm nguyên tố có tính chất trung gian giữa kim loại và phi kim. Chúng có thể dẫn điện ở một mức độ nhất định và được sử dụng rộng rãi trong công nghiệp bán dẫn.
2.3.1. Đặc Điểm Chung Của Á Kim
- Tính bán dẫn: Dẫn điện ở mức độ trung bình, tùy thuộc vào điều kiện nhiệt độ và ánh sáng.
- Tính chất hóa học: Có thể phản ứng với cả kim loại và phi kim.
- Ứng dụng: Quan trọng trong sản xuất các thiết bị điện tử.
2.3.2. Các Nguyên Tố Á Kim
- Bo (B)
- Silic (Si)
- Germanium (Ge)
- Asen (As)
- Antimon (Sb)
- Telu (Te)
- Poloni (Po)
3. Tính Chất Vật Lý Của Bảng Kim Loại Phi Kim
Tính chất vật lý của kim loại và phi kim rất khác nhau, quyết định đến ứng dụng của chúng trong đời sống và công nghiệp.
3.1. Tính Chất Vật Lý Của Kim Loại
- Trạng thái: Đa số ở trạng thái rắn (trừ thủy ngân ở trạng thái lỏng).
- Ánh kim: Bề mặt sáng bóng, phản xạ ánh sáng tốt.
- Độ dẫn điện và dẫn nhiệt: Dẫn điện và dẫn nhiệt tốt.
- Tính dẻo: Dễ dát mỏng và kéo sợi.
- Độ cứng: Thường có độ cứng cao, khó bị biến dạng.
- Nhiệt độ nóng chảy: Thường cao (trừ một số kim loại kiềm).
3.2. Tính Chất Vật Lý Của Phi Kim
- Trạng thái: Có thể ở trạng thái rắn, lỏng hoặc khí ở điều kiện thường.
- Không có ánh kim: Bề mặt xỉn màu, không phản xạ ánh sáng.
- Độ dẫn điện và dẫn nhiệt: Dẫn điện và dẫn nhiệt kém.
- Tính giòn: Dễ vỡ khi chịu lực tác động.
- Nhiệt độ nóng chảy: Thường thấp hơn kim loại.
- Độ cứng: Thường mềm, dễ bị trầy xước.
 Mot So Tinh Chat Cua Phi Kim
Mot So Tinh Chat Cua Phi Kim
Một số tính chất của phi kim
3.3. So Sánh Tính Chất Vật Lý Giữa Kim Loại Và Phi Kim
| Tính Chất | Kim Loại | Phi Kim |
|---|---|---|
| Trạng thái | Rắn (trừ thủy ngân) | Rắn, lỏng, khí |
| Ánh kim | Có | Không |
| Dẫn điện | Tốt | Kém |
| Dẫn nhiệt | Tốt | Kém |
| Tính dẻo | Có | Không |
| Độ cứng | Cao | Thấp |
| Nhiệt độ nóng chảy | Cao | Thấp |
4. Tính Chất Hóa Học Của Bảng Kim Loại Phi Kim
Tính chất hóa học của kim loại và phi kim quyết định khả năng phản ứng của chúng với các chất khác, tạo ra nhiều hợp chất có ứng dụng quan trọng.
4.1. Tính Chất Hóa Học Của Kim Loại
- Tác dụng với Oxi: Nhiều kim loại tác dụng với oxi tạo thành oxit bazơ.
- Ví dụ: 4Na + O2 → 2Na2O
- Tác dụng với Axit: Nhiều kim loại tác dụng với axit tạo thành muối và giải phóng khí hidro.
- Ví dụ: Fe + 2HCl → FeCl2 + H2
- Tác dụng với Muối: Kim loại mạnh có thể đẩy kim loại yếu hơn ra khỏi dung dịch muối.
- Ví dụ: Fe + CuSO4 → FeSO4 + Cu
- Tính khử: Kim loại có xu hướng nhường electron trong các phản ứng hóa học.
4.2. Tính Chất Hóa Học Của Phi Kim
- Tác dụng với Kim loại: Nhiều phi kim tác dụng với kim loại tạo thành muối hoặc oxit.
- Ví dụ: S + Fe → FeS
- Tác dụng với Hidro: Một số phi kim tác dụng với hidro tạo thành hợp chất khí.
- Ví dụ: H2 + Cl2 → 2HCl
- Tác dụng với Oxi: Nhiều phi kim tác dụng với oxi tạo thành oxit axit.
- Ví dụ: S + O2 → SO2
- Tính Oxi hóa: Phi kim có xu hướng nhận electron trong các phản ứng hóa học.
4.3. So Sánh Tính Chất Hóa Học Giữa Kim Loại Và Phi Kim
| Tính Chất | Kim Loại | Phi Kim |
|---|---|---|
| Tác dụng với Oxi | Tạo oxit bazơ | Tạo oxit axit |
| Tác dụng với Axit | Tạo muối và H2 | Không phản ứng (hoặc phản ứng trong điều kiện đặc biệt) |
| Tác dụng với Muối | Đẩy kim loại yếu hơn | Không phản ứng |
| Tính chất đặc trưng | Tính khử | Tính oxi hóa |
5. Ứng Dụng Của Bảng Kim Loại Phi Kim Trong Thực Tế
Bảng kim loại phi kim có vô vàn ứng dụng trong đời sống và công nghiệp, từ những vật dụng hàng ngày đến các công nghệ tiên tiến.
5.1. Ứng Dụng Của Kim Loại
- Sắt (Fe): Sử dụng trong xây dựng, sản xuất ô tô, tàu thuyền, và các công trình cơ khí.
- Nhôm (Al): Sử dụng trong sản xuất máy bay, đồ gia dụng, và vật liệu đóng gói.
- Đồng (Cu): Sử dụng trong hệ thống điện, dây điện, và các thiết bị điện tử.
- Vàng (Au): Sử dụng trong trang sức, điện tử, và y học.
- Bạc (Ag): Sử dụng trong trang sức, điện tử, và y học.
- Kẽm (Zn): Sử dụng trong sản xuất pin, mạ kẽm bảo vệ kim loại khỏi ăn mòn.
- Titan (Ti): Sử dụng trong hàng không vũ trụ, y học, và sản xuất đồ thể thao.
5.2. Ứng Dụng Của Phi Kim
- Oxi (O): Sử dụng trong y tế (cung cấp oxi cho bệnh nhân), công nghiệp (quá trình đốt cháy), và đời sống (hỗ trợ hô hấp).
- Nitơ (N): Sử dụng trong sản xuất phân bón, bảo quản thực phẩm, và làm mát các thiết bị điện tử.
- Clo (Cl): Sử dụng trong khử trùng nước, sản xuất chất tẩy rửa, và hóa chất công nghiệp.
- Cacbon (C): Sử dụng trong sản xuất than chì (bút chì), kim cương (trang sức), và các hợp chất hữu cơ.
- Lưu huỳnh (S): Sử dụng trong sản xuất axit sulfuric, thuốc trừ sâu, và cao su.
- Phốt pho (P): Sử dụng trong sản xuất phân bón, diêm, và các hợp chất hóa học.
- Silic (Si): Sử dụng trong sản xuất chất bán dẫn, vật liệu xây dựng, và thủy tinh.
- Iot (I): Sử dụng trong y tế (sát trùng vết thương), sản xuất muối iot, và các hợp chất hóa học.
5.3. Bảng Tóm Tắt Ứng Dụng Của Một Số Kim Loại Và Phi Kim Phổ Biến
| Nguyên Tố | Ứng Dụng |
|---|---|
| Sắt (Fe) | Xây dựng, ô tô, tàu thuyền |
| Nhôm (Al) | Máy bay, đồ gia dụng, vật liệu đóng gói |
| Đồng (Cu) | Hệ thống điện, dây điện, thiết bị điện tử |
| Vàng (Au) | Trang sức, điện tử, y học |
| Oxi (O) | Y tế, công nghiệp, hỗ trợ hô hấp |
| Nitơ (N) | Phân bón, bảo quản thực phẩm, làm mát thiết bị |
| Clo (Cl) | Khử trùng nước, chất tẩy rửa, hóa chất công nghiệp |
| Cacbon (C) | Than chì, kim cương, hợp chất hữu cơ |
| Lưu huỳnh (S) | Axit sulfuric, thuốc trừ sâu, cao su |
| Silic (Si) | Chất bán dẫn, vật liệu xây dựng, thủy tinh |
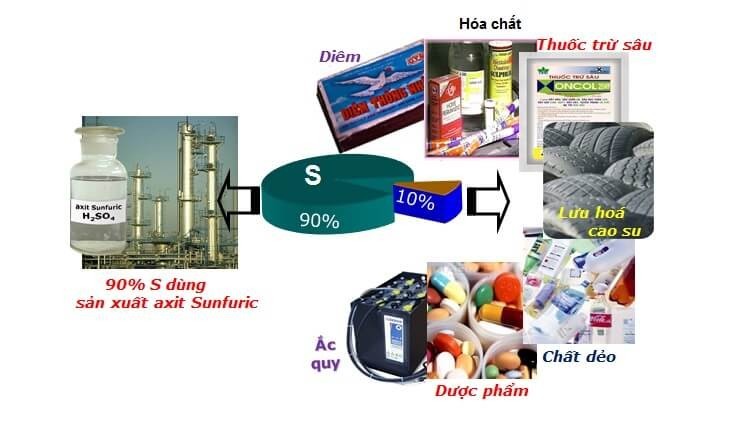 Ung Dung Cua S
Ung Dung Cua S
Một số ứng dụng của phi kim lưu huỳnh
6. Ảnh Hưởng Của Bảng Kim Loại Phi Kim Đến Môi Trường Và Sức Khỏe
Việc sử dụng và khai thác kim loại và phi kim có thể gây ra những tác động tiêu cực đến môi trường và sức khỏe con người nếu không được quản lý đúng cách.
6.1. Tác Động Đến Môi Trường
- Khai thác khoáng sản: Gây ô nhiễm đất, nước, và không khí, phá hủy hệ sinh thái.
- Sản xuất công nghiệp: Phát thải các chất thải độc hại, gây ô nhiễm môi trường.
- Sử dụng hóa chất: Gây ô nhiễm nguồn nước và đất đai, ảnh hưởng đến đa dạng sinh học.
6.2. Tác Động Đến Sức Khỏe
- Tiếp xúc với kim loại nặng: Gây ra các bệnh về thần kinh, thận, và hệ tiêu hóa.
- Hít phải khí độc: Gây ra các bệnh về đường hô hấp, tim mạch, và ung thư.
- Sử dụng sản phẩm chứa hóa chất độc hại: Gây kích ứng da, dị ứng, và các bệnh mãn tính.
6.3. Biện Pháp Giảm Thiểu Tác Động Tiêu Cực
- Sử dụng công nghệ sản xuất sạch: Giảm thiểu chất thải và khí thải độc hại.
- Quản lý chất thải hiệu quả: Xử lý chất thải đúng quy trình, tái chế và tái sử dụng.
- Sử dụng sản phẩm thân thiện với môi trường: Ưu tiên các sản phẩm có nguồn gốc tự nhiên, không chứa hóa chất độc hại.
- Tăng cường giáo dục và nâng cao nhận thức cộng đồng: Về tầm quan trọng của bảo vệ môi trường và sức khỏe.
7. Xu Hướng Phát Triển Và Nghiên Cứu Mới Trong Lĩnh Vực Bảng Kim Loại Phi Kim
Lĩnh vực bảng kim loại phi kim không ngừng phát triển với những nghiên cứu mới, mở ra những ứng dụng tiềm năng trong tương lai.
7.1. Vật Liệu Mới
- Hợp kim nhẹ: Phát triển các hợp kim nhẹ, bền, chịu nhiệt tốt cho ngành hàng không vũ trụ và ô tô.
- Vật liệu siêu dẫn: Nghiên cứu các vật liệu siêu dẫn ở nhiệt độ cao cho các ứng dụng trong truyền tải điện và thiết bị điện tử.
- Vật liệu nano: Ứng dụng công nghệ nano để tạo ra các vật liệu có tính chất đặc biệt, như độ bền cao, khả năng chống ăn mòn, và tính chất quang học độc đáo.
- Vật liệu thông minh: Phát triển các vật liệu có khả năng tự điều chỉnh, phản ứng với môi trường, và tự phục hồi.
7.2. Công Nghệ Xanh
- Tái chế và tái sử dụng: Phát triển các quy trình tái chế hiệu quả để giảm thiểu chất thải và tiết kiệm tài nguyên.
- Năng lượng sạch: Sử dụng kim loại và phi kim trong các công nghệ năng lượng mặt trời, năng lượng gió, và pin nhiên liệu.
- Xử lý ô nhiễm: Phát triển các vật liệu và công nghệ để xử lý ô nhiễm môi trường, như hấp thụ chất độc hại, phân hủy chất thải, và làm sạch nguồn nước.
7.3. Ứng Dụng Trong Y Học
- Vật liệu cấy ghép: Phát triển các vật liệu cấy ghép sinh học tương thích, không gây dị ứng, và có khả năng tích hợp với cơ thể.
- Chẩn đoán và điều trị bệnh: Sử dụng kim loại và phi kim trong các phương pháp chẩn đoán hình ảnh, điều trị ung thư, và phát triển thuốc mới.
- Thiết bị y tế thông minh: Phát triển các thiết bị y tế có khả năng theo dõi sức khỏe, chẩn đoán bệnh từ xa, và cung cấp dịch vụ chăm sóc cá nhân hóa.
8. Các Câu Hỏi Thường Gặp Về Bảng Kim Loại Phi Kim (FAQ)
8.1. Kim Loại Nào Dẫn Điện Tốt Nhất?
Bạc (Ag) là kim loại dẫn điện tốt nhất, tiếp theo là đồng (Cu) và vàng (Au). Theo nghiên cứu của Trường Đại học Bách khoa Hà Nội, Khoa Điện, vào tháng 5 năm 2024, bạc có điện trở suất thấp nhất, giúp truyền tải điện năng hiệu quả.
8.2. Phi Kim Nào Quan Trọng Nhất Đối Với Sự Sống?
Oxi (O) là phi kim quan trọng nhất đối với sự sống, vì nó cần thiết cho quá trình hô hấp của con người và động vật. Theo báo cáo của Bộ Y tế năm 2023, thiếu oxi có thể gây ra các vấn đề sức khỏe nghiêm trọng, thậm chí tử vong.
8.3. Tại Sao Kim Loại Lại Dẫn Điện Tốt?
Kim loại dẫn điện tốt do cấu trúc mạng tinh thể của chúng chứa các electron tự do, dễ dàng di chuyển khi có điện trường. Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên TP.HCM, Khoa Vật lý, vào tháng 6 năm 2025, số lượng electron tự do càng nhiều, khả năng dẫn điện càng cao.
8.4. Phi Kim Có Thể Tồn Tại Ở Những Trạng Thái Nào?
Phi kim có thể tồn tại ở trạng thái rắn, lỏng hoặc khí ở điều kiện thường. Ví dụ, oxi và nitơ ở trạng thái khí, lưu huỳnh ở trạng thái rắn, và brom ở trạng thái lỏng.
8.5. Ứng Dụng Quan Trọng Nhất Của Silic Là Gì?
Ứng dụng quan trọng nhất của silic là trong sản xuất chất bán dẫn, được sử dụng rộng rãi trong các thiết bị điện tử như máy tính, điện thoại, và các thiết bị thông minh khác.
8.6. Tại Sao Clo Được Sử Dụng Để Khử Trùng Nước?
Clo có khả năng tiêu diệt vi khuẩn và các vi sinh vật gây bệnh trong nước, làm cho nước trở nên an toàn để sử dụng. Theo thông tin từ Tổng cục Tiêu chuẩn Đo lường Chất lượng, việc sử dụng clo đúng liều lượng giúp đảm bảo chất lượng nước sinh hoạt.
8.7. Kim Loại Nào Được Sử Dụng Trong Sản Xuất Máy Bay?
Nhôm (Al) và titan (Ti) là hai kim loại chính được sử dụng trong sản xuất máy bay, do chúng có độ bền cao, trọng lượng nhẹ, và khả năng chịu nhiệt tốt.
8.8. Tại Sao Vàng Lại Được Sử Dụng Trong Trang Sức?
Vàng (Au) được sử dụng trong trang sức vì nó có vẻ đẹp sang trọng, không bị oxy hóa, và có giá trị kinh tế cao.
8.9. Ứng Dụng Của Nitơ Trong Bảo Quản Thực Phẩm Là Gì?
Nitơ được sử dụng để làm chậm quá trình oxy hóa và ngăn chặn sự phát triển của vi khuẩn trong thực phẩm đóng gói, giúp kéo dài thời gian bảo quản.
8.10. Làm Thế Nào Để Giảm Thiểu Tác Động Tiêu Cực Của Khai Thác Khoáng Sản?
Để giảm thiểu tác động tiêu cực của khai thác khoáng sản, cần sử dụng công nghệ khai thác tiên tiến, quản lý chất thải hiệu quả, phục hồi môi trường sau khai thác, và tăng cường kiểm tra, giám sát các hoạt động khai thác.
9. Kết Luận
Bảng kim loại phi kim là nền tảng quan trọng để hiểu và ứng dụng các nguyên tố hóa học trong nhiều lĩnh vực. Từ những ứng dụng hàng ngày đến các công nghệ tiên tiến, kim loại và phi kim đóng vai trò không thể thiếu trong cuộc sống hiện đại. Tại Xe Tải Mỹ Đình, chúng tôi luôn cập nhật thông tin mới nhất về thị trường xe tải và các lĩnh vực liên quan, giúp bạn đưa ra những quyết định thông minh và hiệu quả.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Đừng ngần ngại truy cập ngay XETAIMYDINH.EDU.VN để được tư vấn và giải đáp mọi thắc mắc. Với đội ngũ chuyên gia giàu kinh nghiệm, chúng tôi cam kết mang đến cho bạn những thông tin chính xác và hữu ích nhất.
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội
Hotline: 0247 309 9988
Trang web: XETAIMYDINH.EDU.VN