Ancol đơn Chức, một hợp chất hữu cơ quan trọng, đóng vai trò thiết yếu trong nhiều ngành công nghiệp và đời sống. Bài viết này của Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ cung cấp cái nhìn toàn diện về ancol đơn chức, từ định nghĩa, tính chất, điều chế đến ứng dụng, giúp bạn đọc hiểu rõ hơn về hợp chất này. Khám phá ngay những thông tin chi tiết về các loại rượu đơn chức và cồn đơn chức phổ biến nhất hiện nay.
1. Ancol Đơn Chức Là Gì? Định Nghĩa Chi Tiết
Ancol đơn chức là hợp chất hữu cơ mà trong phân tử chỉ chứa một nhóm hydroxyl (-OH) liên kết trực tiếp với một nguyên tử carbon no. Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên Hà Nội, Khoa Hóa học, năm 2024, ancol đơn chức đóng vai trò quan trọng trong các phản ứng hóa học và tổng hợp hữu cơ. Công thức tổng quát của ancol đơn chức no, mạch hở là CnH2n+1OH (n ≥ 1).
 Cong Thuc Ancol Don Chuc
Cong Thuc Ancol Don Chuc
Công thức cấu tạo chung của một ancol đơn chức
2. Phân Loại Ancol Đơn Chức Phổ Biến
Ancol đơn chức có thể được phân loại dựa trên nhiều tiêu chí khác nhau, giúp chúng ta dễ dàng nhận biết và ứng dụng chúng trong thực tế.
2.1. Dựa Vào Cấu Trúc Gốc Hydrocarbon
- Ancol no đơn chức: Gốc hydrocarbon là gốc alkyl no, mạch hở (CnH2n+1). Ví dụ: methanol (CH3OH), ethanol (C2H5OH).
- Ancol không no đơn chức: Gốc hydrocarbon chứa liên kết đôi hoặc liên kết ba. Ví dụ: allyl alcohol (CH2=CH-CH2OH).
- Ancol thơm đơn chức: Nhóm -OH liên kết với mạch nhánh của vòng benzene. Ví dụ: benzyl alcohol (C6H5CH2OH).
2.2. Dựa Vào Bậc Của Nguyên Tử Carbon Liên Kết Với Nhóm -OH
- Ancol bậc 1 (ancol प्राथमिक): Nguyên tử carbon liên kết với nhóm -OH chỉ liên kết với một nguyên tử carbon khác. Ví dụ: ethanol (CH3CH2OH).
Ethanol là một ví dụ điển hình của ancol bậc 1
- Ancol bậc 2 (ancol द्वितीयक): Nguyên tử carbon liên kết với nhóm -OH liên kết với hai nguyên tử carbon khác. Ví dụ: isopropanol (CH3CHOHCH3).
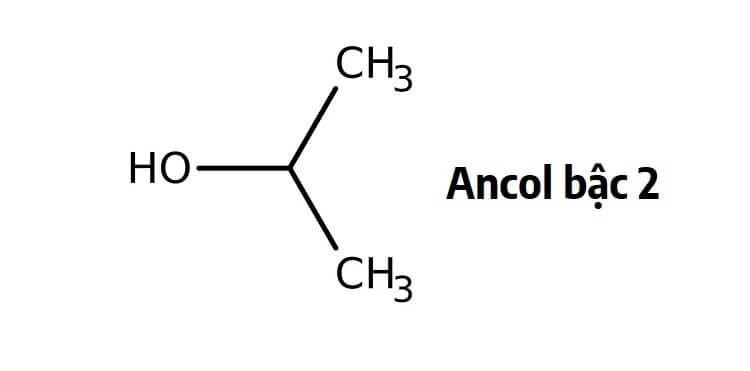 Isopropanol Bậc 2
Isopropanol Bậc 2
Isopropanol, một ancol bậc 2 được sử dụng rộng rãi
- Ancol bậc 3 (ancol तृतीयक): Nguyên tử carbon liên kết với nhóm -OH liên kết với ba nguyên tử carbon khác. Ví dụ: tert-butanol ((CH3)3COH).
3. Cách Gọi Tên Ancol Đơn Chức Theo IUPAC Và Tên Thông Thường
Việc gọi tên ancol đơn chức tuân theo các quy tắc nhất định, giúp chúng ta dễ dàng xác định cấu trúc và tính chất của chúng.
3.1. Tên IUPAC (Danh Pháp Thay Thế)
Tên IUPAC của ancol đơn chức được hình thành theo công thức:
Tên hydrocarbon tương ứng + vị trí nhóm -OH + “-ol”
- Chọn mạch carbon dài nhất chứa nhóm -OH làm mạch chính.
- Đánh số các nguyên tử carbon trên mạch chính sao cho vị trí của nhóm -OH là nhỏ nhất.
- Gọi tên theo thứ tự: vị trí nhóm thế (nếu có) – tên nhóm thế – tên hydrocarbon mạch chính – vị trí nhóm -OH – “ol”.
Ví dụ:
- CH3OH: Methanol
- CH3CH2OH: Ethanol
- CH3CH2CH2OH: Propan-1-ol
- CH3CH(OH)CH3: Propan-2-ol
3.2. Tên Thông Thường
Tên thông thường của ancol đơn chức được hình thành theo công thức:
“Ancol” + tên gốc alkyl + “-ic”
Ví dụ:
- CH3OH: Ancol metylic
- CH3CH2OH: Ancol etylic
- CH3CH2CH2OH: Ancol propylic
- CH3CH(OH)CH3: Ancol isopropylic
4. Tính Chất Vật Lý Đặc Trưng Của Ancol Đơn Chức
Tính chất vật lý của ancol đơn chức ảnh hưởng lớn đến cách chúng ta sử dụng và ứng dụng chúng trong thực tế.
- Trạng thái: Các ancol đơn chức có số carbon nhỏ (từ 1 đến 11) thường ở trạng thái lỏng ở nhiệt độ phòng, các ancol có số carbon lớn hơn thường ở trạng thái rắn.
- Độ tan: Các ancol đơn chức có số carbon nhỏ tan tốt trong nước do tạo được liên kết hydrogen với nước. Độ tan giảm khi số carbon tăng lên do phần hydrocarbon kị nước tăng.
- Nhiệt độ sôi: Nhiệt độ sôi của ancol đơn chức cao hơn so với các hydrocarbon có phân tử khối tương đương do liên kết hydrogen giữa các phân tử ancol. Nhiệt độ sôi tăng khi số carbon tăng.
- Độ nhớt: Ancol đơn chức thường có độ nhớt cao hơn so với các hydrocarbon tương ứng do liên kết hydrogen.
5. Tính Chất Hóa Học Quan Trọng Của Ancol Đơn Chức
Tính chất hóa học của ancol đơn chức là cơ sở cho nhiều ứng dụng quan trọng trong công nghiệp và nghiên cứu.
5.1. Phản Ứng Thế Hydro Của Nhóm -OH
Ancol đơn chức phản ứng với kim loại kiềm như natri (Na) hoặc kali (K) tạo thành alkoxide và giải phóng khí hydrogen.
2R-OH + 2Na → 2R-ONa + H2
Ví dụ:
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2
Phản ứng này chứng minh tính acid yếu của ancol.
5.2. Phản Ứng Với Acid Vô Cơ
Ancol đơn chức phản ứng với acid vô cơ như HCl, HBr, HI tạo thành dẫn xuất halogen và nước.
R-OH + HX → R-X + H2O (X = Cl, Br, I)
Ví dụ:
CH3CH2OH + HCl → CH3CH2Cl + H2O
Phản ứng này thường cần xúc tác acid như H2SO4 đặc.
5.3. Phản Ứng Tách Nước (Dehydration)
Khi đun nóng với xúc tác acid (H2SO4 đặc, H3PO4), ancol đơn chức có thể bị tách nước tạo thành alkene hoặc ether.
- Tạo alkene (ở nhiệt độ cao, >170°C):
CH3CH2OH → CH2=CH2 + H2O
- Tạo ether (ở nhiệt độ thấp hơn, ~140°C):
2CH3CH2OH → CH3CH2OCH2CH3 + H2O
5.4. Phản Ứng Oxy Hóa
Phản ứng oxy hóa ancol đơn chức tạo ra các sản phẩm khác nhau tùy thuộc vào bậc của ancol và tác nhân oxy hóa.
- Ancol bậc 1:
- Oxy hóa nhẹ (ví dụ: sử dụng pyridinium chlorochromate – PCC) tạo thành aldehyde:
RCH2OH → RCHO
* Oxy hóa mạnh (ví dụ: sử dụng KMnO4, K2Cr2O7) tạo thành acid carboxylic:RCH2OH → RCOOH
- Ancol bậc 2:
- Oxy hóa tạo thành ketone:
R1CHOHR2 → R1COR2
- Ancol bậc 3:
- Khó bị oxy hóa hơn, thường cần điều kiện khắc nghiệt và phá vỡ mạch carbon.
5.5. Phản Ứng Este Hóa
Ancol đơn chức phản ứng với acid carboxylic tạo thành ester và nước, phản ứng này được gọi là phản ứng este hóa.
R-OH + R’COOH ⇌ R’COOR + H2O
Phản ứng này thường cần xúc tác acid như H2SO4 đặc.
6. Điều Chế Ancol Đơn Chức Bằng Các Phương Pháp Nào?
Có nhiều phương pháp khác nhau để điều chế ancol đơn chức, tùy thuộc vào nguyên liệu ban đầu và loại ancol mong muốn.
6.1. Hydrat Hóa Alkene
Alkene phản ứng với nước (H2O) trong môi trường acid (H+) tạo thành ancol. Phản ứng tuân theo quy tắc Markovnikov.
RCH=CH2 + H2O → RCH(OH)CH3
 Hydrat Hóa Etylen
Hydrat Hóa Etylen
Quá trình hydrat hóa ethylene để tạo ra ethanol
6.2. Thủy Phân Dẫn Xuất Halogen
Dẫn xuất halogen (alkyl halide) phản ứng với dung dịch kiềm (NaOH, KOH) tạo thành ancol.
R-X + NaOH → R-OH + NaX (X = Cl, Br, I)
6.3. Phản Ứng Grignard
Phản ứng Grignard là một phương pháp quan trọng để tạo liên kết C-C mới và điều chế ancol.
- Aldehyde + Thuốc thử Grignard → Ancol bậc 2
- Ketone + Thuốc thử Grignard → Ancol bậc 3
Ví dụ:
RCHO + R’MgX → RCH(OMgX)R’ → RCH(OH)R’
6.4. Khử Aldehyde Và Ketone
Aldehyde và ketone có thể bị khử bằng các chất khử như NaBH4 hoặc LiAlH4 để tạo thành ancol.
- Khử aldehyde → Ancol bậc 1
- Khử ketone → Ancol bậc 2
Ví dụ:
RCHO + NaBH4 → RCH2OH
6.5. Lên Men Đường Hoặc Tinh Bột
Phương pháp lên men được sử dụng rộng rãi để sản xuất ethanol từ các nguồn đường hoặc tinh bột.
(C6H10O5)n + nH2O → nC6H12O6 (thủy phân tinh bột)
C6H12O6 → 2C2H5OH + 2CO2 (lên men)
7. Ứng Dụng Quan Trọng Của Ancol Đơn Chức Trong Đời Sống Và Công Nghiệp
Ancol đơn chức có rất nhiều ứng dụng quan trọng trong đời sống và công nghiệp, từ làm dung môi đến sản xuất nhiên liệu và hóa chất.
- Dung môi: Ancol đơn chức được sử dụng rộng rãi làm dung môi trong nhiều ngành công nghiệp như sơn, mực in, dược phẩm và mỹ phẩm.
- Nhiên liệu: Ethanol được sử dụng làm nhiên liệu sinh học, có thể pha trộn với xăng để giảm thiểu khí thải.
- Sản xuất hóa chất: Ancol đơn chức là nguyên liệu quan trọng để sản xuất nhiều hóa chất khác như aldehyde, acid carboxylic, ester và ether.
- Chất khử trùng: Isopropanol (cồn isopropyl) được sử dụng làm chất khử trùng trong y tế và gia đình.
- Chất chống đông: Ethylene glycol được sử dụng làm chất chống đông trong ô tô.
- Sản xuất đồ uống có cồn: Ethanol là thành phần chính trong đồ uống có cồn như bia, rượu vang và rượu mạnh.
Ethanol có nhiều ứng dụng, từ khử trùng đến sản xuất đồ uống
8. So Sánh Các Loại Ancol Đơn Chức Phổ Biến Nhất Hiện Nay
| Ancol | Công Thức Hóa Học | Ứng Dụng Chính |
|---|---|---|
| Methanol | CH3OH | Sản xuất formaldehyde, dung môi, phụ gia nhiên liệu. |
| Ethanol | C2H5OH | Đồ uống có cồn, nhiên liệu sinh học, dung môi. |
| Isopropanol | (CH3)2CHOH | Chất khử trùng, dung môi trong công nghiệp. |
| Butanol | C4H9OH | Dung môi, sản xuất chất dẻo, chất tẩy rửa. |
| Pentanol | C5H11OH | Dung môi, sản xuất dược phẩm, hương liệu. |
9. Những Lưu Ý Quan Trọng Khi Sử Dụng Ancol Đơn Chức
Khi sử dụng ancol đơn chức, cần lưu ý các vấn đề sau để đảm bảo an toàn và hiệu quả:
- Độc tính: Một số ancol như methanol có độc tính cao, có thể gây mù lòa hoặc tử vong nếu uống phải.
- Tính dễ cháy: Ancol đơn chức dễ cháy, cần được bảo quản và sử dụng ở nơi thoáng khí, tránh xa nguồn nhiệt và lửa.
- Tác động đến sức khỏe: Tiếp xúc lâu dài với một số ancol có thể gây kích ứng da, mắt và hệ hô hấp.
- Bảo quản: Ancol cần được bảo quản trong các bình chứa kín, đặt ở nơi khô ráo, thoáng mát và tránh ánh nắng trực tiếp.
10. FAQ: Các Câu Hỏi Thường Gặp Về Ancol Đơn Chức
Câu 1: Ancol đơn chức là gì?
Ancol đơn chức là hợp chất hữu cơ mà phân tử chỉ chứa một nhóm hydroxyl (-OH) liên kết trực tiếp với một nguyên tử carbon no.
Câu 2: Công thức tổng quát của ancol đơn chức no, mạch hở là gì?
Công thức tổng quát là CnH2n+1OH (n ≥ 1).
Câu 3: Ancol đơn chức có tan trong nước không?
Các ancol đơn chức có số carbon nhỏ tan tốt trong nước do tạo được liên kết hydrogen với nước. Độ tan giảm khi số carbon tăng lên.
Câu 4: Ancol đơn chức có những ứng dụng gì?
Ancol đơn chức được sử dụng làm dung môi, nhiên liệu, chất khử trùng, chất chống đông và trong sản xuất nhiều hóa chất khác.
Câu 5: Methanol có độc không?
Có, methanol có độc tính cao, có thể gây mù lòa hoặc tử vong nếu uống phải.
Câu 6: Làm thế nào để điều chế ancol đơn chức?
Có nhiều phương pháp điều chế ancol đơn chức như hydrat hóa alkene, thủy phân dẫn xuất halogen, phản ứng Grignard và khử aldehyde/ketone.
Câu 7: Ancol bậc 1, bậc 2 và bậc 3 khác nhau như thế nào?
Sự khác biệt nằm ở số lượng nguyên tử carbon liên kết với nguyên tử carbon mang nhóm -OH: bậc 1 liên kết với 1 carbon, bậc 2 liên kết với 2 carbon và bậc 3 liên kết với 3 carbon.
Câu 8: Tại sao ancol đơn chức lại có nhiệt độ sôi cao hơn so với hydrocarbon tương ứng?
Do liên kết hydrogen giữa các phân tử ancol.
Câu 9: Phản ứng este hóa là gì?
Là phản ứng giữa ancol và acid carboxylic tạo thành ester và nước.
Câu 10: Cần lưu ý gì khi sử dụng ancol đơn chức?
Cần lưu ý về độc tính, tính dễ cháy, tác động đến sức khỏe và bảo quản đúng cách.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình, Hà Nội? Đừng ngần ngại truy cập XETAIMYDINH.EDU.VN ngay hôm nay để được tư vấn và giải đáp mọi thắc mắc. Xe Tải Mỹ Đình cam kết cung cấp thông tin cập nhật, chính xác và hữu ích nhất, giúp bạn đưa ra quyết định sáng suốt khi lựa chọn xe tải phù hợp với nhu cầu và ngân sách của mình. Liên hệ ngay với chúng tôi qua hotline 0247 309 9988 hoặc ghé thăm địa chỉ Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội để trải nghiệm dịch vụ chuyên nghiệp và tận tâm nhất.