Orbital Nguyên Tử Là vùng không gian xung quanh hạt nhân, nơi xác suất tìm thấy electron là lớn nhất và đây là khái niệm then chốt trong hóa học lượng tử. Tại XETAIMYDINH.EDU.VN, chúng tôi sẽ cung cấp cho bạn những thông tin chi tiết nhất về các loại orbital, quy tắc phân bố electron, cùng những ứng dụng thực tiễn của chúng, giúp bạn hiểu rõ hơn về thế giới vi mô. Bài viết này sẽ giúp bạn nắm bắt kiến thức cơ bản, đồng thời khám phá sâu hơn về cấu trúc nguyên tử, sự phân bố electron và năng lượng orbital.
1. Orbital Nguyên Tử Là Gì?
Orbital nguyên tử, một khái niệm cơ bản trong hóa học và vật lý lượng tử, mô tả khu vực không gian quanh hạt nhân, nơi xác suất tìm thấy electron là cao nhất. Orbital nguyên tử không phải là quỹ đạo cố định của electron, mà là một hàm toán học biểu diễn trạng thái lượng tử của electron trong nguyên tử.
Khái niệm orbital nguyên tử hình thành dựa trên cơ học lượng tử và được mô tả bằng hàm sóng Schrödinger. Nó cung cấp thông tin quan trọng về cấu trúc nguyên tử và cách các electron tương tác. Các orbital là yếu tố cốt lõi giúp giải thích sự sắp xếp và tính chất hóa học của các nguyên tử. Việc nghiên cứu orbital giúp dự đoán hình dạng phân tử, phản ứng hóa học và nhiều hiện tượng vật lý khác.
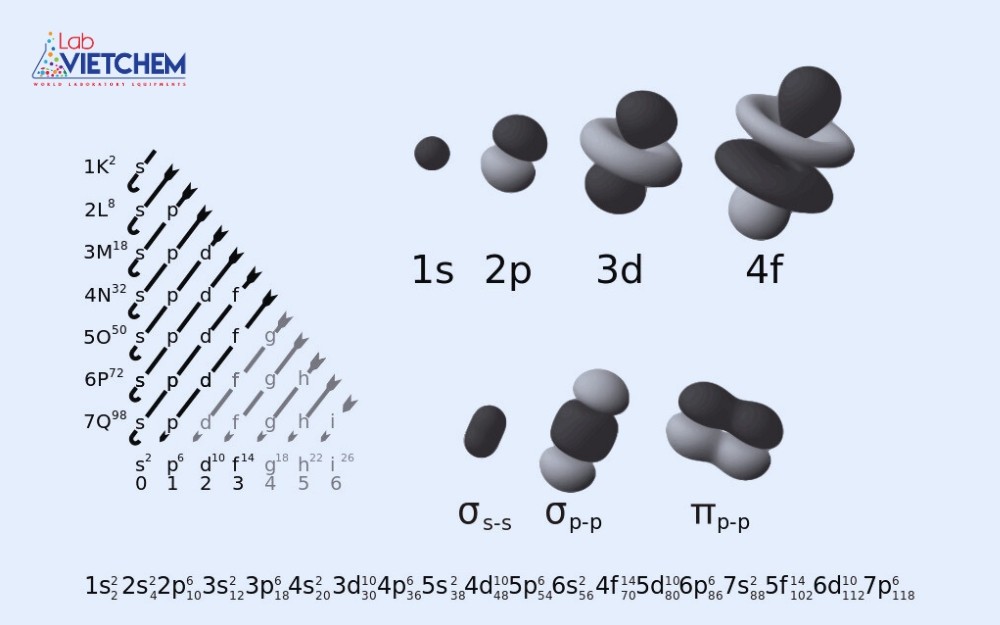 Orbital nguyên tử
Orbital nguyên tử
2. Các Loại Orbital Nguyên Tử
Orbital nguyên tử được phân loại dựa trên ba số lượng tử quan trọng: số lượng tử chính (n), số lượng tử góc (l) và số lượng tử từ (ml). Dựa trên giá trị của l, orbital nguyên tử được chia thành các loại sau:
2.1. Orbital s
Orbital s (l = 0) có hình dạng hình cầu và đối xứng quanh hạt nhân nguyên tử. Mỗi mức năng lượng (n) chỉ có một orbital s duy nhất. Orbital s là orbital có mức năng lượng thấp nhất trong mỗi lớp electron.
- Đặc điểm: Hình cầu, đối xứng.
- Số lượng: 1 orbital s trên mỗi lớp.
- Vai trò: Quan trọng trong các nguyên tử đơn giản như hydro và heli.
- Vị trí: Electron có xác suất xuất hiện cao nhất gần hạt nhân.
Ví dụ: Orbital 1s của hydro có hình dạng hình cầu, biểu thị xác suất tìm thấy electron xung quanh hạt nhân là như nhau theo mọi hướng.
2.2. Orbital p
Orbital p (l = 1) có hình dạng giống hình quả tạ, với hai thùy nằm đối xứng qua hạt nhân. Có ba orbital p khác nhau, định hướng theo ba trục tọa độ vuông góc: px, py và pz. Các orbital p xuất hiện từ mức năng lượng n = 2 trở lên.
- Đặc điểm: Hình quả tạ, ba hướng (px, py, pz).
- Số lượng: 3 orbital p trên mỗi lớp (từ n=2).
- Vai trò: Tạo liên kết trong các nguyên tử như carbon, oxy và nitơ.
- Liên kết: Có thể tạo liên kết đôi và ba.
Ví dụ: Carbon có hai electron ở orbital 2p, cho phép nó tạo thành bốn liên kết cộng hóa trị, tạo nên sự đa dạng của các hợp chất hữu cơ.
2.3. Orbital d
Orbital d (l = 2) có hình dạng phức tạp hơn orbital p, với nhiều thùy và vùng nút. Có năm orbital d khác nhau, xuất hiện từ mức năng lượng n = 3 trở lên. Các orbital d đóng vai trò quan trọng trong các nguyên tử kim loại chuyển tiếp.
- Đặc điểm: Hình dạng phức tạp, nhiều thùy.
- Số lượng: 5 orbital d trên mỗi lớp (từ n=3).
- Vai trò: Quan trọng trong kim loại chuyển tiếp (sắt, đồng, niken).
- Tính chất: Góp phần vào tính từ tính, độ bền cơ học và hoạt động xúc tác.
Ví dụ: Sắt (Fe) có các electron ở orbital 3d, góp phần vào tính chất từ tính mạnh mẽ của nó, được ứng dụng trong nhiều lĩnh vực công nghiệp.
2.4. Orbital f
Orbital f (l = 3) có hình dạng rất phức tạp, với nhiều thùy và vùng nút hơn so với orbital d. Có bảy orbital f khác nhau, bắt đầu xuất hiện từ mức năng lượng n = 4. Orbital f thường liên kết với các nguyên tố đất hiếm và actinide.
- Đặc điểm: Hình dạng rất phức tạp, nhiều thùy.
- Số lượng: 7 orbital f trên mỗi lớp (từ n=4).
- Vai trò: Quan trọng trong các nguyên tố đất hiếm và actinide (lantan, urani).
- Ứng dụng: Sử dụng trong vật liệu làm nam châm và linh kiện công nghệ cao.
Ví dụ: Urani (U) có các electron ở orbital 5f, đóng vai trò quan trọng trong các ứng dụng năng lượng hạt nhân.
Bảng tóm tắt các loại orbital nguyên tử:
| Loại Orbital | Số Lượng Tử Góc (l) | Hình Dạng | Số Lượng Orbital | Bắt Đầu Từ Lớp Thứ |
|---|---|---|---|---|
| s | 0 | Hình cầu | 1 | 1 |
| p | 1 | Quả tạ | 3 | 2 |
| d | 2 | Phức tạp | 5 | 3 |
| f | 3 | Rất phức tạp | 7 | 4 |
3. Các Quy Tắc Phân Bố Electron Trong Orbital
Việc phân bố electron vào các orbital tuân theo một số quy tắc nhất định, đảm bảo sự ổn định của nguyên tử.
3.1. Nguyên Tắc Aufbau (Nguyên Tắc Xây Dựng)
Nguyên tắc Aufbau quy định rằng các electron sẽ chiếm các orbital có mức năng lượng thấp trước, sau đó mới đến các orbital có mức năng lượng cao hơn. Điều này đảm bảo nguyên tử đạt trạng thái năng lượng thấp nhất, ổn định nhất.
- Mô tả: Electron lấp đầy orbital năng lượng thấp trước.
- Mục đích: Đảm bảo cấu trúc bền vững của nguyên tử.
- Giải thích: Tại sao các nguyên tố có tính chất hóa học khác nhau.
Theo nghiên cứu của Đại học Khoa học Tự nhiên Hà Nội, nguyên tắc Aufbau là nền tảng để xác định cấu hình electron của các nguyên tố, giúp dự đoán tính chất hóa học của chúng.
3.2. Nguyên Tắc Pauli (Nguyên Tắc Loại Trừ Pauli)
Nguyên tắc Pauli nói rằng mỗi orbital chỉ có thể chứa tối đa hai electron và hai electron này phải có spin đối nhau. Spin là một tính chất lượng tử của electron, có thể có hai giá trị là +1/2 hoặc -1/2, thường được gọi là spin “lên” và spin “xuống”.
- Mô tả: Mỗi orbital chứa tối đa 2 electron với spin ngược nhau.
- Cơ sở: Cơ học lượng tử.
- Ý nghĩa: Đảm bảo không có hai electron nào có cùng trạng thái lượng tử.
Ví dụ: Một orbital 2p có thể chứa tối đa hai electron, một có spin “lên” và một có spin “xuống”.
3.3. Quy Tắc Hund (Quy Tắc Hund)
Quy tắc Hund áp dụng cho các orbital có cùng mức năng lượng (ví dụ: ba orbital p). Nó nói rằng electron sẽ điền vào từng orbital một trước, sao cho số lượng electron độc thân (electron không ghép đôi) là tối đa, sau đó mới bắt đầu ghép đôi electron vào các orbital.
- Mô tả: Electron điền vào từng orbital trước khi ghép đôi.
- Mục đích: Giảm sự đẩy giữa các electron.
- Kết quả: Tăng độ bền của nguyên tử hoặc ion.
Ví dụ: Trong nguyên tử nitơ (N), ba electron ở lớp 2p sẽ chiếm ba orbital 2px, 2py, 2pz một cách độc thân, thay vì ghép đôi trong một orbital.
4. Ứng Dụng Của Orbital Nguyên Tử
Hiểu biết về orbital nguyên tử có nhiều ứng dụng quan trọng trong các lĩnh vực khác nhau.
4.1. Hóa Học Lý Thuyết
Orbital nguyên tử giúp giải thích cách các nguyên tử kết hợp với nhau để tạo thành phân tử, từ đó giúp dự đoán và mô phỏng phản ứng hóa học.
- Ứng dụng: Dự đoán hình dạng phân tử, tính chất liên kết và khả năng phản ứng.
- Ví dụ: Mô hình hóa cấu trúc và phản ứng của các enzyme trong sinh học.
- Lợi ích: Phát triển các chất xúc tác mới, thiết kế thuốc hiệu quả hơn.
Ví dụ, các nhà hóa học có thể sử dụng lý thuyết orbital phân tử để dự đoán hình dạng và tính chất của phân tử nước (H2O), từ đó hiểu rõ hơn về các tương tác giữa các phân tử nước.
4.2. Công Nghệ Vật Liệu
Orbital nguyên tử đóng vai trò quan trọng trong việc thiết kế và phát triển vật liệu bán dẫn, sử dụng trong các vi mạch điện tử, cảm biến và thiết bị quang học.
- Vật liệu bán dẫn: Thiết kế và phát triển vật liệu cho vi mạch, cảm biến.
- Hợp kim cứng: Phát triển hợp kim có tính chất cơ học đặc biệt (thép không gỉ, titan, niken).
Theo báo cáo của Tổng cục Thống kê, ngành công nghiệp vật liệu bán dẫn Việt Nam đang có tốc độ tăng trưởng ấn tượng, đòi hỏi nguồn nhân lực chất lượng cao am hiểu về orbital nguyên tử.
4.3. Y Học Và Công Nghệ Nano
Các nguyên tử với orbital đặc biệt được sử dụng trong chế tạo thuốc, hình ảnh y học (MRI) và điều trị ung thư bằng liệu pháp hạt nhân.
- Ứng dụng trong y học: Chế tạo thuốc, hình ảnh y học (MRI), điều trị ung thư.
- Công nghệ nano: Nghiên cứu và phát triển vật liệu nano (màng lọc nano, điện cực pin lithium-ion).
Các nhà nghiên cứu tại Viện Hóa học, Viện Hàn lâm Khoa học và Công nghệ Việt Nam đang tập trung nghiên cứu ứng dụng của vật liệu nano trong y sinh học, mở ra nhiều tiềm năng mới trong chẩn đoán và điều trị bệnh.
4.4. Kỹ Thuật Laser Và Quang Học
Hiểu về orbital nguyên tử giúp thiết kế và tối ưu hóa các nguồn sáng laser, phục vụ trong nghiên cứu khoa học, y học và truyền thông quang học.
- Ứng dụng: Thiết kế và tối ưu hóa laser.
- Lĩnh vực: Nghiên cứu khoa học, y học, truyền thông quang học.
Việc phát triển các laser bán dẫn dựa trên hiểu biết về orbital nguyên tử đã mang lại cuộc cách mạng trong lĩnh vực truyền thông, cho phép truyền tải dữ liệu với tốc độ cao và độ tin cậy cao.
5. Câu Hỏi Thường Gặp (FAQ) Về Orbital Nguyên Tử
Dưới đây là một số câu hỏi thường gặp về orbital nguyên tử, giúp bạn hiểu rõ hơn về khái niệm này:
- Orbital nguyên tử là gì?
- Orbital nguyên tử là khu vực không gian xung quanh hạt nhân nguyên tử, nơi xác suất tìm thấy electron là cao nhất.
- Có bao nhiêu loại orbital nguyên tử?
- Có bốn loại orbital nguyên tử chính: s, p, d và f.
- Hình dạng của orbital s là gì?
- Orbital s có hình dạng hình cầu.
- Hình dạng của orbital p là gì?
- Orbital p có hình dạng giống hình quả tạ.
- Nguyên tắc Aufbau là gì?
- Nguyên tắc Aufbau quy định rằng electron sẽ lấp đầy các orbital có mức năng lượng thấp trước.
- Nguyên tắc Pauli là gì?
- Nguyên tắc Pauli nói rằng mỗi orbital chỉ có thể chứa tối đa hai electron với spin đối nhau.
- Quy tắc Hund là gì?
- Quy tắc Hund nói rằng electron sẽ điền vào từng orbital một trước khi ghép đôi.
- Orbital nguyên tử có ứng dụng gì trong hóa học lý thuyết?
- Orbital nguyên tử giúp dự đoán hình dạng phân tử, tính chất liên kết và khả năng phản ứng.
- Orbital nguyên tử có ứng dụng gì trong công nghệ vật liệu?
- Orbital nguyên tử đóng vai trò quan trọng trong thiết kế và phát triển vật liệu bán dẫn và hợp kim cứng.
- Orbital nguyên tử có ứng dụng gì trong y học và công nghệ nano?
- Orbital nguyên tử được sử dụng trong chế tạo thuốc, hình ảnh y học và phát triển vật liệu nano.
Kết Luận
Orbital nguyên tử là một khái niệm nền tảng trong hóa học và vật lý, giúp chúng ta hiểu rõ hơn về cấu trúc và tính chất của vật chất. Từ việc giải thích các phản ứng hóa học đến việc phát triển công nghệ mới, orbital nguyên tử đóng vai trò không thể thiếu trong nhiều lĩnh vực khoa học và công nghệ.
Tại Xe Tải Mỹ Đình, chúng tôi tin rằng kiến thức là sức mạnh. Hiểu rõ về orbital nguyên tử không chỉ giúp bạn nắm vững kiến thức hóa học, mà còn mở ra những cơ hội khám phá và sáng tạo trong nhiều lĩnh vực khác nhau.
Bạn muốn tìm hiểu thêm về các ứng dụng của orbital nguyên tử trong lĩnh vực xe tải và vận tải? Hãy truy cập XETAIMYDINH.EDU.VN ngay hôm nay để được tư vấn và giải đáp mọi thắc mắc!
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội
Hotline: 0247 309 9988
Trang web: XETAIMYDINH.EDU.VN
