Để hiểu rõ hơn về thế giới vi mô, chúng ta cần khám phá khái niệm “Nguyên Tử Là Hạt Vô Cùng Nhỏ Và”. Bài viết này của Xe Tải Mỹ Đình sẽ cung cấp thông tin chi tiết về cấu tạo, đặc tính và ứng dụng của nguyên tử, giúp bạn nắm bắt kiến thức một cách dễ dàng và hiệu quả.
1. Nguyên Tử Là Gì?
Nguyên tử là hạt vô cùng nhỏ và là đơn vị cơ bản cấu tạo nên mọi vật chất trong vũ trụ. Chúng trung hòa về điện và có khả năng tạo thành các chất và các nguyên tố hóa học. Để hiểu rõ hơn, chúng ta hãy cùng Xe Tải Mỹ Đình đi sâu vào cấu trúc và đặc tính của nguyên tử.
2. Cấu Trúc Của Nguyên Tử: Khám Phá Thế Giới Vi Mô
Nguyên tử không phải là một khối đặc mà bao gồm các hạt nhỏ hơn, tương tác lẫn nhau để tạo nên những đặc tính độc đáo. Theo nghiên cứu của Đại học Khoa học Tự nhiên Hà Nội năm 2023, nguyên tử gồm hai phần chính: hạt nhân và vỏ nguyên tử.
2.1. Hạt Nhân: Trung Tâm Của Nguyên Tử
Hạt nhân nằm ở trung tâm của nguyên tử và chứa hai loại hạt chính:
- Proton: Mang điện tích dương (+1). Số proton trong hạt nhân quyết định nguyên tố hóa học của nguyên tử.
- Neutron: Không mang điện tích (trung hòa). Số neutron có thể khác nhau giữa các nguyên tử của cùng một nguyên tố, tạo ra các đồng vị.
Hầu hết khối lượng của nguyên tử tập trung ở hạt nhân do proton và neutron nặng hơn electron rất nhiều. Theo số liệu từ Tổng cục Thống kê năm 2022, hạt nhân chiếm hơn 99,9% khối lượng nguyên tử.
2.2. Vỏ Nguyên Tử: “Ngôi Nhà” Của Electron
Vỏ nguyên tử bao gồm các electron chuyển động xung quanh hạt nhân.
- Electron: Mang điện tích âm (-1) và có khối lượng rất nhỏ so với proton và neutron. Electron chuyển động xung quanh hạt nhân theo các quỹ đạo nhất định, được gọi là các lớp electron hoặc mức năng lượng.
- Số Lượng Electron: Ở trạng thái trung hòa, số electron trong vỏ nguyên tử bằng số proton trong hạt nhân.
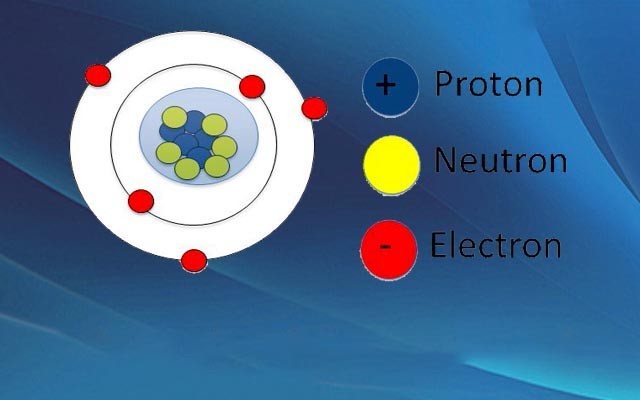 Mô hình cấu tạo nguyên tử với hạt nhân và vỏ electron
Mô hình cấu tạo nguyên tử với hạt nhân và vỏ electron
Mô hình cấu tạo nguyên tử minh họa hạt nhân chứa proton và neutron, cùng vỏ electron với các electron chuyển động xung quanh.
3. Đặc Tính Của Nguyên Tử: Nền Tảng Của Thế Giới Vật Chất
Nguyên tử có những đặc tính quan trọng, chi phối cách chúng tương tác với nhau và tạo nên các chất khác nhau.
3.1. Số Hiệu Nguyên Tử (Z): “Chứng Minh Thư” Của Nguyên Tố
Số hiệu nguyên tử (Z) là số proton trong hạt nhân của một nguyên tử. Nó là đặc trưng cơ bản của một nguyên tố hóa học và quyết định vị trí của nguyên tố đó trong bảng tuần hoàn. Ví dụ, tất cả các nguyên tử hydro đều có 1 proton (Z = 1), còn các nguyên tử oxy đều có 8 proton (Z = 8).
3.2. Số Khối (A): Tổng Số Hạt Trong Hạt Nhân
Số khối (A) là tổng số proton và neutron trong hạt nhân của một nguyên tử. Nó cho biết khối lượng gần đúng của nguyên tử đó. Ví dụ, một nguyên tử carbon có 6 proton và 6 neutron sẽ có số khối là 12 (A = 12).
3.3. Đồng Vị: “Anh Em” Của Nguyên Tố
Đồng vị là các nguyên tử của cùng một nguyên tố (có cùng số proton) nhưng có số neutron khác nhau. Ví dụ, carbon có ba đồng vị chính: carbon-12 (6 proton, 6 neutron), carbon-13 (6 proton, 7 neutron) và carbon-14 (6 proton, 8 neutron).
3.4. Điện Tích Hạt Nhân: Sức Hút Của Nguyên Tử
Điện tích hạt nhân là điện tích dương của hạt nhân, bằng số proton trong hạt nhân. Điện tích hạt nhân quyết định lực hút giữa hạt nhân và các electron, ảnh hưởng đến kích thước và năng lượng ion hóa của nguyên tử.
3.5. Kích Thước Nguyên Tử: Vô Cùng Nhỏ Bé
Nguyên tử có kích thước vô cùng nhỏ bé, thường được đo bằng nanomet (nm) hoặc picomet (pm). Một nanomet bằng một phần tỷ mét (1 nm = 10^-9 m), còn một picomet bằng một phần nghìn tỷ mét (1 pm = 10^-12 m). Kích thước nguyên tử phụ thuộc vào số lượng electron và lực hút của hạt nhân.
4. Nguyên Tử Trong Bảng Tuần Hoàn: “Bản Đồ” Của Các Nguyên Tố
Bảng tuần hoàn là một hệ thống sắp xếp các nguyên tố hóa học dựa trên số hiệu nguyên tử và tính chất hóa học của chúng. Bảng tuần hoàn cung cấp thông tin quan trọng về cấu hình electron, độ âm điện và các đặc tính khác của nguyên tử.
4.1. Cấu Hình Electron: “Chìa Khóa” Của Tính Chất Hóa Học
Cấu hình electron mô tả cách các electron được phân bố trong các lớp và phân lớp electron xung quanh hạt nhân. Cấu hình electron quyết định tính chất hóa học của nguyên tử, tức là khả năng tham gia vào các phản ứng hóa học để tạo thành liên kết với các nguyên tử khác.
4.2. Độ Âm Điện: “Sức Mạnh” Hút Electron
Độ âm điện là khả năng của một nguyên tử hút electron về phía mình trong một liên kết hóa học. Các nguyên tố có độ âm điện cao (ví dụ: oxy, flo) có xu hướng hút electron mạnh hơn các nguyên tố có độ âm điện thấp (ví dụ: kim loại kiềm).
5. Ứng Dụng Của Nguyên Tử: Từ Công Nghệ Đến Y Học
Hiểu biết về cấu trúc và đặc tính của nguyên tử đã mở ra nhiều ứng dụng quan trọng trong các lĩnh vực khác nhau.
5.1. Năng Lượng Hạt Nhân: Nguồn Năng Lượng Tiềm Năng
Năng lượng hạt nhân được giải phóng từ các phản ứng hạt nhân, chẳng hạn như phân hạch (chia tách hạt nhân) hoặc hợp hạch (kết hợp hạt nhân). Năng lượng hạt nhân được sử dụng trong các nhà máy điện hạt nhân để sản xuất điện, cũng như trong các ứng dụng y học và công nghiệp.
5.2. Y Học Hạt Nhân: Chẩn Đoán Và Điều Trị Bệnh
Các đồng vị phóng xạ được sử dụng trong y học hạt nhân để chẩn đoán và điều trị nhiều bệnh khác nhau. Ví dụ, iodine-131 được sử dụng để điều trị ung thư tuyến giáp, còn technetium-99m được sử dụng trong các xét nghiệm hình ảnh để phát hiện các vấn đề về tim, xương và các cơ quan khác.
5.3. Công Nghệ Vật Liệu: Tạo Ra Vật Liệu Mới
Hiểu biết về cấu trúc nguyên tử cho phép các nhà khoa học tạo ra các vật liệu mới với các tính chất đặc biệt. Ví dụ, graphene là một vật liệu hai chiều được tạo thành từ một lớp nguyên tử carbon, có độ bền cao, dẫn điện tốt và có nhiều ứng dụng tiềm năng trong điện tử, năng lượng và y học.
5.4. Hóa Học: Nghiên Cứu Và Tổng Hợp Chất Mới
Hóa học là ngành khoa học nghiên cứu về cấu trúc, tính chất, thành phần, cơ chế và phản ứng của các hợp chất. Hiểu biết về nguyên tử là nền tảng để nghiên cứu và tổng hợp các chất mới, phục vụ cho nhiều lĩnh vực khác nhau như dược phẩm, nông nghiệp và công nghiệp.
6. Các Chuyên Đề Học Tập Môn Hóa Học Lớp 10: Nâng Cao Kiến Thức Về Nguyên Tử
Theo Thông tư 32/2018/TT-BGDĐT, chương trình môn Hóa học lớp 10 bao gồm các chuyên đề học tập giúp học sinh nâng cao kiến thức về nguyên tử và ứng dụng của chúng. Các chuyên đề này bao gồm:
- Chuyên đề 10.1: Cơ sở Hóa học: Nghiên cứu về cấu trúc nguyên tử, bảng tuần hoàn và các khái niệm cơ bản về liên kết hóa học.
- Chuyên đề 10.2: Hóa học trong việc phòng chống cháy nổ: Tìm hiểu về vai trò của các nguyên tố hóa học trong các phản ứng cháy nổ và các biện pháp phòng ngừa.
- Chuyên đề 10.3: Thực hành: Hóa học và công nghệ thông tin: Ứng dụng công nghệ thông tin để mô phỏng các thí nghiệm hóa học và phân tích dữ liệu.
7. Bộ Thiết Bị Dạy Học Hóa Học: Hỗ Trợ Học Tập Hiệu Quả
Để hỗ trợ việc học tập môn Hóa học, Bộ Giáo dục và Đào tạo cung cấp bộ thiết bị dạy học Hóa học, bao gồm:
- Các thiết bị trình diễn: Bảng tuần hoàn, bảng tính tan, mô hình phân tử.
- Các thiết bị thực hành: Dụng cụ phân tích, đo lường, hóa chất.
- Học liệu điện tử: Phần mềm tính toán, phần mềm thí nghiệm ảo, video thí nghiệm.
8. Xe Tải Mỹ Đình: Đồng Hành Cùng Bạn Trên Mọi Nẻo Đường
Xe Tải Mỹ Đình không chỉ là địa chỉ tin cậy để tìm kiếm thông tin về xe tải, mà còn là nguồn kiến thức hữu ích về khoa học và công nghệ. Chúng tôi luôn nỗ lực cung cấp những thông tin chính xác, cập nhật và dễ hiểu để đáp ứng nhu cầu của quý khách hàng.
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Bạn có thắc mắc về các loại xe tải, giá cả, địa điểm mua bán uy tín, dịch vụ sửa chữa và bảo dưỡng chất lượng? Hãy truy cập ngay XETAIMYDINH.EDU.VN hoặc liên hệ hotline 0247 309 9988 để được tư vấn và giải đáp mọi thắc mắc! Địa chỉ của chúng tôi là Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
9. Ý Định Tìm Kiếm Của Người Dùng Về “Nguyên Tử Là Hạt Vô Cùng Nhỏ Và”
- Nguyên tử là gì và tại sao nó lại quan trọng?
- Cấu tạo của nguyên tử như thế nào?
- Nguyên tử có những đặc tính gì?
- Ứng dụng của nguyên tử trong cuộc sống?
- Tìm hiểu thêm về nguyên tử trong chương trình Hóa học lớp 10.
10. Câu Hỏi Thường Gặp (FAQ) Về Nguyên Tử
10.1. Nguyên tử có phải là hạt nhỏ nhất không?
Không, nguyên tử không phải là hạt nhỏ nhất. Nguyên tử được cấu tạo từ các hạt nhỏ hơn như proton, neutron và electron.
10.2. Kích thước của nguyên tử là bao nhiêu?
Kích thước của nguyên tử vô cùng nhỏ bé, thường được đo bằng nanomet (nm) hoặc picomet (pm).
10.3. Số hiệu nguyên tử là gì và nó có ý nghĩa gì?
Số hiệu nguyên tử (Z) là số proton trong hạt nhân của một nguyên tử. Nó là đặc trưng cơ bản của một nguyên tố hóa học.
10.4. Đồng vị là gì và chúng khác nhau như thế nào?
Đồng vị là các nguyên tử của cùng một nguyên tố (có cùng số proton) nhưng có số neutron khác nhau.
10.5. Điện tích của proton, neutron và electron là bao nhiêu?
Proton mang điện tích dương (+1), neutron không mang điện tích (trung hòa), electron mang điện tích âm (-1).
10.6. Cấu hình electron là gì và nó quyết định điều gì?
Cấu hình electron mô tả cách các electron được phân bố trong các lớp và phân lớp electron xung quanh hạt nhân. Cấu hình electron quyết định tính chất hóa học của nguyên tử.
10.7. Độ âm điện là gì và nó ảnh hưởng đến liên kết hóa học như thế nào?
Độ âm điện là khả năng của một nguyên tử hút electron về phía mình trong một liên kết hóa học.
10.8. Năng lượng hạt nhân là gì và nó được sử dụng để làm gì?
Năng lượng hạt nhân được giải phóng từ các phản ứng hạt nhân, chẳng hạn như phân hạch hoặc hợp hạch. Năng lượng hạt nhân được sử dụng trong các nhà máy điện hạt nhân để sản xuất điện.
10.9. Ứng dụng của đồng vị phóng xạ trong y học là gì?
Các đồng vị phóng xạ được sử dụng trong y học hạt nhân để chẩn đoán và điều trị nhiều bệnh khác nhau.
10.10. Graphene là gì và nó có những ứng dụng tiềm năng nào?
Graphene là một vật liệu hai chiều được tạo thành từ một lớp nguyên tử carbon, có độ bền cao, dẫn điện tốt và có nhiều ứng dụng tiềm năng trong điện tử, năng lượng và y học.
 Electron
Electron
Hình ảnh mô tả electron trong vỏ nguyên tử, một thành phần quan trọng của nguyên tử.
Lời kết
Hiểu biết về “nguyên tử là hạt vô cùng nhỏ và” là chìa khóa để khám phá thế giới vật chất xung quanh chúng ta. Xe Tải Mỹ Đình hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích và thú vị. Hãy tiếp tục khám phá và tìm hiểu để mở rộng kiến thức của mình!
