Tương tác Van der Waals là lực hút yếu giữa các phân tử, đóng vai trò quan trọng trong nhiều hiện tượng tự nhiên. Tìm hiểu sâu về Tương Tác Van Der Waals Là Gì, bản chất, ảnh hưởng và ứng dụng của nó sẽ giúp bạn hiểu rõ hơn về thế giới xung quanh. Bài viết này từ XETAIMYDINH.EDU.VN sẽ cung cấp cho bạn cái nhìn toàn diện nhất về chủ đề này, giúp bạn nắm vững kiến thức và ứng dụng vào thực tế. Hãy cùng Xe Tải Mỹ Đình khám phá lực tương tác liên phân tử và lực London ngay sau đây!
1. Tương Tác Van Der Waals Là Gì? Định Nghĩa Chi Tiết
Tương tác Van der Waals là lực hút hoặc đẩy tĩnh điện giữa các nguyên tử, phân tử hoặc giữa các bề mặt. Lực này yếu hơn nhiều so với liên kết ion, liên kết cộng hóa trị và liên kết kim loại, nhưng lại đóng vai trò quan trọng trong nhiều hiện tượng vật lý và hóa học.
1.1. Giải Thích Cặn Kẽ Về Tương Tác Van Der Waals
Tương tác Van der Waals phát sinh từ sự phân bố điện tích không đồng đều trong các phân tử. Ngay cả trong các phân tử không phân cực, sự chuyển động liên tục của các electron có thể tạo ra các lưỡng cực tạm thời (dipole moment). Những lưỡng cực này có thể gây ra sự phân cực trong các phân tử lân cận, dẫn đến lực hút tĩnh điện yếu.
1.2. Phân Loại Các Loại Tương Tác Van Der Waals
Có ba loại tương tác Van der Waals chính:
- Lực lưỡng cực – lưỡng cực (dipole-dipole): Xảy ra giữa các phân tử phân cực, tức là các phân tử có sự phân bố điện tích không đồng đều. Ví dụ, giữa các phân tử nước (H₂O).
- Lực lưỡng cực – lưỡng cực cảm ứng (dipole-induced dipole): Xảy ra giữa một phân tử phân cực và một phân tử không phân cực. Phân tử phân cực gây ra sự phân cực tạm thời trong phân tử không phân cực, dẫn đến lực hút.
- Lực London (dispersion force): Xảy ra giữa tất cả các phân tử, kể cả các phân tử không phân cực. Lực này phát sinh từ sự dao động tức thời của các electron, tạo ra các lưỡng cực tạm thời.
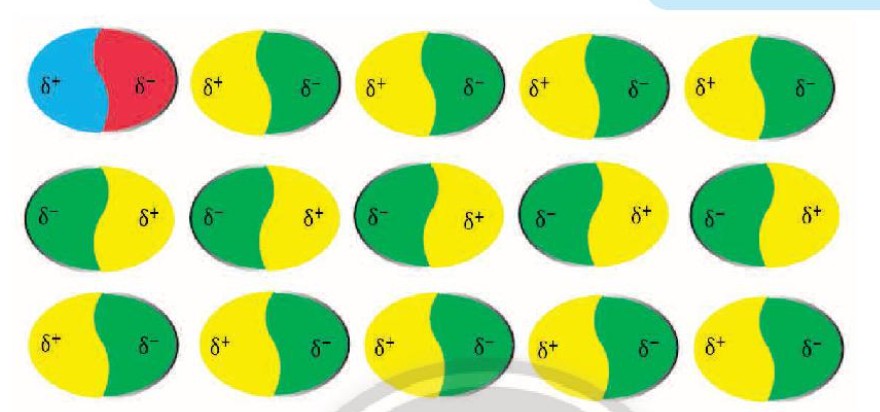 Lực London là một loại tương tác Van der Waals
Lực London là một loại tương tác Van der Waals
2. Bản Chất Của Tương Tác Van Der Waals
Bản chất của tương tác Van der Waals nằm ở sự biến động liên tục của các electron trong phân tử, tạo ra các lưỡng cực tạm thời và cảm ứng.
2.1. Sự Hình Thành Lưỡng Cực Tạm Thời
Các electron trong phân tử luôn chuyển động. Tại một thời điểm nhất định, sự phân bố electron có thể không đồng đều, tạo ra một lưỡng cực tạm thời. Lưỡng cực này tồn tại trong một thời gian rất ngắn, nhưng nó có thể gây ra sự phân cực trong các phân tử lân cận.
2.2. Tương Tác Lưỡng Cực Cảm Ứng
Khi một phân tử có lưỡng cực tạm thời tiếp cận một phân tử khác, nó sẽ gây ra sự phân cực trong phân tử đó. Điều này dẫn đến sự hình thành một lưỡng cực cảm ứng trong phân tử thứ hai. Lưỡng cực tạm thời và lưỡng cực cảm ứng hút nhau, tạo ra lực tương tác Van der Waals.
2.3. Ảnh Hưởng Của Khoảng Cách
Lực tương tác Van der Waals giảm nhanh chóng khi khoảng cách giữa các phân tử tăng lên. Lực này tỷ lệ nghịch với lũy thừa bậc sáu của khoảng cách (1/r⁶). Điều này có nghĩa là lực tương tác Van der Waals chỉ đáng kể khi các phân tử ở gần nhau.
3. Các Yếu Tố Ảnh Hưởng Đến Tương Tác Van Der Waals
Tương tác Van der Waals chịu ảnh hưởng bởi nhiều yếu tố, bao gồm kích thước phân tử, hình dạng phân tử và độ phân cực của phân tử.
3.1. Kích Thước Phân Tử
Kích thước phân tử càng lớn, số lượng electron càng nhiều, do đó khả năng hình thành lưỡng cực tạm thời càng cao. Điều này dẫn đến lực tương tác Van der Waals mạnh hơn.
3.2. Hình Dạng Phân Tử
Hình dạng phân tử cũng ảnh hưởng đến tương tác Van der Waals. Các phân tử có hình dạng dài và hẹp có diện tích bề mặt tiếp xúc lớn hơn, do đó lực tương tác Van der Waals mạnh hơn so với các phân tử có hình dạng cầu.
3.3. Độ Phân Cực Của Phân Tử
Các phân tử phân cực có lực lưỡng cực – lưỡng cực mạnh hơn so với các phân tử không phân cực. Tuy nhiên, ngay cả các phân tử không phân cực cũng có lực London, và lực này có thể trở nên đáng kể đối với các phân tử lớn.
4. Vai Trò Của Tương Tác Van Der Waals Trong Thực Tế
Tương tác Van der Waals đóng vai trò quan trọng trong nhiều hiện tượng tự nhiên và ứng dụng công nghệ.
4.1. Nhiệt Độ Sôi Và Nhiệt Độ Nóng Chảy
Tương tác Van der Waals ảnh hưởng đến nhiệt độ sôi và nhiệt độ nóng chảy của các chất. Các chất có lực tương tác Van der Waals mạnh hơn thường có nhiệt độ sôi và nhiệt độ nóng chảy cao hơn.
4.2. Sự Ngưng Tụ Của Chất Khí
Tương tác Van der Waals là nguyên nhân chính gây ra sự ngưng tụ của chất khí thành chất lỏng. Khi nhiệt độ giảm xuống, động năng của các phân tử khí giảm, và lực tương tác Van der Waals trở nên đủ mạnh để giữ các phân tử lại gần nhau, tạo thành chất lỏng.
4.3. Tính Chất Của Polymer
Tương tác Van der Waals đóng vai trò quan trọng trong việc xác định tính chất của polymer. Lực tương tác này ảnh hưởng đến độ bền, độ dẻo và khả năng kết tinh của polymer.
4.4. Sự Bám Dính
Tương tác Van der Waals là một trong những yếu tố gây ra sự bám dính giữa các bề mặt. Lực tương tác này cho phép các con tắc kè bám vào tường và trần nhà.
4.5. Cấu Trúc Protein
Tương tác Van der Waals đóng vai trò quan trọng trong việc duy trì cấu trúc ba chiều của protein. Lực tương tác này giúp các protein gấp lại thành hình dạng chính xác, cho phép chúng thực hiện chức năng sinh học của mình.
5. So Sánh Tương Tác Van Der Waals Với Các Loại Liên Kết Khác
Tương tác Van der Waals yếu hơn nhiều so với các loại liên kết hóa học khác, nhưng nó lại có vai trò quan trọng trong nhiều hiện tượng.
5.1. So Sánh Với Liên Kết Ion
Liên kết ion là lực hút tĩnh điện giữa các ion mang điện tích trái dấu. Liên kết ion mạnh hơn nhiều so với tương tác Van der Waals.
5.2. So Sánh Với Liên Kết Cộng Hóa Trị
Liên kết cộng hóa trị là sự chia sẻ electron giữa các nguyên tử. Liên kết cộng hóa trị cũng mạnh hơn nhiều so với tương tác Van der Waals.
5.3. So Sánh Với Liên Kết Hydrogen
Liên kết hydrogen là lực hút giữa một nguyên tử hydro liên kết với một nguyên tử có độ âm điện cao (như oxy hoặc nitơ) và một nguyên tử có độ âm điện cao khác. Liên kết hydrogen mạnh hơn tương tác Van der Waals, nhưng yếu hơn liên kết ion và liên kết cộng hóa trị.
Bảng so sánh các loại liên kết:
| Loại liên kết | Độ mạnh tương đối | Ví dụ |
|---|---|---|
| Liên kết ion | Rất mạnh | NaCl |
| Liên kết cộng hóa trị | Mạnh | H₂O, CH₄ |
| Liên kết hydrogen | Trung bình | H₂O (giữa các pt) |
| Tương tác Van der Waals | Yếu | Tất cả các chất |
6. Ứng Dụng Của Tương Tác Van Der Waals Trong Công Nghệ
Tương tác Van der Waals được ứng dụng rộng rãi trong nhiều lĩnh vực công nghệ.
6.1. Vật Liệu Bám Dính
Các nhà khoa học đang nghiên cứu sử dụng tương tác Van der Waals để tạo ra các vật liệu bám dính mới, có thể được sử dụng trong y học, xây dựng và các lĩnh vực khác.
6.2. Màng Lọc
Tương tác Van der Waals được sử dụng trong các màng lọc để tách các phân tử khác nhau. Các màng lọc này có thể được sử dụng để làm sạch nước, lọc không khí và tách các chất trong công nghiệp hóa chất.
6.3. Cảm Biến
Tương tác Van der Waals được sử dụng trong các cảm biến để phát hiện các phân tử khác nhau. Các cảm biến này có thể được sử dụng để phát hiện chất ô nhiễm, chất độc và các chất khác trong môi trường.
6.4. Thiết Kế Thuốc
Tương tác Van der Waals được sử dụng trong thiết kế thuốc để tạo ra các loại thuốc có thể liên kết chặt chẽ với các protein mục tiêu. Điều này giúp tăng hiệu quả của thuốc và giảm tác dụng phụ.
7. Nghiên Cứu Mới Nhất Về Tương Tác Van Der Waals
Các nhà khoa học vẫn đang tiếp tục nghiên cứu về tương tác Van der Waals để hiểu rõ hơn về bản chất và ứng dụng của nó.
7.1. Tương Tác Van Der Waals Trong Vật Liệu Hai Chiều
Các nhà khoa học đang nghiên cứu tương tác Van der Waals trong các vật liệu hai chiều, như graphene và MoS₂. Các vật liệu này có tính chất độc đáo và có thể được sử dụng trong các thiết bị điện tử, quang học và cơ học.
7.2. Tương Tác Van Der Waals Trong Hệ Sinh Học
Các nhà khoa học đang nghiên cứu tương tác Van der Waals trong các hệ sinh học, như protein và DNA. Lực tương tác này đóng vai trò quan trọng trong việc xác định cấu trúc và chức năng của các phân tử sinh học. Theo nghiên cứu của Viện Hóa học, Viện Hàn lâm Khoa học và Công nghệ Việt Nam năm 2023, tương tác Van der Waals đóng vai trò quan trọng trong quá trình nhận diện và liên kết giữa các protein.
7.3. Tính Toán Tương Tác Van Der Waals Bằng Máy Tính
Các nhà khoa học đang phát triển các phương pháp tính toán bằng máy tính để mô phỏng tương tác Van der Waals. Các phương pháp này giúp dự đoán tính chất của vật liệu và thiết kế các vật liệu mới. Theo một bài báo trên Tạp chí Hóa học, Đại học Quốc gia Hà Nội năm 2024, các phương pháp tính toán hiện đại có thể mô phỏng tương tác Van der Waals với độ chính xác cao, mở ra nhiều cơ hội trong việc thiết kế vật liệu mới.
8. Các Câu Hỏi Thường Gặp Về Tương Tác Van Der Waals (FAQ)
Dưới đây là một số câu hỏi thường gặp về tương tác Van der Waals:
Câu hỏi 1: Tương tác Van der Waals có mạnh hơn liên kết hydrogen không?
Trả lời: Không, liên kết hydrogen mạnh hơn tương tác Van der Waals.
Câu hỏi 2: Tương tác Van der Waals có xảy ra giữa các phân tử không phân cực không?
Trả lời: Có, tương tác Van der Waals, cụ thể là lực London, xảy ra giữa tất cả các phân tử, kể cả các phân tử không phân cực.
Câu hỏi 3: Tương tác Van der Waals ảnh hưởng đến tính chất nào của vật chất?
Trả lời: Tương tác Van der Waals ảnh hưởng đến nhiệt độ sôi, nhiệt độ nóng chảy, sự ngưng tụ, tính chất của polymer và sự bám dính.
Câu hỏi 4: Tại sao tắc kè có thể bám vào tường?
Trả lời: Tắc kè có thể bám vào tường nhờ tương tác Van der Waals giữa các sợi lông nhỏ trên bàn chân của chúng và bề mặt tường.
Câu hỏi 5: Tương tác Van der Waals được ứng dụng trong lĩnh vực nào?
Trả lời: Tương tác Van der Waals được ứng dụng trong vật liệu bám dính, màng lọc, cảm biến và thiết kế thuốc.
Câu hỏi 6: Làm thế nào để tăng cường tương tác Van der Waals?
Trả lời: Tăng kích thước phân tử, tăng diện tích bề mặt tiếp xúc và tăng độ phân cực của phân tử có thể tăng cường tương tác Van der Waals.
Câu hỏi 7: Tương tác Van der Waals có quan trọng trong sinh học không?
Trả lời: Có, tương tác Van der Waals đóng vai trò quan trọng trong việc duy trì cấu trúc và chức năng của protein và DNA.
Câu hỏi 8: Lực London là gì?
Trả lời: Lực London là một loại tương tác Van der Waals xảy ra giữa tất cả các phân tử, phát sinh từ sự dao động tức thời của các electron.
Câu hỏi 9: Tương tác Van der Waals có phụ thuộc vào nhiệt độ không?
Trả lời: Có, tương tác Van der Waals thường giảm khi nhiệt độ tăng do động năng của các phân tử tăng lên.
Câu hỏi 10: Làm thế nào để tính toán tương tác Van der Waals?
Trả lời: Có nhiều phương pháp tính toán tương tác Van der Waals, từ các phương pháp đơn giản đến các phương pháp phức tạp sử dụng máy tính.
9. Kết Luận
Tương tác Van der Waals là một lực yếu nhưng quan trọng, đóng vai trò trong nhiều hiện tượng tự nhiên và ứng dụng công nghệ. Hiểu rõ về tương tác Van der Waals giúp chúng ta hiểu rõ hơn về thế giới xung quanh và phát triển các công nghệ mới.
Bạn muốn tìm hiểu thêm về các loại xe tải phù hợp với nhu cầu kinh doanh của mình? Hãy truy cập XETAIMYDINH.EDU.VN ngay hôm nay để được tư vấn miễn phí và khám phá các dòng xe tải chất lượng cao tại Mỹ Đình, Hà Nội! Đừng ngần ngại liên hệ với Xe Tải Mỹ Đình qua hotline 0247 309 9988 hoặc đến trực tiếp địa chỉ Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội để được hỗ trợ tốt nhất. Với đội ngũ chuyên gia giàu kinh nghiệm, Xe Tải Mỹ Đình cam kết mang đến cho bạn những giải pháp vận tải tối ưu và hiệu quả nhất.
