Bạn đang tìm hiểu về phản ứng hóa học của sắt (Fe) và muốn biết Kim Loại Fe Không Phản ứng Với dung dịch nào? Bài viết này của Xe Tải Mỹ Đình – XETAIMYDINH.EDU.VN sẽ cung cấp thông tin chi tiết, chính xác và dễ hiểu về tính chất hóa học của sắt, giúp bạn nắm vững kiến thức và áp dụng vào giải bài tập một cách hiệu quả. Chúng tôi sẽ khám phá các dung dịch mà sắt không phản ứng và lý do tại sao, đồng thời đưa ra những ví dụ minh họa và bài tập vận dụng để bạn thực hành.
1. Kim Loại Fe Không Phản Ứng Với Dung Dịch Nào?
Kim loại sắt (Fe) không phản ứng với dung dịch ZnCl2.
Giải thích: Theo quy tắc α (anpha) trong hóa học, một kim loại chỉ có thể đẩy kim loại đứng sau nó ra khỏi dung dịch muối. Sắt (Fe) đứng sau kẽm (Zn) trong dãy điện hóa, do đó không thể phản ứng với dung dịch ZnCl2 để tạo thành muối sắt và kim loại kẽm.
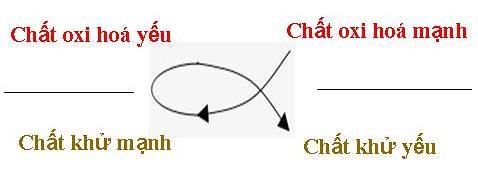 Quy tắc anpha
Quy tắc anpha
Alt: Quy tắc alpha trong phản ứng hóa học, kim loại Fe không phản ứng với dung dịch ZnCl2
1.1. Dãy Điện Hóa Của Kim Loại
Dãy điện hóa của kim loại là một dãy sắp xếp các kim loại theo thứ tự tăng dần tính khử (khả năng nhường electron) và giảm dần tính oxy hóa (khả năng nhận electron) của ion kim loại. Dãy điện hóa giúp ta dự đoán được khả năng phản ứng giữa kim loại và dung dịch muối.
- Dãy điện hóa (dạng đơn giản): K > Na > Mg > Al > Zn > Fe > Ni > Sn > Pb > H > Cu > Ag > Au
- Ý nghĩa: Kim loại đứng trước có thể đẩy kim loại đứng sau ra khỏi dung dịch muối (trừ các kim loại kiềm và kiềm thổ phản ứng với nước).
Ví dụ:
- Fe + CuSO4 → FeSO4 + Cu (Sắt đẩy đồng ra khỏi dung dịch đồng sunfat)
- Zn + FeSO4 → ZnSO4 + Fe (Kẽm đẩy sắt ra khỏi dung dịch sắt sunfat)
1.2. Tại Sao Fe Không Phản Ứng Với ZnCl2?
Trong trường hợp Fe và ZnCl2, ta có:
- Fe đứng sau Zn trong dãy điện hóa.
- Tính khử của Fe yếu hơn Zn.
Do đó, Fe không đủ khả năng khử Zn2+ thành Zn. Phản ứng không xảy ra.
Fe + ZnCl2 → Không phản ứng
2. Tính Chất Hóa Học Của Sắt (Fe) Cần Biết
Để hiểu rõ hơn về khả năng phản ứng của sắt, chúng ta cần nắm vững các tính chất hóa học cơ bản của nó. Sắt là một kim loại có nhiều ứng dụng quan trọng trong đời sống và công nghiệp.
2.1. Tác Dụng Với Phi Kim
Sắt có thể tác dụng với nhiều phi kim khác nhau, đặc biệt là khi đun nóng.
2.1.1. Với Oxi (O2)
Khi đun nóng, sắt tác dụng với oxi tạo thành oxit sắt từ (Fe3O4), là một oxit hỗn hợp của FeO và Fe2O3.
Phương trình phản ứng:
3Fe + 2O2 → Fe3O4
2.1.2. Với Clo (Cl2)
Sắt tác dụng với clo tạo thành sắt(III) clorua (FeCl3).
Phương trình phản ứng:
2Fe + 3Cl2 → 2FeCl3
Alt: Phương trình phản ứng sắt tác dụng với clo tạo thành FeCl3
2.1.3. Với Lưu Huỳnh (S)
Sắt tác dụng với lưu huỳnh tạo thành sắt(II) sunfua (FeS).
Phương trình phản ứng:
Fe + S → FeS
2.2. Tác Dụng Với Axit
Sắt có thể tác dụng với nhiều loại axit khác nhau, nhưng sản phẩm tạo thành phụ thuộc vào loại axit và điều kiện phản ứng.
2.2.1. Với Axit Clohidric (HCl) và Axit Sunfuric Loãng (H2SO4)
Sắt tác dụng với HCl và H2SO4 loãng tạo thành muối sắt(II) và giải phóng khí hidro.
Phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2
Fe + H2SO4 → FeSO4 + H2
2.2.2. Với Axit Nitric (HNO3) và Axit Sunfuric Đặc, Nóng (H2SO4 đặc, nóng)
Sắt không phản ứng với HNO3 đặc, nguội và H2SO4 đặc, nguội vì bị thụ động hóa. Tuy nhiên, khi đun nóng, sắt có thể phản ứng với các axit này tạo thành muối sắt(III), nước và các sản phẩm khử khác như SO2 hoặc NO2.
Phương trình phản ứng:
Fe + 6HNO3 (đặc, nóng) → Fe(NO3)3 + 3NO2 + 3H2O
2Fe + 6H2SO4 (đặc, nóng) → Fe2(SO4)3 + 3SO2 + 6H2O
2.3. Tác Dụng Với Dung Dịch Muối
Sắt có thể tác dụng với dung dịch muối của các kim loại đứng sau nó trong dãy điện hóa.
Ví dụ:
Fe + CuSO4 → FeSO4 + Cu
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
3. Các Trường Hợp Đặc Biệt Cần Lưu Ý
Trong quá trình học tập và làm bài tập, có một số trường hợp đặc biệt liên quan đến phản ứng của sắt mà bạn cần lưu ý để tránh sai sót.
3.1. Hiện Tượng Thụ Động Hóa
Sắt bị thụ động hóa khi tác dụng với HNO3 đặc, nguội và H2SO4 đặc, nguội. Hiện tượng này xảy ra do sự tạo thành một lớp oxit mỏng trên bề mặt kim loại, ngăn cản phản ứng tiếp tục xảy ra.
3.2. Phản Ứng Với Muối Sắt(III)
Sắt có thể phản ứng với muối sắt(III) để tạo thành muối sắt(II).
Phương trình phản ứng:
Fe + 2FeCl3 → 3FeCl2
3.3. Tính Khử Của Sắt
Sắt có tính khử trung bình, có thể bị oxi hóa thành ion Fe2+ hoặc Fe3+ tùy thuộc vào điều kiện phản ứng.
4. Bài Tập Vận Dụng Về Phản Ứng Của Sắt
Để củng cố kiến thức, chúng ta cùng làm một số bài tập vận dụng sau đây:
Câu 1: Cho các dung dịch sau: ZnCl2, CuSO4, AgNO3, HCl. Sắt có thể phản ứng với bao nhiêu dung dịch trong số các dung dịch trên?
Đáp án: 3 dung dịch (CuSO4, AgNO3, HCl).
Giải thích:
- Fe không phản ứng với ZnCl2.
- Fe + CuSO4 → FeSO4 + Cu
- Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
- Fe + 2HCl → FeCl2 + H2
Câu 2: Ngâm một lá sắt trong dung dịch CuSO4. Sau một thời gian, lấy lá sắt ra, rửa sạch, làm khô và cân thấy khối lượng lá sắt tăng lên 1,6 gam. Tính khối lượng đồng bám vào lá sắt.
Giải:
Phương trình phản ứng: Fe + CuSO4 → FeSO4 + Cu
Gọi x là số mol Fe phản ứng. Theo phương trình, số mol Cu tạo thành cũng là x.
Độ tăng khối lượng của lá sắt là: 64x – 56x = 1.6
=> 8x = 1.6
=> x = 0.2 mol
Khối lượng đồng bám vào lá sắt là: 64 * 0.2 = 12.8 gam.
Câu 3: Cho 5,6 gam sắt tác dụng hoàn toàn với dung dịch HCl dư. Tính thể tích khí hidro thu được ở điều kiện tiêu chuẩn.
Giải:
Phương trình phản ứng: Fe + 2HCl → FeCl2 + H2
Số mol Fe phản ứng là: 5.6 / 56 = 0.1 mol
Theo phương trình, số mol H2 thu được là 0.1 mol.
Thể tích khí H2 thu được ở điều kiện tiêu chuẩn là: 0.1 * 22.4 = 2.24 lít.
5. Ứng Dụng Của Sắt Trong Đời Sống Và Công Nghiệp
Sắt là một kim loại có nhiều ứng dụng quan trọng trong đời sống và công nghiệp.
5.1. Trong Xây Dựng
Sắt là thành phần chính của thép, một vật liệu xây dựng quan trọng được sử dụng rộng rãi trong các công trình cầu đường, nhà cao tầng, và các công trình công nghiệp.
5.2. Trong Giao Thông Vận Tải
Sắt được sử dụng để sản xuất ô tô, tàu hỏa, tàu thủy và các phương tiện giao thông khác.
Alt: Ứng dụng của sắt trong giao thông vận tải, sản xuất ô tô
5.3. Trong Sản Xuất Máy Móc
Sắt là vật liệu quan trọng để sản xuất các loại máy móc, thiết bị công nghiệp và nông nghiệp.
5.4. Trong Y Học
Sắt là một nguyên tố vi lượng cần thiết cho cơ thể, tham gia vào quá trình tạo máu. Các chế phẩm chứa sắt được sử dụng để điều trị thiếu máu do thiếu sắt.
6. So Sánh Phản Ứng Của Sắt Với Các Kim Loại Khác
Để hiểu rõ hơn về tính chất hóa học của sắt, chúng ta cùng so sánh phản ứng của sắt với một số kim loại khác.
6.1. So Sánh Với Kẽm (Zn)
- Tính khử: Zn có tính khử mạnh hơn Fe.
- Phản ứng với axit: Cả Zn và Fe đều phản ứng với HCl và H2SO4 loãng, nhưng Zn phản ứng mạnh hơn.
- Phản ứng với dung dịch muối: Zn có thể đẩy Fe ra khỏi dung dịch muối, nhưng Fe không thể đẩy Zn ra khỏi dung dịch muối.
6.2. So Sánh Với Đồng (Cu)
- Tính khử: Fe có tính khử mạnh hơn Cu.
- Phản ứng với axit: Cu không phản ứng với HCl và H2SO4 loãng, nhưng Fe có phản ứng.
- Phản ứng với dung dịch muối: Fe có thể đẩy Cu ra khỏi dung dịch muối, nhưng Cu không thể đẩy Fe ra khỏi dung dịch muối.
| Tính Chất | Sắt (Fe) | Kẽm (Zn) | Đồng (Cu) |
|---|---|---|---|
| Tính Khử | Trung bình | Mạnh | Yếu |
| P/Ư với HCl, H2SO4 loãng | Có | Có, mạnh hơn Fe | Không |
| P/Ư với muối | Đẩy kim loại đứng sau ra khỏi dung dịch muối | Đẩy được nhiều kim loại hơn Fe | Không đẩy được Fe ra khỏi dung dịch muối |
7. Những Lưu Ý Khi Làm Bài Tập Về Sắt
Khi làm bài tập về sắt, bạn cần lưu ý một số điểm sau:
- Nắm vững dãy điện hóa của kim loại: Dãy điện hóa giúp bạn dự đoán khả năng phản ứng giữa kim loại và dung dịch muối.
- Nhớ các phản ứng đặc trưng của sắt: Sắt có nhiều phản ứng đặc trưng, như phản ứng với phi kim, axit, và dung dịch muối.
- Lưu ý hiện tượng thụ động hóa: Sắt bị thụ động hóa khi tác dụng với HNO3 đặc, nguội và H2SO4 đặc, nguội.
- Cân bằng phương trình hóa học: Cân bằng phương trình hóa học giúp bạn tính toán chính xác số mol các chất tham gia và tạo thành trong phản ứng.
8. Tổng Kết
Qua bài viết này, chúng ta đã tìm hiểu chi tiết về câu hỏi “Kim loại Fe không phản ứng với dung dịch nào?”. Sắt không phản ứng với dung dịch ZnCl2 do vị trí của nó trong dãy điện hóa. Đồng thời, chúng ta cũng đã khám phá các tính chất hóa học quan trọng của sắt, các trường hợp đặc biệt cần lưu ý, và các bài tập vận dụng để củng cố kiến thức.
Hy vọng rằng, với những kiến thức và thông tin mà Xe Tải Mỹ Đình – XETAIMYDINH.EDU.VN cung cấp, bạn sẽ tự tin hơn trong việc học tập và giải quyết các bài tập liên quan đến sắt. Nếu bạn có bất kỳ thắc mắc nào, đừng ngần ngại liên hệ với chúng tôi để được tư vấn và giải đáp.
9. Câu Hỏi Thường Gặp (FAQ) Về Phản Ứng Của Sắt
9.1. Tại sao sắt không phản ứng với axit nitric đặc nguội?
Sắt không phản ứng với axit nitric đặc nguội do hiện tượng thụ động hóa. Axit nitric đặc nguội tạo ra một lớp oxit mỏng bảo vệ trên bề mặt sắt, ngăn chặn phản ứng tiếp tục xảy ra.
9.2. Sắt có phản ứng với dung dịch muối của kim loại nào?
Sắt có thể phản ứng với dung dịch muối của các kim loại đứng sau nó trong dãy điện hóa, ví dụ như CuSO4, AgNO3, Pb(NO3)2.
9.3. Sản phẩm của phản ứng giữa sắt và axit clohidric là gì?
Sản phẩm của phản ứng giữa sắt và axit clohidric là sắt(II) clorua (FeCl2) và khí hidro (H2).
9.4. Sắt có thể tác dụng với clo không? Nếu có, sản phẩm là gì?
Có, sắt tác dụng với clo tạo thành sắt(III) clorua (FeCl3).
9.5. Hiện tượng gì xảy ra khi ngâm một lá sắt vào dung dịch đồng sunfat?
Khi ngâm một lá sắt vào dung dịch đồng sunfat, lá sắt sẽ bị ăn mòn, có một lớp đồng màu đỏ bám lên bề mặt lá sắt, và dung dịch đồng sunfat màu xanh lam sẽ nhạt dần.
9.6. Sắt có phản ứng với dung dịch sắt(III) clorua không? Nếu có, sản phẩm là gì?
Có, sắt phản ứng với dung dịch sắt(III) clorua tạo thành sắt(II) clorua (FeCl2).
9.7. Tại sao cần lưu ý hiện tượng thụ động hóa của sắt?
Cần lưu ý hiện tượng thụ động hóa của sắt để tránh sai sót khi dự đoán khả năng phản ứng của sắt với các chất khác, đặc biệt là với axit nitric đặc nguội và axit sulfuric đặc nguội.
9.8. Sắt có vai trò gì trong cơ thể con người?
Sắt là một nguyên tố vi lượng cần thiết cho cơ thể, tham gia vào quá trình tạo máu, vận chuyển oxy, và nhiều quá trình sinh hóa quan trọng khác.
9.9. Ứng dụng quan trọng nhất của sắt trong công nghiệp là gì?
Ứng dụng quan trọng nhất của sắt trong công nghiệp là sản xuất thép, một vật liệu xây dựng và chế tạo quan trọng.
9.10. Làm thế nào để bảo quản các vật dụng bằng sắt khỏi bị gỉ sét?
Để bảo quản các vật dụng bằng sắt khỏi bị gỉ sét, có thể áp dụng các biện pháp như sơn phủ, mạ kẽm, hoặc sử dụng các chất ức chế ăn mòn.
10. Liên Hệ Với Xe Tải Mỹ Đình Để Được Tư Vấn
Bạn đang gặp khó khăn trong việc tìm kiếm thông tin về xe tải, giá cả, thủ tục mua bán, hoặc các dịch vụ sửa chữa xe tải uy tín tại khu vực Mỹ Đình, Hà Nội? Xe Tải Mỹ Đình – XETAIMYDINH.EDU.VN là địa chỉ tin cậy, nơi bạn có thể tìm thấy mọi thông tin cần thiết và được tư vấn tận tình bởi đội ngũ chuyên gia giàu kinh nghiệm.
Chúng tôi cam kết cung cấp:
- Thông tin chi tiết và cập nhật về các loại xe tải có sẵn trên thị trường.
- So sánh giá cả và thông số kỹ thuật giữa các dòng xe khác nhau.
- Tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách của bạn.
- Giải đáp mọi thắc mắc liên quan đến thủ tục mua bán, đăng ký, bảo dưỡng xe tải.
- Thông tin về các dịch vụ sửa chữa xe tải uy tín trong khu vực Mỹ Đình.
Hãy truy cập ngay XETAIMYDINH.EDU.VN hoặc liên hệ với chúng tôi qua:
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
- Hotline: 0247 309 9988
Xe Tải Mỹ Đình – Luôn đồng hành cùng bạn trên mọi nẻo đường!

