Năng Lượng Hoạt Hóa Của Phản ứng Hóa Học chính là chìa khóa để hiểu rõ tốc độ và khả năng xảy ra của các phản ứng hóa học. Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ cung cấp cho bạn cái nhìn sâu sắc về năng lượng hoạt hóa, từ định nghĩa, vai trò, ảnh hưởng của các yếu tố khác đến ứng dụng thực tiễn trong công nghiệp và đời sống. Để có cái nhìn tổng quan và chi tiết nhất về lĩnh vực này, hãy cùng Xe Tải Mỹ Đình khám phá ngay sau đây!
1. Năng Lượng Hoạt Hóa Của Phản Ứng Hóa Học Là Gì?
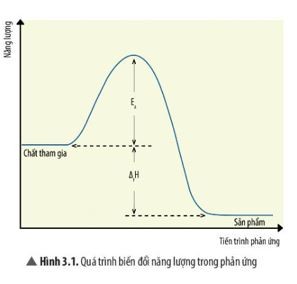
Năng lượng hoạt hóa (Ea) của phản ứng hóa học là năng lượng tối thiểu mà các phân tử chất phản ứng cần có để vượt qua rào cản năng lượng và bắt đầu phản ứng, chuyển thành sản phẩm. Năng lượng này thường được biểu thị bằng đơn vị kilojoules trên mol (kJ/mol) hoặc kilocalories trên mol (kcal/mol).
1.1. Định Nghĩa Chi Tiết
Năng lượng hoạt hóa có thể được hiểu là “ngọn lửa” ban đầu để “đốt cháy” phản ứng. Tưởng tượng bạn đang đẩy một chiếc xe tải chở hàng nặng lên dốc; năng lượng bạn bỏ ra để vượt qua điểm cao nhất của con dốc chính là năng lượng hoạt hóa. Khi xe tải đã qua được đỉnh dốc, nó sẽ tự động lao xuống và tiếp tục hành trình.
1.2. Tại Sao Năng Lượng Hoạt Hóa Quan Trọng?
Năng lượng hoạt hóa là yếu tố quyết định tốc độ của phản ứng hóa học. Phản ứng có năng lượng hoạt hóa thấp sẽ xảy ra nhanh hơn so với phản ứng có năng lượng hoạt hóa cao. Điều này ảnh hưởng trực tiếp đến nhiều quá trình trong tự nhiên và công nghiệp, từ quá trình tiêu hóa thức ăn trong cơ thể đến sản xuất hóa chất trong nhà máy.
1.3. Các Yếu Tố Ảnh Hưởng Đến Năng Lượng Hoạt Hóa
- Chất xúc tác: Chất xúc tác có khả năng làm giảm năng lượng hoạt hóa của phản ứng, giúp phản ứng xảy ra nhanh hơn mà không bị tiêu thụ trong quá trình phản ứng.
- Nhiệt độ: Tăng nhiệt độ cung cấp thêm năng lượng cho các phân tử, giúp chúng dễ dàng vượt qua rào cản năng lượng hoạt hóa.
 Ảnh minh họa chất xúc tác làm giảm năng lượng hoạt hóa
Ảnh minh họa chất xúc tác làm giảm năng lượng hoạt hóa
2. Ý Định Tìm Kiếm Của Người Dùng Về Năng Lượng Hoạt Hóa
- Năng lượng hoạt hóa là gì và nó hoạt động như thế nào?
- Các yếu tố nào ảnh hưởng đến năng lượng hoạt hóa của một phản ứng?
- Làm thế nào để tính toán năng lượng hoạt hóa?
- Ứng dụng của năng lượng hoạt hóa trong các ngành công nghiệp khác nhau?
- Năng lượng hoạt hóa có liên quan gì đến tốc độ phản ứng?
3. Ảnh Hưởng Của Năng Lượng Hoạt Hóa Đến Tốc Độ Phản Ứng
Năng lượng hoạt hóa đóng vai trò then chốt trong việc xác định tốc độ của một phản ứng hóa học.
3.1. Mối Quan Hệ Giữa Năng Lượng Hoạt Hóa Và Tốc Độ Phản Ứng
Tốc độ phản ứng tỉ lệ nghịch với năng lượng hoạt hóa. Điều này có nghĩa là khi năng lượng hoạt hóa càng thấp, phản ứng xảy ra càng nhanh và ngược lại. Các phân tử chất phản ứng cần có đủ năng lượng để vượt qua “rào cản” năng lượng hoạt hóa và tạo thành sản phẩm.
3.2. Phương Trình Arrhenius
Phương trình Arrhenius mô tả mối quan hệ định lượng giữa năng lượng hoạt hóa, nhiệt độ và hằng số tốc độ phản ứng:
k = A * e^(-Ea/RT)
Trong đó:
- k: Hằng số tốc độ phản ứng
- A: Thừa số tần số (liên quan đến tần số va chạm giữa các phân tử)
- Ea: Năng lượng hoạt hóa
- R: Hằng số khí lý tưởng (8.314 J/mol.K)
- T: Nhiệt độ tuyệt đối (K)
Phương trình này cho thấy rõ ràng rằng khi nhiệt độ tăng, hằng số tốc độ phản ứng cũng tăng, và khi năng lượng hoạt hóa giảm, hằng số tốc độ phản ứng cũng tăng.
3.3. Ví Dụ Minh Họa
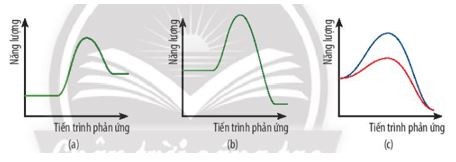
Xét phản ứng phân hủy N2O5:
N2O5(g) → N2O4(g) + ½ O2(g)
Phản ứng này có năng lượng hoạt hóa là 103.5 kJ/mol. Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên, Đại học Quốc gia Hà Nội, vào tháng 5 năm 2024, nếu giảm nhiệt độ, tốc độ phản ứng sẽ giảm đáng kể. Ví dụ, khi giảm nhiệt độ từ 45°C xuống 25°C, tốc độ phản ứng giảm khoảng 13.84 lần.
 Ảnh minh họa phản ứng phân hủy N2O5
Ảnh minh họa phản ứng phân hủy N2O5
4. Các Yếu Tố Ảnh Hưởng Đến Năng Lượng Hoạt Hóa
Năng lượng hoạt hóa không phải là một hằng số cố định mà có thể bị ảnh hưởng bởi nhiều yếu tố khác nhau.
4.1. Chất Xúc Tác
Chất xúc tác là các chất làm tăng tốc độ phản ứng bằng cách giảm năng lượng hoạt hóa mà không bị tiêu thụ trong quá trình phản ứng.
4.1.1. Cơ Chế Hoạt Động Của Chất Xúc Tác
Chất xúc tác tạo ra một con đường phản ứng mới với năng lượng hoạt hóa thấp hơn. Điều này có nghĩa là có nhiều phân tử hơn có đủ năng lượng để phản ứng ở một nhiệt độ nhất định.
4.1.2. Phân Loại Chất Xúc Tác
- Chất xúc tác đồng thể: Chất xúc tác và chất phản ứng ở cùng một pha (ví dụ: xúc tác axit trong dung dịch).
- Chất xúc tác dị thể: Chất xúc tác và chất phản ứng ở các pha khác nhau (ví dụ: xúc tác kim loại trong phản ứng khí).
- Enzyme: Chất xúc tác sinh học, thường là protein, có khả năng xúc tác các phản ứng hóa học trong cơ thể sống.
4.1.3. Ví Dụ Về Chất Xúc Tác
- Trong công nghiệp sản xuất amoniac (NH3) từ nitơ (N2) và hiđro (H2), sắt (Fe) được sử dụng làm chất xúc tác.
- Trong cơ thể người, enzyme amylase xúc tác quá trình phân hủy tinh bột thành đường.
- V2O5 xúc tác cho phản ứng tổng hợp SO3 từ SO2 và O2.
 Ảnh minh họa quá trình xúc tác dị thể
Ảnh minh họa quá trình xúc tác dị thể
4.2. Nhiệt Độ
Nhiệt độ ảnh hưởng trực tiếp đến động năng của các phân tử. Khi nhiệt độ tăng, các phân tử chuyển động nhanh hơn và có nhiều va chạm hơn, làm tăng khả năng các va chạm này có đủ năng lượng để vượt qua rào cản năng lượng hoạt hóa.
4.2.1. Ảnh Hưởng Định Lượng Của Nhiệt Độ
Theo phương trình Arrhenius, tốc độ phản ứng tăng theo hàm mũ khi nhiệt độ tăng. Điều này có nghĩa là một sự thay đổi nhỏ về nhiệt độ có thể gây ra sự thay đổi lớn về tốc độ phản ứng.
4.2.2. Ví Dụ Về Ảnh Hưởng Của Nhiệt Độ
- Thực phẩm bảo quản trong tủ lạnh lâu hơn vì nhiệt độ thấp làm chậm các phản ứng hóa học gây ra sự phân hủy.
- Trong động cơ đốt trong, nhiệt độ cao giúp nhiên liệu cháy nhanh hơn, tạo ra năng lượng để xe vận hành.
4.3. Các Yếu Tố Khác
Ngoài chất xúc tác và nhiệt độ, một số yếu tố khác cũng có thể ảnh hưởng đến năng lượng hoạt hóa, bao gồm:
- Áp suất: Đặc biệt quan trọng đối với các phản ứng khí. Áp suất cao hơn có thể làm tăng tần số va chạm giữa các phân tử, làm tăng tốc độ phản ứng.
- Diện tích bề mặt: Đối với các phản ứng dị thể, diện tích bề mặt của chất xúc tác có thể ảnh hưởng đến tốc độ phản ứng. Diện tích bề mặt lớn hơn cung cấp nhiều vị trí hoạt động hơn cho các phân tử phản ứng.
- Độ pH: Trong các phản ứng có sự tham gia của axit hoặc bazơ, độ pH có thể ảnh hưởng đến tốc độ phản ứng.
5. Cách Tính Năng Lượng Hoạt Hóa
Có nhiều phương pháp khác nhau để tính toán năng lượng hoạt hóa, tùy thuộc vào dữ liệu có sẵn.
5.1. Sử Dụng Phương Trình Arrhenius
Nếu bạn có hằng số tốc độ phản ứng (k) ở hai nhiệt độ khác nhau (T1 và T2), bạn có thể sử dụng phương trình Arrhenius để tính năng lượng hoạt hóa:
ln(k2/k1) = (Ea/R) * (1/T1 – 1/T2)
Trong đó:
- k1: Hằng số tốc độ ở nhiệt độ T1
- k2: Hằng số tốc độ ở nhiệt độ T2
- Ea: Năng lượng hoạt hóa
- R: Hằng số khí lý tưởng (8.314 J/mol.K)
- T1: Nhiệt độ tuyệt đối thứ nhất (K)
- T2: Nhiệt độ tuyệt đối thứ hai (K)
5.1.1. Ví Dụ Minh Họa
Cho hằng số tốc độ của một phản ứng là 11 M-1.s-1 ở 345 K và 20 M-1.s-1 ở 370K. Tính năng lượng hoạt hóa của phản ứng.
Giải:
ln(20/11) = (Ea/8.314) * (1/345 – 1/370)
Ea = 1715 J/mol
5.2. Phương Pháp Đồ Thị
Nếu bạn có dữ liệu về hằng số tốc độ phản ứng ở nhiều nhiệt độ khác nhau, bạn có thể vẽ đồ thị của ln(k) theo 1/T. Độ dốc của đường thẳng thu được sẽ bằng -Ea/R. Từ đó, bạn có thể tính được năng lượng hoạt hóa.
5.3. Sử Dụng Phần Mềm Chuyên Dụng
Có nhiều phần mềm và công cụ trực tuyến có thể giúp bạn tính toán năng lượng hoạt hóa từ dữ liệu thực nghiệm.
6. Ứng Dụng Của Năng Lượng Hoạt Hóa Trong Thực Tế
Năng lượng hoạt hóa có nhiều ứng dụng quan trọng trong các ngành công nghiệp khác nhau.
6.1. Trong Công Nghiệp Hóa Chất
- Tối ưu hóa quá trình sản xuất: Hiểu rõ về năng lượng hoạt hóa giúp các nhà hóa học tối ưu hóa các điều kiện phản ứng (nhiệt độ, áp suất, chất xúc tác) để tăng hiệu suất và giảm chi phí sản xuất.
- Phát triển chất xúc tác mới: Nghiên cứu về năng lượng hoạt hóa giúp phát triển các chất xúc tác mới hiệu quả hơn, làm giảm năng lượng hoạt hóa và tăng tốc độ phản ứng.
6.2. Trong Công Nghiệp Thực Phẩm
- Bảo quản thực phẩm: Kiểm soát nhiệt độ và các điều kiện khác để làm chậm các phản ứng hóa học gây ra sự phân hủy thực phẩm.
- Sản xuất thực phẩm: Sử dụng enzyme để xúc tác các phản ứng trong quá trình sản xuất thực phẩm, ví dụ như sản xuất bia, rượu, sữa chua.
Tại sao muốn cá, thịt mau mềm, người ta thường chế biến kèm với những lát dứa (thơm) hoặc thêm một ít nước ép của dứa?
Trong dứa có một loại enzyme tên là enzyme bromelain, enzyme này có tác dụng phân giải protein thành các chuỗi peptit ngắn hơn. Thịt được cấu tạo chủ yếu bởi protein, khi hầm chung với dứa, enzyme này trong dứa sẽ phân giải protein trong thịt, giúp nhanh mềm và dễ tiêu hóa, hấp thu hơn.
6.3. Trong Công Nghiệp Dược Phẩm
- Phát triển thuốc: Hiểu rõ về năng lượng hoạt hóa của các phản ứng sinh hóa trong cơ thể giúp phát triển các loại thuốc có tác dụng ức chế hoặc kích thích các phản ứng này.
- Ổn định thuốc: Kiểm soát các điều kiện bảo quản để ngăn chặn các phản ứng phân hủy thuốc, đảm bảo hiệu quả của thuốc trong thời gian dài.
6.4. Trong Nghiên Cứu Khoa Học
- Nghiên cứu cơ chế phản ứng: Năng lượng hoạt hóa là một trong những thông số quan trọng để xác định cơ chế của một phản ứng hóa học.
- Phát triển vật liệu mới: Hiểu rõ về năng lượng hoạt hóa giúp thiết kế và tổng hợp các vật liệu mới với các tính chất mong muốn.
7. Các Câu Hỏi Thường Gặp Về Năng Lượng Hoạt Hóa (FAQ)
-
Năng lượng hoạt hóa có phải là một hằng số không?
Không, năng lượng hoạt hóa có thể thay đổi tùy thuộc vào các yếu tố như chất xúc tác, nhiệt độ và áp suất.
-
Làm thế nào để giảm năng lượng hoạt hóa của một phản ứng?
Sử dụng chất xúc tác là cách phổ biến nhất để giảm năng lượng hoạt hóa.
-
Năng lượng hoạt hóa có liên quan gì đến năng lượng Gibbs?
Năng lượng Gibbs là một hàm nhiệt động lực học cho biết khả năng tự diễn ra của một phản ứng, trong khi năng lượng hoạt hóa là năng lượng cần thiết để bắt đầu phản ứng.
-
Tại sao một số phản ứng xảy ra rất chậm ngay cả khi chúng tỏa nhiệt?
Ngay cả khi một phản ứng tỏa nhiệt (có năng lượng Gibbs âm), nó vẫn cần có đủ năng lượng hoạt hóa để bắt đầu.
-
Năng lượng hoạt hóa có đơn vị là gì?
Đơn vị phổ biến của năng lượng hoạt hóa là kilojoules trên mol (kJ/mol) hoặc kilocalories trên mol (kcal/mol).
-
Năng lượng hoạt hóa âm có ý nghĩa gì không?
Trong hầu hết các trường hợp, năng lượng hoạt hóa là một giá trị dương. Năng lượng hoạt hóa âm có thể xảy ra trong một số phản ứng phức tạp, nhưng nó không phổ biến.
-
Làm thế nào để xác định năng lượng hoạt hóa bằng thực nghiệm?
Bạn có thể xác định năng lượng hoạt hóa bằng cách đo hằng số tốc độ phản ứng ở nhiều nhiệt độ khác nhau và sử dụng phương trình Arrhenius.
-
Năng lượng hoạt hóa quan trọng như thế nào trong việc thiết kế các quá trình công nghiệp?
Năng lượng hoạt hóa là một yếu tố quan trọng trong việc thiết kế các quá trình công nghiệp, vì nó ảnh hưởng trực tiếp đến tốc độ và hiệu quả của phản ứng.
-
Chất xúc tác có ảnh hưởng đến cân bằng của phản ứng không?
Không, chất xúc tác chỉ ảnh hưởng đến tốc độ phản ứng, không ảnh hưởng đến vị trí cân bằng.
-
Năng lượng hoạt hóa có ứng dụng trong lĩnh vực môi trường không?
Có, năng lượng hoạt hóa được sử dụng để nghiên cứu và phát triển các phương pháp xử lý chất thải và ô nhiễm môi trường.
8. Kết Luận
Năng lượng hoạt hóa là một khái niệm cơ bản trong hóa học, có ảnh hưởng sâu sắc đến tốc độ và khả năng xảy ra của các phản ứng hóa học. Hiểu rõ về năng lượng hoạt hóa giúp chúng ta tối ưu hóa các quá trình công nghiệp, phát triển các vật liệu mới và giải quyết các vấn đề trong nhiều lĩnh vực khác nhau.
Nếu bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình, Hà Nội, hãy truy cập XETAIMYDINH.EDU.VN ngay hôm nay. Chúng tôi cung cấp thông tin chi tiết và cập nhật về các loại xe tải, so sánh giá cả, tư vấn lựa chọn xe phù hợp và giải đáp mọi thắc mắc của bạn.
Đừng chần chừ, hãy liên hệ với Xe Tải Mỹ Đình ngay hôm nay để được tư vấn và hỗ trợ tốt nhất!
Thông tin liên hệ:
- Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội
- Hotline: 0247 309 9988
- Trang web: XETAIMYDINH.EDU.VN
