Nhóm B Trong Bảng Tuần Hoàn là một chủ đề quan trọng trong hóa học. Bạn muốn tìm hiểu sâu hơn về nhóm B trong bảng tuần hoàn, bao gồm định nghĩa, đặc điểm và ứng dụng thực tế của nó? Hãy cùng Xe Tải Mỹ Đình khám phá chi tiết về nhóm nguyên tố này. Tại XETAIMYDINH.EDU.VN, chúng tôi cung cấp những thông tin chi tiết và đáng tin cậy giúp bạn hiểu rõ hơn về thế giới hóa học. Xe Tải Mỹ Đình cung cấp các thông tin về hóa trị, cấu hình electron, tính chất vật lý và hóa học, cũng như vai trò quan trọng của chúng trong đời sống và công nghiệp.
1. Tổng Quan Về Bảng Tuần Hoàn Các Nguyên Tố Hóa Học
Trước khi đi sâu vào nhóm B, hãy cùng Xe Tải Mỹ Đình điểm qua cấu trúc chung của bảng tuần hoàn để hiểu rõ hơn về vị trí và vai trò của nhóm này.
1.1. Cấu Trúc Bảng Tuần Hoàn
Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo ba nguyên tắc chính:
- Nguyên tắc 1: Các nguyên tố hóa học được sắp xếp theo chiều tăng dần điện tích hạt nhân.
- Nguyên tắc 2: Các nguyên tố mà nguyên tử của nó có cùng số lớp electron được xếp thành một hàng (chu kỳ).
- Nguyên tắc 3: Các nguyên tố mà nguyên tử của nó có cùng số electron hóa trị được xếp thành một cột (nhóm).
Electron hóa trị là những hạt electron có khả năng tham gia hình thành các liên kết hóa học (electron lớp ngoài cùng hoặc phân lớp gần ngoài cùng chưa bão hòa).
1.2. Ô Nguyên Tố
Mỗi nguyên tố hóa học được xếp vào một ô trong bảng, gọi là ô nguyên tố. Số thứ tự của ô nguyên tố bằng chính số hiệu nguyên tử của nguyên tố đó.
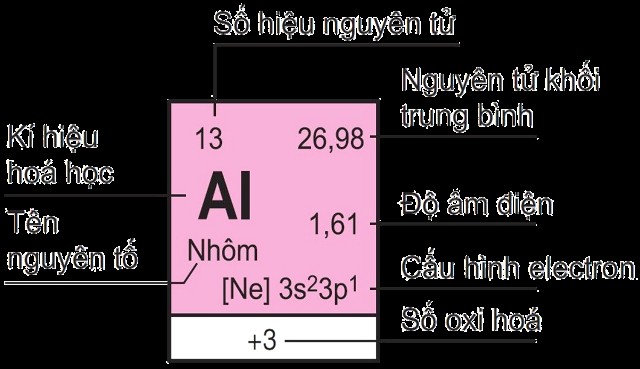 Ô nguyên tố trong bảng tuần hoàn
Ô nguyên tố trong bảng tuần hoàn
1.3. Chu Kỳ
1.3.1. Định Nghĩa
Chu kỳ là dãy các nguyên tố mà nguyên tử của chúng có số lớp electron bằng nhau, được sắp xếp theo chiều điện tích hạt nhân tăng dần từ trái sang phải.
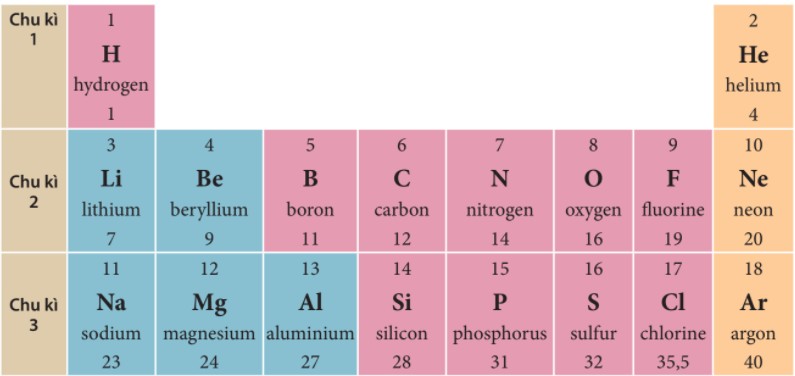 Chu kỳ trong bảng tuần hoàn
Chu kỳ trong bảng tuần hoàn
1.3.2. Các Chu Kỳ
- Chu kỳ 1: Gồm 2 nguyên tố từ H (Z=1) đến He (Z=2).
- Chu kỳ 2: Gồm 8 nguyên tố từ Li (Z=3) đến Ne (Z=10).
- Chu kỳ 3: Gồm 8 nguyên tố từ Na (Z=11) đến Ar (Z=18).
- Chu kỳ 4: Gồm 18 nguyên tố từ K (Z=19) đến Kr (Z=36).
- Chu kỳ 5: Gồm 18 nguyên tố từ Rb (Z=37) đến Xe (Z=54).
- Chu kỳ 6: Gồm 32 nguyên tố từ Cs (Z=55) đến Rn (Z=86).
- Chu kỳ 7: Bắt đầu từ nguyên tố Fr (Z=87) đến nguyên tố có Z=110, đây là một chu kỳ chưa được hoàn thành.
1.3.3. Phân Loại Chu Kỳ
- Chu kỳ nhỏ: Bao gồm chu kỳ 1, 2 và 3.
- Chu kỳ lớn: Bao gồm chu kỳ 4, 5, 6 và 7.
1.3.4. Nhận Xét Chung
Các nguyên tố thuộc cùng một chu kỳ có số lớp electron bằng nhau và bằng chính số thứ tự của chu kỳ. Mở đầu mỗi chu kỳ là kim loại kiềm, đến gần cuối chu kỳ là halogen (trừ chu kỳ 1) và cuối chu kỳ là khí hiếm. Hai hàng cuối của bảng tuần hoàn là hai họ nguyên tố có cấu hình electron đặc biệt là Lantan và Actini.
- Họ Lantan: Thuộc chu kỳ 6, gồm 14 nguyên tố đứng sau La (Z=57).
- Họ Actini: Thuộc chu kỳ 7, gồm 14 nguyên tố sau Ac (Z=89).
1.4. Nhóm Nguyên Tố
1.4.1. Định Nghĩa
Nhóm nguyên tố là tập hợp các nguyên tố hóa học có đặc điểm nguyên tử của nó có cấu hình electron tương tự nhau, vì vậy chúng có tính chất hóa học gần giống nhau và được sắp xếp chung 1 cột.
1.4.2. Phân Loại
Bảng tuần hoàn chia thành 8 nhóm A và 8 nhóm B được đánh số lần lượt từ IA đến VIIIA và từ IB đến VIIIB. Mỗi nhóm là 1 cột, chỉ riêng nhóm VIIIB gồm 3 cột. Nguyên tử các nguyên tố thuộc cùng một nhóm có số electron hóa trị bằng nhau và bằng số thứ tự của nhóm (ngoại trừ hai cột cuối của nhóm VIIIB).
1.5. Khối Nguyên Tố
Khối các nguyên tố s gồm các nguyên tố trong nhóm IA và IIA. Khối các nguyên tố p gồm các nguyên tố trong nhóm IIIA đến nhóm VIIIA (trừ He). Nhóm A chỉ gồm các nguyên tố s và p. Khối các nguyên tố d bao gồm các nguyên tố hóa học thuộc nhóm B. Khối các nguyên tố f gồm các nguyên tố xếp ở hai hàng cuối của bảng tuần hoàn. Nhóm B bao gồm các nguyên tố d và f.
2. Nhóm B Trong Bảng Tuần Hoàn
2.1. Vị Trí và Đặc Điểm Chung
Nhóm B bao gồm các nguyên tố d và f, nằm ở khu vực trung tâm của bảng tuần hoàn. Các nguyên tố này còn được gọi là các kim loại chuyển tiếp.
-
Vị trí: Từ nhóm IIIB đến IIB (từ cột 3 đến cột 12) trong bảng tuần hoàn.
-
Đặc điểm chung:
- Đa số là kim loại có ánh kim, dẫn điện và nhiệt tốt.
- Có nhiều trạng thái oxy hóa khác nhau.
- Tạo thành các hợp chất có màu sắc đa dạng.
- Nhiều nguyên tố trong nhóm B có vai trò quan trọng trong xúc tác hóa học.
2.2. Cấu Hình Electron
Cấu hình electron tổng quát của các nguyên tố nhóm B là (n-1)d^(1-10)ns^(1-2), trong đó n là số lớp electron ngoài cùng. Điều này giải thích tại sao các nguyên tố này có nhiều trạng thái oxy hóa khác nhau, do electron có thể được lấy đi từ cả lớp d và lớp s.
2.3. Tính Chất Vật Lý
- Tính kim loại: Đa số các nguyên tố nhóm B là kim loại, có độ cứng, độ bền cao và khả năng dẫn điện, dẫn nhiệt tốt. Ví dụ, sắt (Fe), đồng (Cu) và kẽm (Zn) là những kim loại quan trọng trong công nghiệp và đời sống. Theo Tổng cục Thống kê, sản lượng thép thô của Việt Nam năm 2023 đạt 23 triệu tấn, cho thấy vai trò quan trọng của sắt trong nền kinh tế.
- Nhiệt độ nóng chảy và nhiệt độ sôi: Các nguyên tố nhóm B thường có nhiệt độ nóng chảy và nhiệt độ sôi cao do liên kết kim loại mạnh. Ví dụ, vonfram (W) có nhiệt độ nóng chảy cao nhất trong các kim loại (3422 °C), được sử dụng trong các ứng dụng chịu nhiệt cao như sợi đốt bóng đèn.
- Màu sắc: Nhiều hợp chất của các nguyên tố nhóm B có màu sắc đặc trưng do sự chuyển electron giữa các mức năng lượng d. Ví dụ, muối đồng (CuSO4) có màu xanh lam, muối niken (NiCl2) có màu xanh lục.
2.4. Tính Chất Hóa Học
- Tính khử: Các kim loại chuyển tiếp có tính khử, có thể tác dụng với oxy, halogen và axit. Ví dụ, sắt tác dụng với oxy tạo thành oxit sắt (gỉ sắt).
- Nhiều trạng thái oxy hóa: Các nguyên tố nhóm B có khả năng tạo thành nhiều trạng thái oxy hóa khác nhau, do năng lượng giữa các electron lớp d và s gần nhau. Ví dụ, mangan (Mn) có các trạng thái oxy hóa từ +2 đến +7. Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên Hà Nội vào tháng 5 năm 2024, khả năng thay đổi trạng thái oxy hóa của mangan làm cho nó trở thành chất xúc tác quan trọng trong nhiều phản ứng hóa học.
- Khả năng tạo phức chất: Các ion kim loại chuyển tiếp có khả năng tạo phức chất với các phối tử như nước, amoniac, halogen và các ion âm khác. Phức chất có cấu trúc và tính chất đa dạng, được ứng dụng trong nhiều lĩnh vực như hóa phân tích, y học và công nghiệp.
3. Các Nhóm Nhỏ Trong Nhóm B
3.1. Nhóm Scandi (Nhóm 3)
Nhóm Scandi bao gồm các nguyên tố scandi (Sc), yttri (Y), luteti (Lu) và lawrenci (Lr). Chúng là các kim loại hoạt động, có cấu hình electron lớp ngoài cùng là ns²(n-1)d¹. Scandi được sử dụng trong hợp kim nhôm để tăng độ bền và giảm trọng lượng. Yttri được sử dụng trong sản xuất các vật liệu siêu dẫn và đèn huỳnh quang.
3.2. Nhóm Titan (Nhóm 4)
Nhóm Titan bao gồm các nguyên tố titan (Ti), zirconi (Zr), hafini (Hf) và rutherfordi (Rf). Titan là một kim loại nhẹ, bền và chống ăn mòn tốt, được sử dụng rộng rãi trong ngành hàng không, y tế và công nghiệp hóa chất. Zirconi được sử dụng trong lò phản ứng hạt nhân và sản xuất gốm sứ chịu nhiệt.
3.3. Nhóm Vanadi (Nhóm 5)
Nhóm Vanadi bao gồm các nguyên tố vanadi (V), niobi (Nb), tantali (Ta) và dubni (Db). Vanadi được sử dụng làm chất phụ gia trong thép để tăng độ cứng và độ bền. Niobi và tantali được sử dụng trong sản xuất các thiết bị điện tử và hợp kim chịu nhiệt.
3.4. Nhóm Crom (Nhóm 6)
Nhóm Crom bao gồm các nguyên tố crom (Cr), molipden (Mo), vonfram (W) và seaborgi (Sg). Crom là một kim loại cứng, chống ăn mòn tốt, được sử dụng để mạ bảo vệ và sản xuất thép không gỉ. Molipden và vonfram được sử dụng trong sản xuất thép công cụ và các hợp kim chịu nhiệt cao.
3.5. Nhóm Mangan (Nhóm 7)
Nhóm Mangan bao gồm các nguyên tố mangan (Mn), techneti (Tc), reni (Re) và bohri (Bh). Mangan là một kim loại cứng, giòn, được sử dụng làm chất khử oxy và chất phụ gia trong thép. Techneti là một nguyên tố phóng xạ, được sử dụng trong y học hạt nhân. Reni được sử dụng trong các chất xúc tác và hợp kim chịu nhiệt cao.
3.6. Nhóm Sắt (Nhóm 8)
Nhóm Sắt bao gồm các nguyên tố sắt (Fe), ruteni (Ru), osmi (Os) và hassi (Hs). Sắt là một kim loại quan trọng, được sử dụng rộng rãi trong xây dựng, giao thông và sản xuất máy móc. Ruteni và osmi là các kim loại quý hiếm, được sử dụng trong các hợp kim cứng và chất xúc tác.
3.7. Nhóm Coban (Nhóm 9)
Nhóm Coban bao gồm các nguyên tố coban (Co), rhodi (Rh), iridi (Ir) và meitneri (Mt). Coban là một kim loại cứng, được sử dụng trong sản xuất nam châm, hợp kim chịu nhiệt và chất xúc tác. Rhodi và iridi là các kim loại quý hiếm, được sử dụng trong các chất xúc tác và thiết bị điện tử.
3.8. Nhóm Niken (Nhóm 10)
Nhóm Niken bao gồm các nguyên tố niken (Ni), paladi (Pd), platina (Pt) và darmstadti (Ds). Niken là một kim loại dẻo, dễ uốn, được sử dụng để mạ bảo vệ, sản xuất pin và hợp kim chịu nhiệt. Paladi và platina là các kim loại quý hiếm, được sử dụng trong các chất xúc tác, thiết bị điện tử và trang sức.
3.9. Nhóm Đồng (Nhóm 11)
Nhóm Đồng bao gồm các nguyên tố đồng (Cu), bạc (Ag), vàng (Au) và roentgeni (Rg). Đồng là một kim loại dẫn điện tốt, được sử dụng rộng rãi trong hệ thống điện, ống dẫn nước và sản xuất hợp kim. Bạc và vàng là các kim loại quý hiếm, được sử dụng trong trang sức, tiền tệ và thiết bị điện tử.
3.10. Nhóm Kẽm (Nhóm 12)
Nhóm Kẽm bao gồm các nguyên tố kẽm (Zn), cadmi (Cd), thủy ngân (Hg) và copernici (Cn). Kẽm là một kim loại được sử dụng để mạ bảo vệ, sản xuất pin và hợp kim. Cadmi là một kim loại độc hại, được sử dụng trong pin và mạ điện. Thủy ngân là một kim loại lỏng ở nhiệt độ phòng, được sử dụng trong nhiệt kế, áp kế và sản xuất hóa chất.
4. Ứng Dụng Quan Trọng Của Các Nguyên Tố Nhóm B
4.1. Trong Công Nghiệp
- Sản xuất thép: Sắt (Fe), crom (Cr), mangan (Mn), niken (Ni) và vanadi (V) là các nguyên tố quan trọng trong sản xuất thép, giúp tăng độ cứng, độ bền và khả năng chống ăn mòn của thép.
- Xúc tác hóa học: Nhiều nguyên tố nhóm B như platina (Pt), paladi (Pd), niken (Ni) và coban (Co) được sử dụng làm chất xúc tác trong các quá trình hóa học quan trọng như sản xuất phân bón, xăng dầu và hóa chất.
- Điện tử: Đồng (Cu), bạc (Ag) và vàng (Au) là các kim loại dẫn điện tốt, được sử dụng rộng rãi trong các thiết bị điện tử, dây điện và bảng mạch in.
- Hàng không vũ trụ: Titan (Ti) và các hợp kim của nó được sử dụng trong ngành hàng không vũ trụ do có độ bền cao, trọng lượng nhẹ và khả năng chịu nhiệt tốt.
4.2. Trong Y Học
- Chẩn đoán hình ảnh: Techneti (Tc) được sử dụng trong y học hạt nhân để chẩn đoán các bệnh về tim mạch, ung thư và các bệnh lý khác.
- Dụng cụ y tế: Titan (Ti) được sử dụng trong sản xuất các dụng cụ y tế như khớp nhân tạo, implant nha khoa do có tính tương thích sinh học cao và không gây dị ứng.
- Thuốc: Platina (Pt) được sử dụng trong các loại thuốc điều trị ung thư như cisplatin.
4.3. Trong Đời Sống
- Trang sức: Vàng (Au), bạc (Ag) và platina (Pt) là các kim loại quý hiếm được sử dụng trong trang sức do có vẻ đẹp, độ bền và giá trị cao.
- Tiền tệ: Vàng (Au) và bạc (Ag) được sử dụng để đúc tiền xu và làm vật dự trữ giá trị.
- Đồ gia dụng: Thép không gỉ (chứa crom và niken) được sử dụng trong sản xuất các đồ gia dụng như nồi, chảo, dao và kéo do có khả năng chống ăn mòn và dễ vệ sinh.
5. So Sánh Nhóm A và Nhóm B
| Đặc điểm | Nhóm A (Nguyên tố s và p) | Nhóm B (Nguyên tố d và f) |
|---|---|---|
| Vị trí | Hai bên bảng tuần hoàn | Trung tâm bảng tuần hoàn |
| Cấu hình e | ns^a np^b | (n-1)d^(1-10)ns^(1-2) |
| Tính chất | Đa dạng, kim loại, phi kim, khí hiếm | Đa số là kim loại, có tính khử |
| Trạng thái oxh | Ít trạng thái oxy hóa | Nhiều trạng thái oxy hóa |
| Ứng dụng | Đa dạng trong nhiều lĩnh vực | Công nghiệp, xúc tác, y học |
6. Những Câu Hỏi Thường Gặp Về Nhóm B
6.1. Nhóm B gồm những nguyên tố nào?
Nhóm B bao gồm các nguyên tố từ nhóm 3 (IIIB) đến nhóm 12 (IIB) trong bảng tuần hoàn, bao gồm các kim loại chuyển tiếp như sắt (Fe), đồng (Cu), kẽm (Zn), và các nguyên tố thuộc họ Lanthan và Actini.
6.2. Tại sao các nguyên tố nhóm B có nhiều trạng thái oxy hóa?
Các nguyên tố nhóm B có nhiều trạng thái oxy hóa do cấu hình electron của chúng có electron ở cả lớp d và lớp s, với năng lượng giữa các lớp này gần nhau, cho phép electron dễ dàng được lấy đi hoặc thêm vào.
6.3. Tính chất đặc trưng của các nguyên tố nhóm B là gì?
Tính chất đặc trưng của các nguyên tố nhóm B bao gồm tính kim loại, khả năng tạo thành nhiều trạng thái oxy hóa khác nhau, tạo thành các hợp chất có màu sắc, và khả năng làm chất xúc tác trong nhiều phản ứng hóa học.
6.4. Các nguyên tố nhóm B có vai trò gì trong công nghiệp?
Các nguyên tố nhóm B có vai trò quan trọng trong công nghiệp, đặc biệt trong sản xuất thép, xúc tác hóa học, điện tử, hàng không vũ trụ và nhiều lĩnh vực khác.
6.5. Các nguyên tố nhóm B có độc hại không?
Một số nguyên tố nhóm B như cadmi (Cd) và thủy ngân (Hg) có độc tính cao và gây hại cho sức khỏe con người và môi trường.
6.6. Làm thế nào để phân biệt nhóm A và nhóm B trong bảng tuần hoàn?
Nhóm A bao gồm các nguyên tố s và p nằm ở hai bên bảng tuần hoàn, trong khi nhóm B bao gồm các nguyên tố d và f nằm ở trung tâm bảng tuần hoàn.
6.7. Tại sao các nguyên tố nhóm B thường tạo thành các hợp chất có màu sắc?
Các hợp chất của các nguyên tố nhóm B thường có màu sắc do sự chuyển electron giữa các mức năng lượng d, hấp thụ ánh sáng ở các bước sóng khác nhau và tạo ra màu sắc đặc trưng.
6.8. Ứng dụng của titan (Ti) trong y học là gì?
Titan (Ti) được sử dụng trong y học để sản xuất các dụng cụ y tế như khớp nhân tạo, implant nha khoa do có tính tương thích sinh học cao, không gây dị ứng và khả năng chịu lực tốt.
6.9. Tại sao vàng (Au) được sử dụng trong trang sức và tiền tệ?
Vàng (Au) được sử dụng trong trang sức và tiền tệ do có vẻ đẹp, độ bền, khả năng chống ăn mòn và giá trị cao.
6.10. Vai trò của niken (Ni) trong sản xuất thép không gỉ là gì?
Niken (Ni) được thêm vào thép để tạo thành thép không gỉ, giúp tăng khả năng chống ăn mòn và làm cho thép dễ vệ sinh hơn.
7. Kết Luận
Nhóm B trong bảng tuần hoàn là một nhóm các nguyên tố quan trọng với nhiều ứng dụng trong công nghiệp, y học và đời sống. Việc hiểu rõ về cấu trúc, tính chất và ứng dụng của các nguyên tố này giúp chúng ta nắm vững kiến thức hóa học và ứng dụng nó vào thực tế.
Nếu bạn muốn tìm hiểu thêm về các loại xe tải và các ứng dụng của chúng trong ngành vận tải, hãy truy cập XETAIMYDINH.EDU.VN ngay hôm nay. Chúng tôi cung cấp thông tin chi tiết và cập nhật về các loại xe tải, giúp bạn lựa chọn được chiếc xe phù hợp với nhu cầu của mình.
Bạn đang gặp khó khăn trong việc tìm kiếm thông tin về xe tải hoặc cần tư vấn về các dịch vụ liên quan? Đừng ngần ngại liên hệ với Xe Tải Mỹ Đình qua hotline 0247 309 9988 hoặc truy cập trang web XETAIMYDINH.EDU.VN để được hỗ trợ nhanh chóng và tận tình. Chúng tôi luôn sẵn sàng giải đáp mọi thắc mắc của bạn! Địa chỉ của chúng tôi là Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội. Hãy đến với Xe Tải Mỹ Đình để trải nghiệm dịch vụ chuyên nghiệp và tận tâm nhất!