Tính chất hóa học của oxit quyết định cách chúng tương tác với các chất khác, tạo ra nhiều ứng dụng quan trọng trong công nghiệp và đời sống, và Xe Tải Mỹ Đình sẽ giúp bạn hiểu rõ hơn về điều này. Bài viết này sẽ đi sâu vào tính chất hóa học của oxit, phân loại và các ứng dụng thực tế, giúp bạn nắm vững kiến thức và áp dụng hiệu quả.
1. Oxit Là Gì? Tổng Quan Về Định Nghĩa Và Phân Loại
Oxit là hợp chất hóa học được tạo thành từ sự kết hợp giữa nguyên tố oxi và một nguyên tố khác. Dựa vào tính chất hóa học, oxit được chia thành 4 loại chính: oxit bazơ, oxit axit, oxit lưỡng tính và oxit trung tính.
1.1. Định Nghĩa Oxit
Oxit là hợp chất hóa học, trong đó oxi liên kết với một hoặc nhiều nguyên tố khác. Công thức chung của oxit là $X_mO_n$, trong đó X là nguyên tố khác oxi, m và n là các chỉ số nguyên dương. Theo “Tuyển tập các bài giảng Hóa học” của GS.TS. Trần Quốc Sơn (Nhà xuất bản Giáo dục Việt Nam), oxit chiếm vị trí quan trọng trong hóa học vô cơ, tham gia vào nhiều quá trình phản ứng và có nhiều ứng dụng thực tế.
1.2. Phân Loại Oxit Dựa Trên Tính Chất Hóa Học
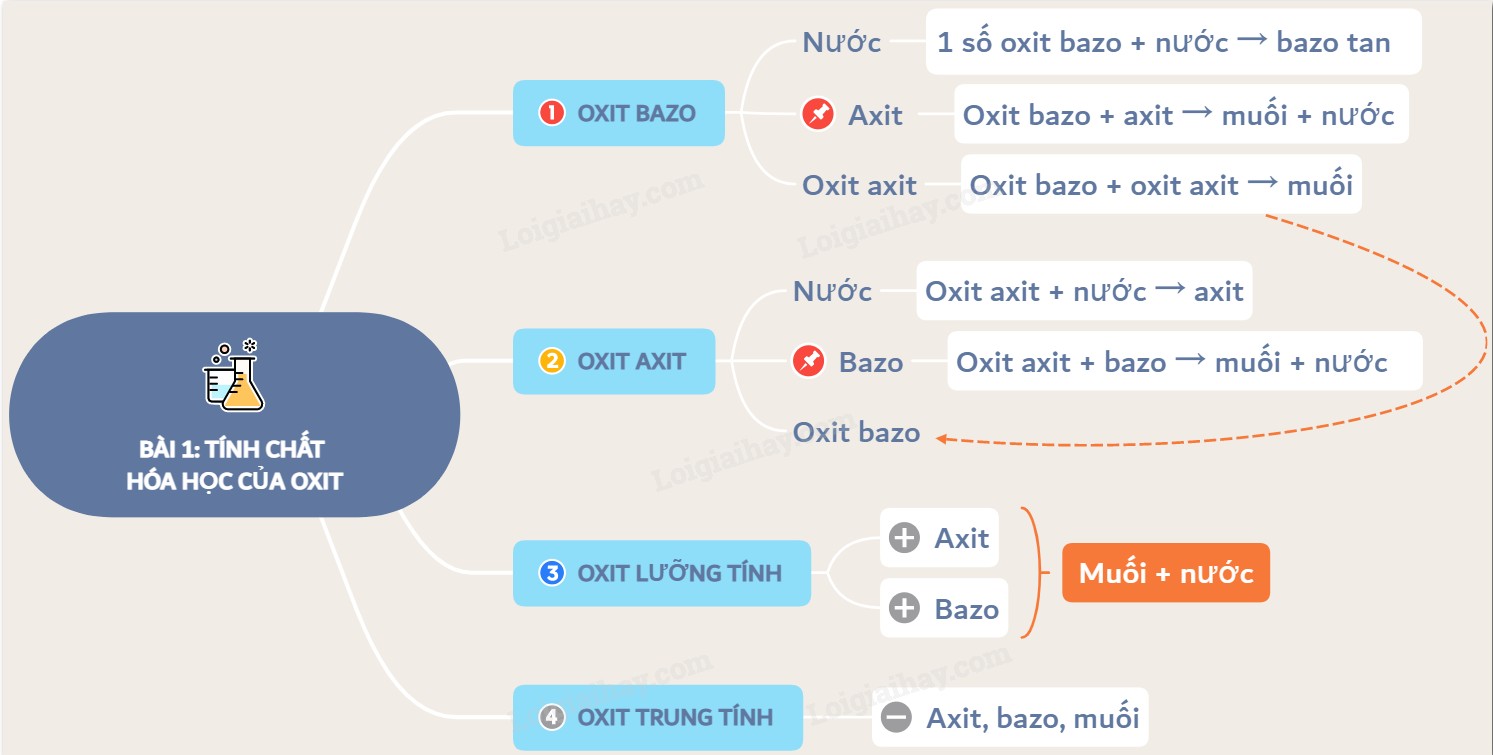
Dựa vào tính chất hóa học, oxit được phân thành 4 loại chính:
- Oxit Bazơ: Thường là oxit của kim loại, tác dụng với axit tạo thành muối và nước.
- Oxit Axit: Thường là oxit của phi kim, tác dụng với bazơ tạo thành muối và nước.
- Oxit Lưỡng Tính: Vừa tác dụng được với axit, vừa tác dụng được với bazơ để tạo thành muối và nước.
- Oxit Trung Tính (Oxit Không Tạo Muối): Không tác dụng với axit, bazơ hay nước.
Bảng phân loại oxit theo tính chất hóa học:
| Loại Oxit | Tính Chất Hóa Học Chính | Ví Dụ |
|---|---|---|
| Oxit Bazơ | Tác dụng với axit tạo muối và nước | Na2O, CaO |
| Oxit Axit | Tác dụng với bazơ tạo muối và nước | SO2, CO2 |
| Oxit Lưỡng Tính | Tác dụng với cả axit và bazơ tạo muối và nước | Al2O3, ZnO |
| Oxit Trung Tính | Không tác dụng với axit, bazơ và nước | CO, NO |
1.3. Ý Nghĩa Của Việc Phân Loại Oxit Trong Hóa Học
Việc phân loại oxit giúp chúng ta dễ dàng dự đoán tính chất và khả năng phản ứng của chúng trong các phản ứng hóa học. Điều này rất quan trọng trong việc nghiên cứu, ứng dụng và điều chế các hợp chất hóa học khác nhau.
2. Tính Chất Hóa Học Của Oxit Bazơ
Oxit bazơ thường là oxit của các kim loại kiềm và kiềm thổ. Chúng có khả năng tác dụng với nước, axit và oxit axit để tạo thành các sản phẩm khác nhau.
2.1. Tác Dụng Với Nước: Tạo Thành Dung Dịch Bazơ (Kiềm)
Một số oxit bazơ, đặc biệt là oxit của kim loại kiềm và kiềm thổ, có khả năng tác dụng với nước tạo thành dung dịch bazơ (kiềm). Phản ứng này thường diễn ra mạnh mẽ và tỏa nhiệt.
Ví dụ:
-
Natri oxit tác dụng với nước:
$Na_2O + H_2O rightarrow 2NaOH$
-
Bari oxit tác dụng với nước:
$BaO + H_2O rightarrow Ba(OH)_2$
Theo “Hóa học Vô cơ” của Hoàng Nhâm (Nhà xuất bản Giáo dục), các oxit bazơ tan trong nước tạo thành dung dịch bazơ mạnh, có khả năng làm đổi màu chất chỉ thị và tác dụng với axit.
2.2. Tác Dụng Với Axit: Tạo Thành Muối Và Nước
Oxit bazơ tác dụng với axit tạo thành muối và nước. Đây là một phản ứng trung hòa, trong đó oxit bazơ đóng vai trò là chất bazơ, axit đóng vai trò là chất axit.
Ví dụ:
-
Bari oxit tác dụng với axit clohydric:
$BaO + 2HCl rightarrow BaCl_2 + H_2O$
-
Sắt(III) oxit tác dụng với axit sulfuric:
$Fe_2O_3 + 3H_2SO_4 rightarrow Fe_2(SO_4)_3 + 3H_2O$
2.3. Tác Dụng Với Oxit Axit: Tạo Thành Muối
Một số oxit bazơ có khả năng tác dụng với oxit axit để tạo thành muối. Phản ứng này thường xảy ra ở nhiệt độ cao.
Ví dụ:
-
Canxi oxit tác dụng với cacbon đioxit:
$CaO + CO_2 rightarrow CaCO_3$
2.4. Bảng Tổng Hợp Tính Chất Hóa Học Của Oxit Bazơ
| Phản Ứng | Phương Trình Tổng Quát | Ví Dụ |
|---|---|---|
| Oxit bazơ + Nước | $Oxit ; bazơ + H_2O rightarrow Bazơ$ | $Na_2O + H_2O rightarrow 2NaOH$ |
| Oxit bazơ + Axit | $Oxit ; bazơ + Axit rightarrow Muối + Nước$ | $MgO + 2HCl rightarrow MgCl_2 + H_2O$ |
| Oxit bazơ + Oxit axit | $Oxit ; bazơ + Oxit ; axit rightarrow Muối$ | $CaO + CO_2 rightarrow CaCO_3$ |
3. Tính Chất Hóa Học Của Oxit Axit
Oxit axit thường là oxit của các phi kim. Chúng có khả năng tác dụng với nước, bazơ và oxit bazơ để tạo thành các sản phẩm khác nhau.
3.1. Tác Dụng Với Nước: Tạo Thành Dung Dịch Axit
Nhiều oxit axit tác dụng với nước tạo thành dung dịch axit. Phản ứng này thường diễn ra khi oxit axit tan trong nước.
Ví dụ:
-
Lưu huỳnh trioxit tác dụng với nước:
$SO_3 + H_2O rightarrow H_2SO_4$
-
Điphotpho pentaoxit tác dụng với nước:
$P_2O_5 + 3H_2O rightarrow 2H_3PO_4$
Theo “250 Bài tập Hóa học Vô cơ Chọn Lọc” của Cao Thị Thặng (Nhà xuất bản Đại học Sư phạm), các oxit axit khi tan trong nước tạo thành các axit tương ứng, có khả năng làm đổi màu chất chỉ thị và tác dụng với bazơ.
3.2. Tác Dụng Với Dung Dịch Bazơ: Tạo Thành Muối Và Nước
Oxit axit tác dụng với dung dịch bazơ tạo thành muối và nước. Đây là một phản ứng trung hòa, trong đó oxit axit đóng vai trò là chất axit, bazơ đóng vai trò là chất bazơ.
Ví dụ:
-
Cacbon đioxit tác dụng với canxi hidroxit:
$CO_2 + Ca(OH)_2 rightarrow CaCO_3 + H_2O$
3.3. Tác Dụng Với Oxit Bazơ: Tạo Thành Muối
Oxit axit tác dụng với oxit bazơ tạo thành muối. Phản ứng này thường xảy ra ở nhiệt độ cao.
Ví dụ:
-
Cacbon đioxit tác dụng với bari oxit:
$CO_2 + BaO rightarrow BaCO_3$
3.4. Bảng Tổng Hợp Tính Chất Hóa Học Của Oxit Axit
| Phản Ứng | Phương Trình Tổng Quát | Ví Dụ |
|---|---|---|
| Oxit axit + Nước | $Oxit ; axit + H_2O rightarrow Axit$ | $SO_2 + H_2O rightarrow H_2SO_3$ |
| Oxit axit + Dung dịch bazơ | $Oxit ; axit + Bazơ rightarrow Muối + Nước$ | $CO_2 + 2NaOH rightarrow Na_2CO_3 + H_2O$ |
| Oxit axit + Oxit bazơ | $Oxit ; axit + Oxit ; bazơ rightarrow Muối$ | $SO_3 + K_2O rightarrow K_2SO_4$ |
4. Tính Chất Hóa Học Của Oxit Lưỡng Tính
Oxit lưỡng tính là những oxit vừa có khả năng tác dụng với axit, vừa có khả năng tác dụng với bazơ để tạo thành muối và nước.
4.1. Khái Niệm Về Oxit Lưỡng Tính
Oxit lưỡng tính là oxit có thể hiện tính chất của cả oxit axit và oxit bazơ, tùy thuộc vào chất phản ứng. Các oxit lưỡng tính thường là oxit của các kim loại có số oxi hóa trung bình. Theo “Cẩm nang Hóa học” của David R. Lide, oxit lưỡng tính có vai trò quan trọng trong nhiều quá trình hóa học và công nghiệp.
4.2. Tác Dụng Với Axit: Tạo Thành Muối Và Nước
Oxit lưỡng tính tác dụng với axit tạo thành muối và nước, tương tự như oxit bazơ.
Ví dụ:
-
Nhôm oxit tác dụng với axit clohydric:
$Al_2O_3 + 6HCl rightarrow 2AlCl_3 + 3H_2O$
-
Kẽm oxit tác dụng với axit sulfuric:
$ZnO + H_2SO_4 rightarrow ZnSO_4 + H_2O$
4.3. Tác Dụng Với Dung Dịch Bazơ: Tạo Thành Muối Và Nước
Oxit lưỡng tính tác dụng với dung dịch bazơ tạo thành muối và nước. Trong phản ứng này, oxit lưỡng tính thể hiện tính chất của một oxit axit.
Ví dụ:
-
Nhôm oxit tác dụng với natri hidroxit:
$Al_2O_3 + 2NaOH rightarrow 2NaAlO_2 + H_2O$ (natri aluminat)
-
Kẽm oxit tác dụng với natri hidroxit:
$ZnO + 2NaOH rightarrow Na_2ZnO_2 + H_2O$ (natri zincat)
4.4. Danh Sách Các Oxit Lưỡng Tính Phổ Biến
Một số oxit lưỡng tính phổ biến bao gồm:
- Nhôm oxit ($Al_2O_3$)
- Kẽm oxit ($ZnO$)
- Thiếc oxit ($SnO$)
- Crôm(III) oxit ($Cr_2O_3$)
4.5. Bảng Tổng Hợp Tính Chất Hóa Học Của Oxit Lưỡng Tính
| Phản Ứng | Phương Trình Tổng Quát | Ví Dụ |
|---|---|---|
| Oxit lưỡng tính + Axit | $Oxit ; lưỡng ; tính + Axit rightarrow Muối + Nước$ | $Al_2O_3 + 6HCl rightarrow 2AlCl_3 + 3H_2O$ |
| Oxit lưỡng tính + Dung dịch bazơ | $Oxit ; lưỡng ; tính + Bazơ rightarrow Muối + Nước$ | $ZnO + 2NaOH rightarrow Na_2ZnO_2 + H_2O$ |
5. Oxit Trung Tính (Oxit Không Tạo Muối)
Oxit trung tính là những oxit không tác dụng với axit, bazơ và nước. Chúng thường là oxit của các nguyên tố phi kim có số oxi hóa thấp.
5.1. Định Nghĩa Oxit Trung Tính
Oxit trung tính là loại oxit không thể tạo ra muối khi tác dụng với axit hoặc bazơ. Chúng không có tính axit hoặc tính bazơ rõ rệt.
5.2. Các Oxit Trung Tính Phổ Biến
Một số oxit trung tính phổ biến bao gồm:
- Cacbon monoxit (CO)
- Nitơ monoxit (NO)
- Đinitơ oxit ($N_2O$)
5.3. Ứng Dụng Của Oxit Trung Tính
Mặc dù không tham gia vào các phản ứng tạo muối, oxit trung tính vẫn có nhiều ứng dụng quan trọng. Ví dụ, cacbon monoxit được sử dụng trong sản xuất hóa chất và luyện kim, nitơ monoxit có vai trò trong sinh học và y học.
6. Ứng Dụng Thực Tế Của Oxit Trong Đời Sống Và Công Nghiệp
Oxit có rất nhiều ứng dụng quan trọng trong đời sống và công nghiệp, từ sản xuất vật liệu xây dựng đến công nghệ điện tử và y học.
6.1. Trong Xây Dựng
- Canxi oxit (CaO): Còn gọi là vôi sống, được sử dụng để sản xuất vữa xây dựng, xi măng và các vật liệu xây dựng khác.
- Silic đioxit (SiO2): Thành phần chính của cát và thạch anh, được sử dụng trong sản xuất thủy tinh, gốm sứ và bê tông. Theo Tổng cục Thống kê, ngành xây dựng sử dụng hàng triệu tấn oxit mỗi năm, đóng góp lớn vào sự phát triển kinh tế.
6.2. Trong Nông Nghiệp
- Canxi oxit (CaO): Được sử dụng để cải tạo đất chua, khử trùng đất và cung cấp canxi cho cây trồng.
- Photpho pentaoxit (P2O5): Nguyên liệu để sản xuất phân lân, cung cấp photpho cho cây trồng, giúp tăng năng suất và chất lượng nông sản.
6.3. Trong Công Nghiệp Luyện Kim
- Sắt(III) oxit (Fe2O3): Nguyên liệu chính để sản xuất gang và thép trong các lò luyện kim.
- Nhôm oxit (Al2O3): Sử dụng trong sản xuất nhôm và các hợp kim nhôm, có tính chất nhẹ, bền và chống ăn mòn.
6.4. Trong Công Nghiệp Hóa Chất
- Lưu huỳnh trioxit (SO3): Nguyên liệu để sản xuất axit sulfuric (H2SO4), một hóa chất quan trọng được sử dụng rộng rãi trong nhiều ngành công nghiệp.
- Titan đioxit (TiO2): Sử dụng làm chất tạo màu trắng trong sơn, nhựa, giấy và mỹ phẩm. Theo Bộ Công Thương, ngành hóa chất sử dụng oxit để sản xuất ra hàng ngàn sản phẩm khác nhau, phục vụ nhu cầu tiêu dùng và xuất khẩu.
6.5. Trong Y Học
- Kẽm oxit (ZnO): Sử dụng trong các loại kem chống nắng, thuốc mỡ trị bỏng và các sản phẩm chăm sóc da, có tác dụng bảo vệ da khỏi tác hại của tia UV và làm dịu da.
- Nhôm oxit (Al2O3): Thành phần trong một số loại thuốc kháng axit, giúp giảm triệu chứng ợ nóng và khó tiêu.
6.6. Trong Công Nghệ Điện Tử
- Silic đioxit (SiO2): Sử dụng làm chất cách điện trong các vi mạch và linh kiện điện tử, đảm bảo hoạt động ổn định và hiệu quả của các thiết bị điện tử.
7. Ảnh Hưởng Của Tính Chất Hóa Học Oxit Đến Môi Trường
Tính chất hóa học của oxit không chỉ có ứng dụng rộng rãi mà còn có những ảnh hưởng nhất định đến môi trường.
7.1. Ô Nhiễm Không Khí
Các oxit như lưu huỳnh đioxit ($SO_2$) và nitơ oxit ($NO_x$) là những chất gây ô nhiễm không khí chính. Chúng được thải ra từ các hoạt động công nghiệp, giao thông vận tải và đốt nhiên liệu hóa thạch. Theo báo cáo của Bộ Tài nguyên và Môi trường, nồng độ các oxit này vượt quá tiêu chuẩn cho phép ở nhiều khu vực đô thị và công nghiệp, gây ảnh hưởng đến sức khỏe con người và môi trường.
7.2. Mưa Axit
Lưu huỳnh đioxit và nitơ oxit trong không khí có thể phản ứng với nước tạo thành axit sulfuric ($H_2SO_4$) và axit nitric ($HNO_3$). Khi mưa xuống, các axit này hòa tan trong nước mưa, tạo thành mưa axit. Mưa axit gây hại cho các hệ sinh thái, ăn mòn các công trình xây dựng và ảnh hưởng đến chất lượng nước.
7.3. Hiệu Ứng Nhà Kính
Cacbon đioxit ($CO_2$) là một trong những khí nhà kính chính gây ra biến đổi khí hậu. Nồng độ $CO_2$ trong khí quyển tăng lên do đốt nhiên liệu hóa thạch, phá rừng và các hoạt động công nghiệp. Hiệu ứng nhà kính làm tăng nhiệt độ trái đất, gây ra các hiện tượng thời tiết cực đoan và mực nước biển dâng cao.
7.4. Giải Pháp Giảm Thiểu Tác Động Tiêu Cực
Để giảm thiểu tác động tiêu cực của oxit đến môi trường, cần thực hiện các biện pháp sau:
- Kiểm soát khí thải: Áp dụng các công nghệ xử lý khí thải hiện đại để loại bỏ các oxit gây ô nhiễm trước khi thải ra môi trường.
- Sử dụng năng lượng sạch: Chuyển đổi sang sử dụng các nguồn năng lượng tái tạo như năng lượng mặt trời, năng lượng gió và năng lượng nước để giảm lượng khí thải $CO_2$.
- Tiết kiệm năng lượng: Sử dụng năng lượng hiệu quả trong sản xuất và sinh hoạt để giảm nhu cầu sử dụng nhiên liệu hóa thạch.
- Bảo vệ rừng: Trồng rừng và bảo vệ rừng hiện có để tăng khả năng hấp thụ $CO_2$ từ khí quyển.
8. Các Câu Hỏi Thường Gặp Về Tính Chất Hóa Học Của Oxit (FAQ)
8.1. Oxit là gì và chúng được phân loại như thế nào?
Oxit là hợp chất hóa học được tạo thành từ sự kết hợp giữa oxi và một nguyên tố khác. Chúng được phân loại thành oxit bazơ, oxit axit, oxit lưỡng tính và oxit trung tính, dựa trên tính chất hóa học của chúng.
8.2. Oxit bazơ tác dụng với những chất nào?
Oxit bazơ tác dụng với nước tạo thành bazơ, tác dụng với axit tạo thành muối và nước, và tác dụng với oxit axit tạo thành muối.
8.3. Oxit axit tác dụng với những chất nào?
Oxit axit tác dụng với nước tạo thành axit, tác dụng với bazơ tạo thành muối và nước, và tác dụng với oxit bazơ tạo thành muối.
8.4. Oxit lưỡng tính là gì và chúng có tính chất đặc biệt nào?
Oxit lưỡng tính là oxit có thể tác dụng với cả axit và bazơ để tạo thành muối và nước. Chúng có tính chất của cả oxit axit và oxit bazơ, tùy thuộc vào chất phản ứng.
8.5. Oxit trung tính có tác dụng với axit hoặc bazơ không?
Không, oxit trung tính không tác dụng với axit, bazơ hoặc nước.
8.6. Ứng dụng của oxit trong đời sống và công nghiệp là gì?
Oxit có nhiều ứng dụng quan trọng trong xây dựng, nông nghiệp, luyện kim, công nghiệp hóa chất, y học và công nghệ điện tử.
8.7. Oxit gây ra những vấn đề môi trường nào?
Một số oxit gây ô nhiễm không khí, mưa axit và hiệu ứng nhà kính, ảnh hưởng đến sức khỏe con người và môi trường.
8.8. Làm thế nào để giảm thiểu tác động tiêu cực của oxit đến môi trường?
Cần kiểm soát khí thải, sử dụng năng lượng sạch, tiết kiệm năng lượng và bảo vệ rừng để giảm thiểu tác động tiêu cực của oxit đến môi trường.
8.9. Tại sao cần phải hiểu rõ về tính chất hóa học của oxit?
Hiểu rõ về tính chất hóa học của oxit giúp chúng ta dự đoán và kiểm soát các phản ứng hóa học, ứng dụng chúng vào các lĩnh vực khác nhau và giảm thiểu tác động tiêu cực đến môi trường.
8.10. Oxit nào được sử dụng phổ biến nhất trong ngành xây dựng?
Canxi oxit (CaO) và silic đioxit (SiO2) là hai oxit được sử dụng phổ biến nhất trong ngành xây dựng.
9. Tại Sao Nên Tìm Hiểu Về Xe Tải Tại Xe Tải Mỹ Đình?
Bạn đang tìm kiếm thông tin đáng tin cậy về xe tải ở Mỹ Đình, Hà Nội? XETAIMYDINH.EDU.VN là địa chỉ bạn không thể bỏ qua. Chúng tôi cung cấp thông tin chi tiết và cập nhật về các loại xe tải, giá cả, địa điểm mua bán uy tín và dịch vụ sửa chữa chất lượng.
 Hình ảnh minh họa xe tải các loại
Hình ảnh minh họa xe tải các loại
Xe Tải Mỹ Đình cam kết mang đến cho bạn những thông tin chính xác và hữu ích nhất, giúp bạn đưa ra quyết định sáng suốt khi mua xe tải. Với đội ngũ chuyên gia giàu kinh nghiệm, chúng tôi sẵn sàng tư vấn và giải đáp mọi thắc mắc của bạn về xe tải.
Đừng bỏ lỡ cơ hội tìm hiểu thông tin chi tiết và nhận tư vấn miễn phí tại XETAIMYDINH.EDU.VN. Hãy liên hệ với chúng tôi ngay hôm nay để được hỗ trợ tốt nhất!
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
Hotline: 0247 309 9988
Trang web: XETAIMYDINH.EDU.VN
Lời kêu gọi hành động (CTA): Truy cập XETAIMYDINH.EDU.VN ngay hôm nay để khám phá thế giới xe tải và nhận tư vấn chuyên nghiệp từ đội ngũ của chúng tôi. Hãy để Xe Tải Mỹ Đình đồng hành cùng bạn trên mọi nẻo đường!
