Zn hóa trị mấy? Tìm hiểu chi tiết về tính chất lý hóa và ứng dụng của kẽm ngay tại XETAIMYDINH.EDU.VN. Bài viết này sẽ cung cấp thông tin chi tiết về kẽm, giúp bạn hiểu rõ hơn về nguyên tố hóa học quan trọng này và các ứng dụng của nó trong đời sống và công nghiệp. Khám phá ngay những kiến thức hữu ích về kẽm, từ hóa trị đến ứng dụng thực tiễn, cùng các thông tin chuyên sâu về kim loại kẽm và hợp chất kẽm.
1. Kẽm (Zn) Là Gì?
Kẽm, ký hiệu Zn, là nguyên tố hóa học thứ 30 trong bảng tuần hoàn. Đây là kim loại lưỡng tính phổ biến trên Trái Đất, chiếm khoảng 0,0075% vỏ Trái Đất và đứng thứ 24 về độ phổ biến. Nồng độ kẽm trong khí quyển dao động từ 0,1 đến 4 microgam/m3, và khoảng 30 ppb trong nước biển.
 Kẽm là kim loại phổ biến trên Trái Đất
Kẽm là kim loại phổ biến trên Trái Đất
2. Zn Hóa Trị Mấy?
Vậy, Zn hóa trị mấy? Đây là câu hỏi nhiều người quan tâm. Kẽm có 2 electron ở lớp ngoài cùng, dễ dàng mất 2e để tạo ion có hóa trị 2+. Do đó, kẽm có hóa trị 2.
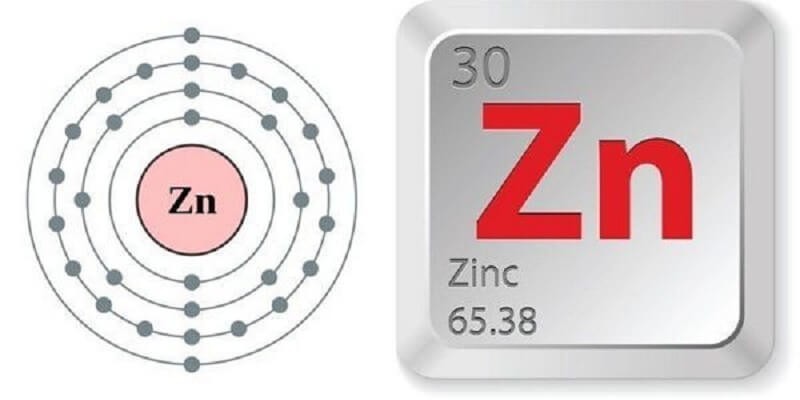 Kẽm có hóa trị 2
Kẽm có hóa trị 2
Kẽm luôn thể hiện hóa trị +2 trong các hợp chất hóa học của mình. Điều này có nghĩa là mỗi nguyên tử kẽm có khả năng liên kết với hai nguyên tử khác thông qua việc nhường hai electron.
3. Trạng Thái Tự Nhiên Của Kẽm
Trong tự nhiên, kẽm không tồn tại ở dạng đơn lẻ mà thường kết hợp với các kim loại khác như chì và đồng trong quặng, hemimorphite, smithsonite, wurtzite,… Trên thị trường, kẽm chủ yếu được khai thác từ quặng sphalerit, có trữ lượng lớn ở nhiều quốc gia như Canada, Mỹ, Úc và Iran. Mỗi năm, hơn 13 triệu tấn kẽm được khai thác, làm cho nó trở thành một trong những kim loại được khai thác nhiều nhất trên thế giới.
4. Tính Chất Vật Lý Của Kẽm
Kẽm dễ nhận biết với màu ánh kim trắng xanh. Cấu trúc tinh thể của kẽm là mạng lưới hexagonal không đều, thuộc loại sáu phương. Nó là chất dẫn điện tốt và dễ bị phá hủy ở mọi điều kiện nhiệt độ. Mặc dù có độ cứng tương đối, kẽm dễ uốn cong và chế tác ở nhiệt độ 100°C – 150°C.
 Tính chất vật lý của kẽm
Tính chất vật lý của kẽm
Bảng 1: Các tính chất vật lý của kẽm
| Tính chất | Giá trị |
|---|---|
| Màu sắc | Ánh kim trắng xanh |
| Cấu trúc tinh thể | Hexagonal không đều (sáu phương) |
| Độ dẫn điện | Tốt |
| Nhiệt độ nóng chảy | 419.58 °C |
| Nhiệt độ sôi | 907 °C |
| Độ cứng (Mohs) | 2.5 |
| Khối lượng riêng | 7.14 g/cm³ |
5. Tính Chất Hóa Học Của Kẽm
Kẽm là kim loại có tính oxi hóa mạnh nhưng mức độ hoạt động trung bình. Khi cháy trong không khí, ngọn lửa chứa kẽm có màu xanh lục đặc trưng. Phản ứng hóa học diễn ra như sau:
2Zn + O2 → 2ZnO
Kẽm tác dụng tốt với phi kim, kiềm và một số axit:
- Tác dụng với phi kim: Zn + Cl2 → ZnCl2
- Tác dụng với dung dịch kiềm: Zn + 2NaOH → Na2ZnO2 + H2
- Tác dụng với axit: Zn + H2SO4 → ZnSO4 + SO2 + 2H2O
Ngoài ra, kẽm không phản ứng với nước ở điều kiện nhiệt độ thường do lớp hydrozincite bảo vệ bên ngoài.
Bảng 2: Phản ứng hóa học đặc trưng của kẽm
| Phản ứng | Mô tả |
|---|---|
| Tác dụng với oxy (O2) | Kẽm cháy trong không khí tạo thành kẽm oxit (ZnO), một chất bột màu trắng. Phản ứng này tỏa nhiệt. |
| Tác dụng với clo (Cl2) | Kẽm phản ứng mạnh mẽ với clo tạo thành kẽm clorua (ZnCl2), một chất rắn không màu, hút ẩm mạnh. |
| Tác dụng với axit clohydric (HCl) | Kẽm tan trong axit clohydric tạo thành kẽm clorua (ZnCl2) và khí hydro (H2). Phản ứng này diễn ra nhanh chóng và thường được sử dụng để điều chế khí hydro trong phòng thí nghiệm. |
| Tác dụng với axit sulfuric loãng (H2SO4) | Kẽm tan trong axit sulfuric loãng tạo thành kẽm sulfat (ZnSO4) và khí hydro (H2). Tốc độ phản ứng chậm hơn so với axit clohydric. |
| Tác dụng với dung dịch kiềm (NaOH) | Kẽm phản ứng với dung dịch kiềm mạnh như natri hydroxit (NaOH) tạo thành các phức chất tan trong nước như natri zincat (Na2ZnO2) và giải phóng khí hydro (H2). Phản ứng này thể hiện tính chất lưỡng tính của kẽm. |
6. Ứng Dụng Của Kẽm
Kẽm là chất hóa học phổ biến và được ứng dụng rộng rãi trong nhiều lĩnh vực khác nhau.
6.1. Vật Liệu Chống Ăn Mòn
Kẽm dễ bị oxy hóa nên được dùng làm vật liệu chống ăn mòn cho cầu treo, hàng rào thép gai, thiết bị trao đổi nhiệt,… Quá trình mạ kẽm giúp bảo vệ kim loại khỏi bị ăn mòn, kéo dài tuổi thọ của sản phẩm. Theo Tổng cục Thống kê, việc sử dụng kẽm trong bảo vệ chống ăn mòn đã giúp giảm thiểu thiệt hại kinh tế đáng kể cho các ngành công nghiệp.
6.2. Tạo Hợp Kim
Đồng thau là hợp kim phổ biến nhất của kẽm, bao gồm đồng và kẽm, được dùng trong sản phẩm âm nhạc, thiết bị truyền thông,… Hợp kim kẽm có độ bền cao, khả năng chống ăn mòn tốt và dễ gia công, nên được ứng dụng rộng rãi trong nhiều lĩnh vực.
6.3. Ứng Dụng Trong Công Nghiệp
Một số ứng dụng của kẽm trong công nghiệp:
- Chất khử mùi.
- Sản xuất sơn (chất tạo màu).
- Chất xúc tác trong chế biến cao su.
- Tổng hợp chất hữu cơ.
- Chất phát quang trong màn hình tivi,…
 Ứng dụng của ống thép mạ kẽm trong công nghiệp
Ứng dụng của ống thép mạ kẽm trong công nghiệp
Bảng 3: Ứng dụng của kẽm trong các ngành công nghiệp khác nhau
| Ngành công nghiệp | Ứng dụng của kẽm |
|---|---|
| Xây dựng | Mạ kẽm cho thép để chống ăn mòn trong các công trình xây dựng, cầu đường, nhà xưởng. |
| Ô tô | Sử dụng trong các bộ phận kim loại để chống ăn mòn, trong sản xuất lốp xe để tăng độ bền và tuổi thọ. |
| Điện tử | Thành phần của pin, ắc quy, các linh kiện điện tử. |
| Hóa chất | Chất xúc tác trong sản xuất hóa chất, chất tạo màu trong sơn, chất khử mùi. |
| Nông nghiệp | Vi chất dinh dưỡng trong phân bón, thuốc trừ sâu. |
| Y tế | Thành phần của thuốc mỡ, kem chống nắng, thực phẩm chức năng bổ sung kẽm. |
7. Điều Chế Kẽm
Kẽm trong tự nhiên được khai thác chủ yếu từ quặng sunfit. Quặng này được nghiền nhỏ và trải qua nhiều công đoạn để thu được kẽm tinh khiết.
Quá trình điều chế Zn như sau:
- Tạo phản ứng để quặng sunfit thành kẽm oxit: 2ZnS + 3O2 → 2ZnO + 2SO2
- Khử kẽm oxit ở nhiệt độ cao 950°C bằng CO hoặc Cacbon: 2ZnO + C → 2Zn + CO2 hoặc 2ZnO + 2CO → 2Zn + 2CO2
Ngoài ra, có thể sử dụng H2SO4 để khử kẽm oxit. Phương trình phản ứng:
- ZnO + H2SO4 → ZnSO4 + H2O
- 2ZnSO4 + 2H2O → 2Zn + 2H2SO4 + O2
Sơ đồ quy trình điều chế kẽm từ quặng sunfua
- Khai thác và nghiền quặng: Quặng kẽm sunfua (ZnS) được khai thác từ mỏ và nghiền nhỏ để tăng diện tích bề mặt tiếp xúc cho các giai đoạn xử lý tiếp theo.
- Tuyển nổi: Quặng nghiền được đưa vào quá trình tuyển nổi để tách kẽm sunfua khỏi các tạp chất khác. Trong quá trình này, các hóa chất được thêm vào để làm cho kẽm sunfua bám vào bọt khí và nổi lên trên, trong khi các tạp chất chìm xuống.
- Rang quặng: Kẽm sunfua thu được từ quá trình tuyển nổi được rang trong lò nung ở nhiệt độ cao để chuyển đổi thành kẽm oxit (ZnO). Phản ứng hóa học xảy ra như sau:
2ZnS + 3O2 → 2ZnO + 2SO2
Khí SO2 tạo ra trong quá trình rang quặng được thu hồi để sản xuất axit sulfuric. - Hòa tan kẽm oxit: Kẽm oxit được hòa tan trong axit sulfuric loãng (H2SO4) để tạo thành dung dịch kẽm sulfat (ZnSO4). Phản ứng hóa học xảy ra như sau:
ZnO + H2SO4 → ZnSO4 + H2O - Điện phân: Dung dịch kẽm sulfat được đưa vào quá trình điện phân để thu được kẽm kim loại. Quá trình điện phân sử dụng dòng điện một chiều để khử ion kẽm (Zn2+) thành kẽm kim loại (Zn) tại catot. Phản ứng hóa học xảy ra như sau:
Zn2+ + 2e- → Zn
Kẽm kim loại được thu thập tại catot và cạo ra. - Tinh luyện (tùy chọn): Kẽm kim loại thu được từ quá trình điện phân có thể được tinh luyện thêm để loại bỏ các tạp chất còn lại và nâng cao độ tinh khiết. Quá trình tinh luyện có thể được thực hiện bằng phương pháp điện phân hoặc phương pháp дистилляции.
8. Vai Trò Của Kẽm Với Sức Khỏe Con Người
Kẽm là nguyên tố vi lượng quan trọng trong cơ thể, giúp ích rất nhiều cho sức khỏe:
- Não bộ cần kẽm để thúc đẩy sự phát triển. Trẻ nhỏ hấp thu đủ kẽm sẽ cải thiện trí thông minh và nhận thức. Theo nghiên cứu của Viện Dinh dưỡng Quốc gia, thiếu kẽm ở trẻ em có thể dẫn đến chậm phát triển trí tuệ và thể chất.
- Kẽm tham gia vào quá trình tạo cấu trúc tế bào.
- Hỗ trợ các enzyme chuyển hóa của cơ thể.
- Kẽm là một phần quan trọng trong quá trình tổng hợp tế bào, protein, AND, ARN và hệ xương.
- Điều hòa Glucose và tham gia tạo hormone giới tính.
- Đóng vai trò quan trọng trong chuyển hóa các nguyên tố vi lượng khác.
- Tốt cho hệ miễn dịch, da, tóc, móng,…
Bảng 4: Vai trò của kẽm đối với sức khỏe con người
| Chức năng | Vai trò của kẽm |
|---|---|
| Hệ miễn dịch | Kẽm giúp tăng cường hệ miễn dịch bằng cách kích thích sản xuất các tế bào miễn dịch và tăng cường chức năng của chúng. Nó cũng giúp bảo vệ tế bào khỏi tổn thương do các gốc tự do. |
| Phát triển và tăng trưởng | Kẽm rất cần thiết cho sự phát triển và tăng trưởng bình thường của cơ thể, đặc biệt là ở trẻ em và thanh thiếu niên. Nó tham gia vào quá trình tổng hợp protein, DNA và RNA, cũng như quá trình phân chia tế bào. |
| Chức năng thần kinh | Kẽm đóng vai trò quan trọng trong chức năng thần kinh, bao gồm truyền tín hiệu thần kinh, học tập và trí nhớ. |
| Chức năng sinh sản | Kẽm rất cần thiết cho chức năng sinh sản bình thường ở cả nam và nữ. Ở nam giới, nó tham gia vào sản xuất tinh trùng và hormone testosterone. Ở nữ giới, nó tham gia vào quá trình rụng trứng và mang thai. |
| Chữa lành vết thương | Kẽm giúp thúc đẩy quá trình chữa lành vết thương bằng cách kích thích sản xuất collagen và các tế bào da mới. |
| Thị giác | Kẽm đóng vai trò quan trọng trong thị giác bằng cách giúp vận chuyển vitamin A từ gan đến võng mạc. |
| Vị giác và khứu giác | Kẽm cần thiết cho vị giác và khứu giác bình thường. |
Qua bài viết này, Xe Tải Mỹ Đình hy vọng bạn đã hiểu rõ Zn hóa trị mấy, tính chất và ứng dụng của kẽm. Nếu bạn muốn tìm hiểu thêm về nguyên tố hóa học này, hãy liên hệ với Xe Tải Mỹ Đình qua hotline 0247 309 9988 hoặc truy cập XETAIMYDINH.EDU.VN để được tư vấn cụ thể. Địa chỉ của chúng tôi là Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội. Đừng ngần ngại liên hệ để được giải đáp mọi thắc mắc!
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình? Bạn muốn so sánh giá cả, thông số kỹ thuật và nhận tư vấn lựa chọn xe phù hợp? Hãy truy cập ngay XETAIMYDINH.EDU.VN để khám phá thế giới xe tải đa dạng và nhận sự hỗ trợ tận tâm từ đội ngũ chuyên gia của chúng tôi.
FAQ – Câu Hỏi Thường Gặp Về Kẽm (Zn)
1. Tại sao kẽm lại quan trọng đối với sức khỏe con người?
Kẽm là một khoáng chất thiết yếu tham gia vào nhiều quá trình sinh học quan trọng, bao gồm chức năng miễn dịch, tổng hợp protein, chữa lành vết thương, và phát triển tế bào.
2. Thiếu kẽm có thể gây ra những vấn đề sức khỏe nào?
Thiếu kẽm có thể dẫn đến suy giảm hệ miễn dịch, chậm phát triển ở trẻ em, các vấn đề về da, rụng tóc, và suy giảm vị giác.
3. Làm thế nào để đảm bảo cung cấp đủ kẽm cho cơ thể?
Bạn có thể tăng cường kẽm thông qua chế độ ăn uống giàu kẽm (thịt đỏ, hải sản, các loại hạt) hoặc sử dụng thực phẩm chức năng bổ sung kẽm theo chỉ định của bác sĩ.
4. Kẽm có độc hại không?
Tiêu thụ quá nhiều kẽm có thể gây ra các tác dụng phụ như buồn nôn, nôn mửa, đau bụng và tiêu chảy. Liều lượng kẽm an toàn hàng ngày là khoảng 11mg cho nam giới và 8mg cho nữ giới.
5. Kẽm được sử dụng trong ngành công nghiệp nào?
Kẽm được sử dụng rộng rãi trong nhiều ngành công nghiệp, bao gồm sản xuất thép mạ kẽm, hợp kim (đồng thau), pin, sơn, và dược phẩm.
6. Tại sao kẽm lại được sử dụng để mạ thép?
Kẽm có khả năng chống ăn mòn cao, giúp bảo vệ thép khỏi bị gỉ sét và kéo dài tuổi thọ của sản phẩm.
7. Kẽm có ảnh hưởng đến môi trường không?
Kẽm có thể gây ô nhiễm môi trường nếu không được xử lý đúng cách. Các hoạt động khai thác và sản xuất kẽm cần tuân thủ các quy định về bảo vệ môi trường để giảm thiểu tác động tiêu cực.
8. Kẽm có thể tái chế được không?
Có, kẽm là một kim loại có thể tái chế được. Quá trình tái chế kẽm giúp tiết kiệm năng lượng và tài nguyên thiên nhiên.
9. Các loại thực phẩm nào giàu kẽm nhất?
Các loại thực phẩm giàu kẽm bao gồm thịt đỏ, hải sản (đặc biệt là hàu), các loại hạt (hạnh nhân, hạt điều), đậu, và ngũ cốc nguyên hạt.
10. Kẽm có tương tác với các loại thuốc nào không?
Kẽm có thể tương tác với một số loại thuốc, bao gồm thuốc kháng sinh tetracycline và quinolone, thuốc lợi tiểu thiazide, và thuốc ức chế ACE. Hãy tham khảo ý kiến bác sĩ hoặc dược sĩ nếu bạn đang sử dụng các loại thuốc này và muốn bổ sung kẽm.