Bạn đang muốn tìm hiểu phản ứng oxi hóa khử là gì? Bài viết này của Xe Tải Mỹ Đình sẽ cung cấp định nghĩa chi tiết, các dấu hiệu nhận biết, ví dụ minh họa và ứng dụng thực tế của phản ứng oxi hóa khử, giúp bạn hiểu rõ bản chất và tầm quan trọng của nó trong hóa học và đời sống.
1. Phản Ứng Oxi Hóa Khử Là Gì?
Phản ứng oxi hóa khử là một loại phản ứng hóa học, trong đó có sự thay đổi số oxi hóa của một hoặc nhiều nguyên tố. Hiểu một cách đơn giản, đây là quá trình chuyển electron giữa các chất phản ứng. Theo nghiên cứu của Trường Đại học Khoa học Tự nhiên Hà Nội, Khoa Hóa học, năm 2023, phản ứng oxi hóa khử đóng vai trò then chốt trong nhiều quá trình tự nhiên và công nghiệp.
- Chất khử: Chất nhường electron, làm tăng số oxi hóa của mình.
- Chất oxi hóa: Chất nhận electron, làm giảm số oxi hóa của mình.
- Quá trình oxi hóa: Quá trình chất khử nhường electron.
- Quá trình khử: Quá trình chất oxi hóa nhận electron.
Ví dụ về phản ứng oxi hóa khử:
Fe + CuSO4 -> Cu + FeSO4Trong phản ứng này:
- Sắt (Fe) là chất khử, số oxi hóa tăng từ 0 lên +2 (Fe0 → Fe2+ + 2e).
- Đồng (Cu) trong CuSO4 là chất oxi hóa, số oxi hóa giảm từ +2 xuống 0 (Cu2+ + 2e → Cu0).
Kết luận: Phản ứng trên là phản ứng oxi hóa khử vì có đồng thời sự oxi hóa và sự khử.
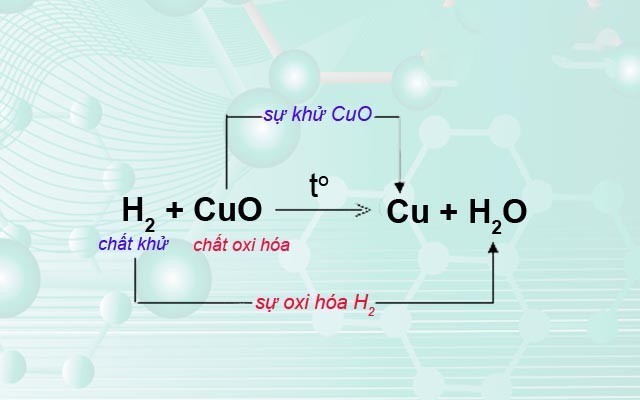
2. Dấu Hiệu Nhận Biết Phản Ứng Oxi Hóa Khử
Dấu hiệu chính để nhận biết phản ứng oxi hóa khử là sự thay đổi số oxi hóa của các nguyên tố trước và sau phản ứng.
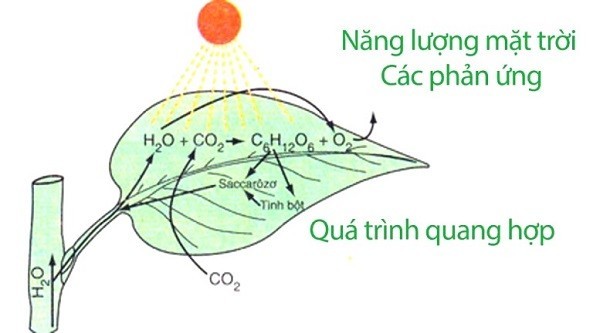 Quá trình quang hợp của cây xanh cũng là một phản ứng oxi hóa – khử
Quá trình quang hợp của cây xanh cũng là một phản ứng oxi hóa – khử
Phản ứng oxi hóa khử có mặt ở khắp nơi trong đời sống:
- Quá trình hô hấp của thực vật: Cây xanh hấp thụ CO2 và giải phóng O2, đồng thời thực hiện các quá trình trao đổi chất phức tạp.
- Sự đốt cháy nhiên liệu: Động cơ đốt trong hoạt động dựa trên phản ứng oxi hóa khử giữa nhiên liệu và oxi.
- Quá trình điện phân: Ứng dụng trong sản xuất nhôm, clo, và các kim loại khác.
- Phản ứng trong pin: Pin hoạt động dựa trên phản ứng oxi hóa khử để tạo ra dòng điện.
Ngoài ra, nhiều quy trình sản xuất công nghiệp như luyện kim, sản xuất chất dẻo, dược phẩm, phân bón hóa học,… đều dựa trên các phản ứng oxi hóa khử.
3. Các Bước Viết Phương Trình Phản Ứng Oxi Hóa Khử
Để viết và cân bằng phương trình phản ứng oxi hóa khử, bạn có thể thực hiện theo các bước sau:
Bước 1: Xác định số oxi hóa của tất cả các nguyên tố trong phản ứng để tìm ra chất oxi hóa và chất khử.
Bước 2: Viết các phương trình bán phản ứng oxi hóa và bán phản ứng khử. Cân bằng số nguyên tử của mỗi nguyên tố và số electron trao đổi trong mỗi bán phản ứng.
Bước 3: Nhân các bán phản ứng với hệ số thích hợp sao cho tổng số electron nhường bằng tổng số electron nhận. Cộng các bán phản ứng lại để được phương trình phản ứng oxi hóa khử hoàn chỉnh.
4. Các Loại Phản Ứng Oxi Hóa Khử Phổ Biến
Có nhiều loại phản ứng oxi hóa khử khác nhau, bao gồm:
-
Phản ứng oxi hóa khử thông thường: Chất oxi hóa và chất khử thuộc về các phân tử khác nhau.
- Ví dụ 1: C + 4HNO3 (đặc) → CO2 + 4NO2 + 2H2O
- Ví dụ 2: Cu + 2H2SO4 (đặc) → CuSO4 + SO2 + 2H2O
-
Phản ứng oxi hóa khử nội phân tử: Chất oxi hóa và chất khử cùng thuộc về một phân tử, nhưng ở các nguyên tử khác nhau.
- Ví dụ 1: AgNO3 → Ag + NO2 + O2
- Ví dụ 2: Cu(NO3)2 → CuO + NO2 + O2
-
Phản ứng tự oxi hóa khử (tự phản ứng): Một chất vừa là chất oxi hóa, vừa là chất khử.
- Ví dụ 1: Cl2 + 2KOH → KCl + KClO + H2O
- Ví dụ 2: 4KClO3 → 3KClO4 + KCl
5. Ví Dụ Về Phản Ứng Oxi Hóa Khử Trong Hóa Học Lớp 10
Dưới đây là một số ví dụ cụ thể về phản ứng oxi hóa khử thường gặp trong chương trình hóa học lớp 10:
5.1. Phản Ứng Giữa Al và HNO3
Trong phản ứng giữa nhôm (Al) và axit nitric (HNO3), hãy xác định sự thay đổi số oxi hóa của các nguyên tố.
5.2. Phản Ứng Của KMnO4
Trong phản ứng giữa kali pemanganat (KMnO4) và axit clohidric (HCl), xác định số oxi hóa của các nguyên tố thay đổi.
 Phản ứng oxi hóa khử bài tập 2
Phản ứng oxi hóa khử bài tập 2
5.3. Phản Ứng Giữa Cu và H2SO4
Trong phản ứng giữa đồng (Cu) và axit sulfuric (H2SO4), hãy xác định số oxi hóa của các nguyên tố thay đổi.
 Phản ứng oxi hóa khử bài tập 3
Phản ứng oxi hóa khử bài tập 3
6. Bài Tập Vận Dụng Về Phản Ứng Oxi Hóa Khử Lớp 10
Để củng cố kiến thức, hãy cùng xem xét một số bài tập thường gặp về phản ứng oxi hóa khử:
 Giải bài tập phản ứng oxi hóa khử hóa 10
Giải bài tập phản ứng oxi hóa khử hóa 10
Bài tập 1: Xác định phản ứng nào sau đây là phản ứng oxi hóa khử:
A: 2HgO → 2Hg + O2
B: CaCO3 → CaO + CO2
C: 2Al(OH)3 → Al2O3 + 3H2O
D: 2NaHCO3 → Na2CO3 + CO2 + H2O
Lời giải: Đáp án đúng là A. Các đáp án khác không có sự thay đổi số oxi hóa của các nguyên tố.
2HgO → 2Hg + O2
Hg2+ + 2e → Hg0
2O2- → O2 + 4e
Bài tập 2: Trong phản ứng nào sau đây, NH3 đóng vai trò là chất khử?
A: 4NH3 + 5O2 → 4NO + 6H2O
B: 2NH3 + 3Cl2 → N2 + 6HCl
C: 2NH3 + 3CuO → 3Cu + N2 + 3H2O
D: 2NH3 + H2O2 + MnSO4 → MnO2 + (NH4)2SO4
Lời giải: Đáp án đúng là A, vì N trong NH3 tăng số oxi hóa từ -3 lên +2 trong NO.
Bài tập 3: Phản ứng nào sau đây là phản ứng oxi hóa khử?
A: HNO3 + NaOH → NaNO3 + H2O
B: N2O5 + H2O → 2HNO3
C: 2HNO3 + 3H2S → 3S + 2NO + 4H2O
D: 2Fe(OH)3 → Fe2O3 + 3H2O
Lời giải: Đáp án đúng là C. Trong phản ứng này, S trong H2S bị oxi hóa thành S, và N trong HNO3 bị khử thành NO.
Bài tập 4: Phản ứng oxi hóa khử là gì? Cho 3 ví dụ.
Lời giải: Phản ứng oxi hóa khử là phản ứng hóa học, trong đó có sự chuyển electron giữa các chất phản ứng.
Ví dụ:
- H2 + Cl2 → 2HCl
- Fe + 2HCl → FeCl2 + H2
- FeCl2 + Cl2 → 2FeCl3
Bài tập 5: Cần bao nhiêu gam đồng để khử hoàn toàn lượng ion bạc có trong 85ml dung dịch AgNO3 0,15M?
Lời giải:
VAgNO3 = 85 ml = 85/1000 lít
→ Cm = n/V => n = (0,15 x 85)/1000 = 0,01275 mol
Phương trình phản ứng:
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Theo phương trình, ta có:
nCu = ½ nAgNO3 = 0,01275/2 = 0,006375 mol
Vậy mCu = 0,006375 x 64 = 0,408g.
Ngoài ra, có rất nhiều dạng bài tập phản ứng oxi hóa khử lớp 10 nâng cao khác. Tùy thuộc vào từng đề bài mà chúng ta sẽ đưa ra phương án giải phù hợp.
7. Ứng Dụng Quan Trọng Của Phản Ứng Oxi Hóa Khử Trong Đời Sống Và Công Nghiệp
Phản ứng oxi hóa khử đóng vai trò vô cùng quan trọng trong nhiều lĩnh vực:
- Sản xuất điện: Các loại pin và ắc quy hoạt động dựa trên phản ứng oxi hóa khử để tạo ra dòng điện.
- Luyện kim: Quá trình luyện gang, thép từ quặng sắt sử dụng các phản ứng khử oxit sắt bằng than cốc.
- Xử lý nước: Ozon hóa và clo hóa sử dụng phản ứng oxi hóa khử để khử trùng và loại bỏ các chất ô nhiễm trong nước. Theo báo cáo của Bộ Tài nguyên và Môi trường năm 2024, các phương pháp này giúp cải thiện đáng kể chất lượng nguồn nước.
- Sản xuất hóa chất: Nhiều hóa chất quan trọng như axit sulfuric, axit nitric, clo, và các loại phân bón được sản xuất thông qua các phản ứng oxi hóa khử.
- Bảo vệ môi trường: Các hệ thống xử lý khí thải sử dụng phản ứng oxi hóa khử để loại bỏ các chất độc hại như NOx và SO2.
- Trong y học: Các chất oxi hóa như oxy già (H2O2) được sử dụng để sát trùng vết thương.
- Trong công nghiệp thực phẩm: Phản ứng oxi hóa khử xảy ra trong quá trình lên men, giúp sản xuất các loại thực phẩm như rượu, bia, sữa chua…
8. Lưu Ý Khi Học Về Phản Ứng Oxi Hóa Khử
Để nắm vững kiến thức về phản ứng oxi hóa khử, bạn cần lưu ý:
- Nắm vững khái niệm: Hiểu rõ định nghĩa chất oxi hóa, chất khử, quá trình oxi hóa, quá trình khử.
- Xác định số oxi hóa: Luyện tập xác định số oxi hóa của các nguyên tố trong hợp chất.
- Cân bằng phương trình: Thành thạo các phương pháp cân bằng phương trình phản ứng oxi hóa khử.
- Vận dụng linh hoạt: Giải nhiều bài tập khác nhau để làm quen với các dạng bài và cách giải.
- Liên hệ thực tế: Tìm hiểu các ứng dụng của phản ứng oxi hóa khử trong đời sống và công nghiệp để hiểu rõ hơn tầm quan trọng của nó.
9. FAQ – Câu Hỏi Thường Gặp Về Phản Ứng Oxi Hóa Khử
-
Phản ứng oxi hóa khử có bắt buộc phải có mặt cả chất oxi hóa và chất khử không?
- Có, phản ứng oxi hóa khử luôn có sự tham gia đồng thời của chất oxi hóa (nhận electron) và chất khử (nhường electron).
-
Số oxi hóa là gì và làm thế nào để xác định nó?
- Số oxi hóa là điện tích hình thức của một nguyên tử trong một hợp chất, giả định rằng tất cả các liên kết đều là ion. Có các quy tắc cụ thể để xác định số oxi hóa, ví dụ như số oxi hóa của oxi thường là -2, của hidro thường là +1, v.v.
-
Làm thế nào để cân bằng một phương trình phản ứng oxi hóa khử?
- Có hai phương pháp chính để cân bằng phản ứng oxi hóa khử: phương pháp thăng bằng electron và phương pháp ion-electron (nửa phản ứng). Cả hai phương pháp đều dựa trên việc đảm bảo tổng số electron nhường bằng tổng số electron nhận.
-
Phản ứng oxi hóa khử có xảy ra trong môi trường axit và bazơ không?
- Có, phản ứng oxi hóa khử có thể xảy ra trong cả môi trường axit và bazơ. Môi trường có thể ảnh hưởng đến quá trình phản ứng và các sản phẩm tạo thành.
-
Phản ứng oxi hóa khử có ứng dụng trong lĩnh vực năng lượng không?
- Có, phản ứng oxi hóa khử là cơ sở của nhiều công nghệ năng lượng, ví dụ như pin nhiên liệu, trong đó oxi hóa hidro tạo ra điện và nước.
-
Phản ứng ăn mòn kim loại có phải là một dạng của phản ứng oxi hóa khử không?
- Đúng vậy, ăn mòn kim loại là một quá trình oxi hóa khử, trong đó kim loại bị oxi hóa bởi các tác nhân trong môi trường như oxi và nước.
-
Chất xúc tác có vai trò gì trong phản ứng oxi hóa khử?
- Chất xúc tác có thể làm tăng tốc độ phản ứng oxi hóa khử bằng cách cung cấp một cơ chế phản ứng khác có năng lượng hoạt hóa thấp hơn, nhưng bản thân chất xúc tác không bị tiêu thụ trong phản ứng.
-
Phản ứng quang hợp ở cây xanh có phải là một phản ứng oxi hóa khử không?
- Có, quang hợp là một phản ứng oxi hóa khử phức tạp, trong đó nước bị oxi hóa để tạo ra oxi, và carbon dioxide bị khử để tạo ra glucose.
-
Phản ứng oxi hóa khử có liên quan đến các vấn đề môi trường như thế nào?
- Phản ứng oxi hóa khử có liên quan đến nhiều vấn đề môi trường, ví dụ như sự hình thành mưa axit (do oxi hóa sulfur dioxide) và sự phân hủy các chất ô nhiễm hữu cơ.
-
Làm thế nào để phân biệt phản ứng oxi hóa khử với các loại phản ứng hóa học khác?
- Dấu hiệu chính để phân biệt phản ứng oxi hóa khử là sự thay đổi số oxi hóa của các nguyên tố trong phản ứng. Các loại phản ứng khác như phản ứng trung hòa, phản ứng trao đổi không có sự thay đổi này.
10. Xe Tải Mỹ Đình – Địa Chỉ Tin Cậy Cho Mọi Thông Tin Về Xe Tải
Hy vọng rằng, với những chia sẻ vừa rồi, bạn đã hiểu rõ hơn về phản ứng oxi hóa khử, các dấu hiệu nhận biết và ứng dụng của nó. Nếu bạn có bất kỳ thắc mắc nào khác, đừng ngần ngại truy cập XETAIMYDINH.EDU.VN để tìm hiểu thêm thông tin chi tiết và được tư vấn tận tình.
Bạn đang tìm kiếm thông tin về các loại xe tải, giá cả, địa điểm mua bán uy tín, hay dịch vụ sửa chữa và bảo dưỡng chất lượng? Xe Tải Mỹ Đình sẽ giúp bạn giải quyết mọi lo ngại:
- Thông tin chi tiết và cập nhật: Về các loại xe tải có sẵn ở Mỹ Đình, Hà Nội.
- So sánh giá cả và thông số kỹ thuật: Giúp bạn lựa chọn xe phù hợp với nhu cầu và ngân sách.
- Tư vấn chuyên nghiệp: Giải đáp mọi thắc mắc liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải.
- Dịch vụ sửa chữa uy tín: Cung cấp thông tin về các dịch vụ sửa chữa xe tải uy tín trong khu vực.
Hãy đến với Xe Tải Mỹ Đình để trải nghiệm sự khác biệt!
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
Hotline: 0247 309 9988
Trang web: XETAIMYDINH.EDU.VN
Liên hệ ngay với Xe Tải Mỹ Đình để được tư vấn và giải đáp mọi thắc mắc về xe tải!