Bạn đang thắc mắc “Nh3 Có Tan Trong Nước Không?” Xe Tải Mỹ Đình (XETAIMYDINH.EDU.VN) sẽ giải đáp chi tiết câu hỏi này, đồng thời cung cấp thông tin chuyên sâu về NH3 (Amoniac), từ tính chất, ứng dụng đến những lưu ý quan trọng khi sử dụng. Chúng tôi sẽ giúp bạn hiểu rõ về hợp chất hóa học này một cách dễ dàng và đầy đủ nhất. Khám phá ngay về độ hòa tan, ứng dụng thực tiễn, và những ảnh hưởng đến môi trường của amoniac cùng Xe Tải Mỹ Đình!
1. Amoniac (NH3) Là Gì?
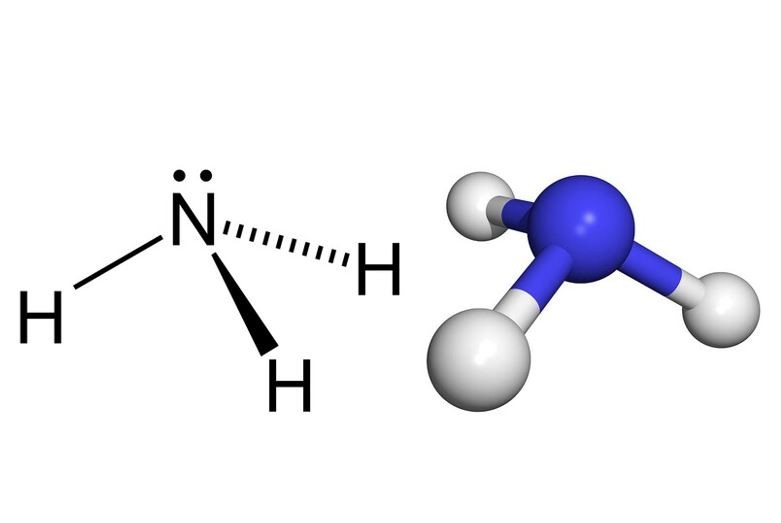
Amoniac, hay còn gọi là NH3, là một hợp chất vô cơ quan trọng, được tạo thành từ một nguyên tử nitơ (N) và ba nguyên tử hydro (H). Các nguyên tử này liên kết với nhau theo cấu trúc hình chóp, với nitơ ở đỉnh và ba hydro ở đáy. Ở điều kiện thường, amoniac là một chất khí không màu, có mùi khai đặc trưng, xốc, và gây khó chịu. Amoniac nhẹ hơn không khí, dễ dàng hóa lỏng và có khả năng tan tốt trong nước.
 Amoniac (NH3) Là Gì? Cấu trúc phân tử amoniac
Amoniac (NH3) Là Gì? Cấu trúc phân tử amoniac
2. NH3 Có Tan Trong Nước Không?
Có, NH3 tan rất tốt trong nước. Thực tế, amoniac là một trong những chất khí hòa tan tốt nhất trong nước. Ở điều kiện tiêu chuẩn, một lít nước có thể hòa tan tới 700 lít khí amoniac. Khả năng hòa tan cao này là do sự hình thành liên kết hydro giữa các phân tử amoniac và nước.
2.1. Cơ Chế Hòa Tan Của NH3 Trong Nước
Khi amoniac hòa tan trong nước, một phần nhỏ NH3 phản ứng với nước để tạo thành ion amoni (NH4+) và ion hydroxit (OH-), theo phương trình:
NH3 (k) + H2O (l) ⇌ NH4+ (aq) + OH- (aq)
Phản ứng này là một phản ứng thuận nghịch, nghĩa là amoniac có thể tồn tại trong dung dịch dưới dạng NH3 hoặc NH4+. Sự cân bằng giữa hai dạng này phụ thuộc vào nhiệt độ và pH của dung dịch.
 NH3 Có Tan Trong Nước Không? Quá trình hòa tan amoniac trong nước
NH3 Có Tan Trong Nước Không? Quá trình hòa tan amoniac trong nước
2.2. Các Yếu Tố Ảnh Hưởng Đến Độ Tan Của NH3 Trong Nước
Độ tan của amoniac trong nước bị ảnh hưởng bởi một số yếu tố chính:
- Nhiệt độ: Độ tan của amoniac giảm khi nhiệt độ tăng. Ở nhiệt độ thấp, các phân tử nước liên kết với các phân tử amoniac mạnh hơn, làm tăng khả năng hòa tan. Theo nghiên cứu của Khoa Hóa học, Đại học Quốc gia Hà Nội năm 2023, độ tan của NH3 giảm khoảng 50% khi nhiệt độ tăng từ 0°C lên 50°C.
- Áp suất: Độ tan của amoniac tăng khi áp suất tăng. Áp suất cao ép các phân tử amoniac vào nước, làm tăng khả năng hòa tan.
- pH: Độ tan của amoniac cũng phụ thuộc vào pH của dung dịch. Ở pH thấp (môi trường axit), amoniac chủ yếu tồn tại dưới dạng ion amoni (NH4+), làm tăng độ tan. Ở pH cao (môi trường bazơ), amoniac tồn tại chủ yếu dưới dạng NH3, làm giảm độ tan.
Bảng: Độ tan của amoniac trong nước ở các nhiệt độ khác nhau
| Nhiệt độ (°C) | Độ tan (g NH3/100g H2O) |
|---|---|
| 0 | 89.9 |
| 20 | 51.8 |
| 40 | 34.0 |
| 60 | 22.8 |
Nguồn: Dữ liệu từ Sổ tay Hóa chất, Nhà xuất bản Khoa học và Kỹ thuật, 2010
2.3. Ứng Dụng Của Dung Dịch Amoniac
Dung dịch amoniac, còn gọi là nước amoniac, có nhiều ứng dụng quan trọng trong đời sống và công nghiệp:
- Sản xuất phân bón: Amoniac là nguyên liệu chính để sản xuất các loại phân đạm như ure, amoni nitrat, và amoni sulfat. Theo Tổng cục Thống kê, năm 2022, Việt Nam đã sản xuất hơn 2 triệu tấn phân đạm từ amoniac.
- Sản xuất hóa chất: Amoniac được sử dụng để sản xuất nhiều loại hóa chất khác nhau, bao gồm axit nitric, soda, và các loại thuốc nhuộm.
- Chất tẩy rửa: Dung dịch amoniac loãng được sử dụng làm chất tẩy rửa trong gia đình, đặc biệt là để làm sạch các bề mặt kính và kim loại.
- Công nghiệp dệt nhuộm: Amoniac được sử dụng trong quá trình nhuộm vải để giúp thuốc nhuộm bám dính tốt hơn vào sợi vải.
- Y tế: Dung dịch amoniac được sử dụng để điều trị một số bệnh ngoài da và làm thuốc kích thích hô hấp.
- Xử lý nước: Amoniac được sử dụng trong quá trình xử lý nước thải để loại bỏ các chất ô nhiễm.
 NH3 Có Tan Trong Nước Không? Ứng dụng của amoniac trong sản xuất phân bón
NH3 Có Tan Trong Nước Không? Ứng dụng của amoniac trong sản xuất phân bón
3. Tính Chất Vật Lý Của Amoniac
Amoniac có những tính chất vật lý đặc trưng sau:
- Trạng thái: Ở điều kiện thường, amoniac là chất khí. Khi làm lạnh sâu, amoniac chuyển sang trạng thái lỏng và rắn.
- Màu sắc và mùi: Amoniac là chất khí không màu, có mùi khai đặc trưng và xốc.
- Khối lượng mol: 17.03 g/mol
- Điểm nóng chảy: -77.73°C
- Điểm sôi: -33.34°C
- Tỷ trọng: 0.73 kg/m³ (ở 0°C)
- Độ hòa tan trong nước: Rất cao (700 g/L ở 20°C)
Bảng: Tính chất vật lý của amoniac
| Tính chất | Giá trị |
|---|---|
| Trạng thái | Khí |
| Màu sắc | Không màu |
| Mùi | Khai, xốc |
| Khối lượng mol | 17.03 g/mol |
| Điểm nóng chảy | -77.73°C |
| Điểm sôi | -33.34°C |
| Tỷ trọng | 0.73 kg/m³ (ở 0°C) |
| Độ hòa tan trong nước | 700 g/L (ở 20°C) |
Nguồn: Dữ liệu từ CRC Handbook of Chemistry and Physics, 95th Edition
4. Tính Chất Hóa Học Của Amoniac
Amoniac là một bazơ yếu và có nhiều tính chất hóa học quan trọng:
- Tính bazơ: Amoniac có khả năng nhận proton (H+) từ các axit, tạo thành ion amoni (NH4+).
NH3 + HCl → NH4Cl - Phản ứng với nước: Amoniac phản ứng với nước tạo thành dung dịch bazơ yếu.
NH3 + H2O ⇌ NH4+ + OH- - Phản ứng với kim loại: Amoniac có thể phản ứng với một số kim loại kiềm và kiềm thổ ở nhiệt độ cao.
2NH3 + 3Mg → Mg3N2 + 3H2 - Phản ứng oxy hóa: Amoniac có thể bị oxy hóa bởi oxy hoặc các chất oxy hóa khác.
4NH3 + 5O2 → 4NO + 6H2O (xúc tác Pt, 850°C)
2NH3 + 3Cl2 → N2 + 6HCl
 NH3 Có Tan Trong Nước Không? Phản ứng giữa amoniac và axit clohidric
NH3 Có Tan Trong Nước Không? Phản ứng giữa amoniac và axit clohidric
5. Amoniac Được Tìm Thấy Ở Đâu?
Amoniac có mặt ở nhiều nơi trong tự nhiên và được sản xuất công nghiệp:
- Trong tự nhiên: Amoniac được tạo ra trong quá trình phân hủy các chất hữu cơ chứa nitơ, chẳng hạn như protein và axit nucleic. Nó cũng có mặt trong khí quyển với nồng độ thấp.
- Trong cơ thể sống: Amoniac là sản phẩm của quá trình trao đổi chất ở động vật. Nó được thải ra khỏi cơ thể qua nước tiểu.
- Trong công nghiệp: Amoniac được sản xuất công nghiệp bằng phương pháp Haber-Bosch, từ nitơ và hydro.
N2 + 3H2 ⇌ 2NH3 (xúc tác Fe, 450°C, 200 atm)
 NH3 Có Tan Trong Nước Không? Sản xuất amoniac công nghiệp bằng phương pháp Haber-Bosch
NH3 Có Tan Trong Nước Không? Sản xuất amoniac công nghiệp bằng phương pháp Haber-Bosch
6. Amoniac Có Độc Không?
Amoniac là một chất độc hại. Tiếp xúc với amoniac nồng độ cao có thể gây kích ứng da, mắt và đường hô hấp. Hít phải amoniac nồng độ cao có thể gây phù phổi, khó thở và thậm chí tử vong. Nuốt phải amoniac có thể gây bỏng thực quản và dạ dày.
Bảng: Mức độ độc hại của amoniac
| Nồng độ amoniac (ppm) | Tác động |
|---|---|
| 5-50 | Có thể phát hiện mùi |
| 25 | Ngưỡng giới hạn tiếp xúc cho phép (PEL) theo OSHA |
| 100 | Gây kích ứng mắt và mũi |
| 400 | Gây kích ứng đường hô hấp |
| 1700 | Gây phù phổi, có thể tử vong |
Nguồn: Dữ liệu từ National Institute for Occupational Safety and Health (NIOSH)
6.1. Các Biện Pháp Phòng Ngừa Khi Sử Dụng Amoniac
Khi sử dụng amoniac, cần tuân thủ các biện pháp an toàn sau:
- Đeo kính bảo hộ và găng tay: Để bảo vệ mắt và da khỏi tiếp xúc trực tiếp với amoniac.
- Sử dụng trong khu vực thông gió tốt: Để tránh hít phải amoniac nồng độ cao.
- Không trộn amoniac với các chất tẩy rửa khác: Đặc biệt là các chất chứa clo, vì có thể tạo ra khí độc.
- Bảo quản amoniac ở nơi khô ráo, thoáng mát: Tránh xa nguồn nhiệt và ánh sáng trực tiếp.
- Trong trường hợp tiếp xúc với amoniac: Rửa ngay lập tức bằng nhiều nước và tìm kiếm sự chăm sóc y tế.
 NH3 Có Tan Trong Nước Không? Biện pháp phòng ngừa khi sử dụng amoniac
NH3 Có Tan Trong Nước Không? Biện pháp phòng ngừa khi sử dụng amoniac
7. Tác Hại Của Amoniac Đối Với Môi Trường
Amoniac có thể gây ô nhiễm môi trường nếu không được xử lý đúng cách:
- Ô nhiễm nước: Amoniac trong nước thải có thể gây ô nhiễm nguồn nước, làm suy giảm chất lượng nước và ảnh hưởng đến đời sống của các sinh vật thủy sinh.
- Ô nhiễm không khí: Amoniac trong không khí có thể gây mưa axit và góp phần vào sự hình thành các hạt bụi mịn, gây ô nhiễm không khí.
- Ô nhiễm đất: Amoniac trong phân bón có thể gây ô nhiễm đất, làm thay đổi độ pH của đất và ảnh hưởng đến sự phát triển của cây trồng.
7.1. Các Biện Pháp Giảm Thiểu Tác Động Tiêu Cực Của Amoniac Đến Môi Trường
Để giảm thiểu tác động tiêu cực của amoniac đến môi trường, cần thực hiện các biện pháp sau:
- Xử lý nước thải chứa amoniac: Áp dụng các công nghệ xử lý nước thải tiên tiến để loại bỏ amoniac trước khi xả thải ra môi trường.
- Sử dụng phân bón hợp lý: Sử dụng phân bón chứa amoniac đúng liều lượng và thời điểm để tránh gây ô nhiễm đất.
- Kiểm soát khí thải amoniac: Áp dụng các biện pháp kiểm soát khí thải để giảm thiểu lượng amoniac thải ra môi trường từ các hoạt động công nghiệp và nông nghiệp.
8. Amoniac Trong Xử Lý Nước Thải: Thách Thức Và Giải Pháp
Amoniac là một trong những chỉ tiêu quan trọng cần kiểm soát trong xử lý nước thải. Nồng độ amoniac cao trong nước thải có thể gây ra nhiều vấn đề môi trường nghiêm trọng.
8.1. Thách Thức Trong Xử Lý Amoniac Trong Nước Thải
Việc xử lý amoniac trong nước thải gặp phải nhiều thách thức:
- Chi phí: Các công nghệ xử lý amoniac thường đòi hỏi chi phí đầu tư và vận hành cao.
- Hiệu quả: Một số công nghệ xử lý amoniac có hiệu quả không cao, đặc biệt là khi nồng độ amoniac trong nước thải quá cao.
- Quản lý: Việc quản lý và vận hành các hệ thống xử lý amoniac đòi hỏi đội ngũ kỹ thuật có chuyên môn cao.
8.2. Các Giải Pháp Xử Lý Amoniac Trong Nước Thải
Hiện nay, có nhiều công nghệ xử lý amoniac trong nước thải khác nhau, bao gồm:
- Xử lý sinh học: Sử dụng vi sinh vật để chuyển hóa amoniac thành nitrat và nitơ. Đây là phương pháp phổ biến và hiệu quả. Theo nghiên cứu của Bộ Tài nguyên và Môi trường, xử lý sinh học có thể loại bỏ tới 90% amoniac trong nước thải.
- Xử lý hóa học: Sử dụng các hóa chất để oxy hóa amoniac thành nitơ. Phương pháp này thường được sử dụng khi nồng độ amoniac quá cao hoặc khi cần xử lý nhanh chóng.
- Xử lý vật lý: Sử dụng các phương pháp vật lý như stripping khí hoặc hấp phụ để loại bỏ amoniac khỏi nước thải.
Bảng: So sánh các công nghệ xử lý amoniac trong nước thải
| Công nghệ | Ưu điểm | Nhược điểm |
|---|---|---|
| Xử lý sinh học | Hiệu quả cao, chi phí vận hành thấp | Đòi hỏi diện tích lớn, thời gian xử lý dài |
| Xử lý hóa học | Xử lý nhanh, hiệu quả với nồng độ amoniac cao | Chi phí hóa chất cao, có thể tạo ra các sản phẩm phụ độc hại |
| Xử lý vật lý | Đơn giản, dễ vận hành | Hiệu quả không cao, chi phí đầu tư ban đầu lớn |
Nguồn: Tổng hợp từ các báo cáo khoa học về xử lý nước thải
9. FAQ: Các Câu Hỏi Thường Gặp Về Amoniac
9.1. Amoniac có mùi gì?
Amoniac có mùi khai đặc trưng, xốc và gây khó chịu.
9.2. Amoniac có cháy không?
Amoniac không dễ cháy trong điều kiện thường. Tuy nhiên, nó có thể cháy trong không khí với nồng độ cao và có nguồn nhiệt mạnh.
9.3. Amoniac có ăn mòn không?
Amoniac có tính ăn mòn đối với một số kim loại, đặc biệt là đồng và kẽm.
9.4. Amoniac có tác dụng gì trong nông nghiệp?
Amoniac là nguyên liệu chính để sản xuất các loại phân đạm, giúp cung cấp nitơ cho cây trồng.
9.5. Làm thế nào để nhận biết rò rỉ amoniac?
Rò rỉ amoniac có thể được nhận biết qua mùi khai đặc trưng và sự xuất hiện của khói trắng.
9.6. Amoniac có gây hại cho sức khỏe không?
Có, amoniac là một chất độc hại. Tiếp xúc với amoniac nồng độ cao có thể gây kích ứng da, mắt và đường hô hấp, thậm chí tử vong.
9.7. Amoniac được sử dụng trong ngành công nghiệp nào?
Amoniac được sử dụng trong nhiều ngành công nghiệp, bao gồm sản xuất phân bón, hóa chất, dệt nhuộm, và xử lý nước.
9.8. Amoniac có gây ô nhiễm môi trường không?
Có, amoniac có thể gây ô nhiễm nước, không khí và đất nếu không được xử lý đúng cách.
9.9. Làm thế nào để bảo quản amoniac an toàn?
Amoniac cần được bảo quản ở nơi khô ráo, thoáng mát, tránh xa nguồn nhiệt và ánh sáng trực tiếp.
9.10. Amoniac có thể loại bỏ khỏi nước bằng cách nào?
Amoniac có thể được loại bỏ khỏi nước bằng các phương pháp xử lý sinh học, hóa học và vật lý.
10. Liên Hệ Xe Tải Mỹ Đình Để Được Tư Vấn
Qua bài viết này, Xe Tải Mỹ Đình hy vọng bạn đã có câu trả lời đầy đủ cho câu hỏi “NH3 có tan trong nước không?” và hiểu rõ hơn về các khía cạnh liên quan đến amoniac. Nếu bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về xe tải ở Mỹ Đình, hoặc có bất kỳ thắc mắc nào liên quan đến lĩnh vực này, đừng ngần ngại liên hệ với chúng tôi tại XETAIMYDINH.EDU.VN.
Chúng tôi cam kết cung cấp thông tin chính xác, cập nhật và hữu ích nhất, giúp bạn đưa ra những quyết định sáng suốt. Hãy truy cập trang web của chúng tôi ngay hôm nay để khám phá thêm nhiều thông tin giá trị và nhận được sự tư vấn tận tình từ đội ngũ chuyên gia của Xe Tải Mỹ Đình.
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
Hotline: 0247 309 9988.
Trang web: XETAIMYDINH.EDU.VN.
Hãy để Xe Tải Mỹ Đình đồng hành cùng bạn trên mọi nẻo đường!
