Mol Là Lượng Chất Chứa đựng bao nhiêu nguyên tử hoặc phân tử? Ứng dụng của nó trong tính toán hóa học ra sao? Xe Tải Mỹ Đình sẽ giải đáp tất tần tật những thắc mắc này, giúp bạn hiểu rõ về mol và ứng dụng hiệu quả trong công việc và học tập. Cùng khám phá khái niệm, khối lượng mol, thể tích mol và cách tính toán liên quan đến mol nhé!
1. Mol Là Lượng Chất Chứa Bao Nhiêu? Định Nghĩa Chi Tiết
Mol là lượng chất chứa một số lượng hạt vi mô (nguyên tử, phân tử, ion,…) tương đương với số nguyên tử có trong 12 gam cacbon-12 (12C). Số lượng hạt này được gọi là số Avogadro, ký hiệu là NA, và có giá trị xấp xỉ 6,022 x 1023.
Hiểu một cách đơn giản, 1 mol của một chất bất kỳ sẽ chứa 6,022 x 1023 hạt cấu thành chất đó. Số Avogadro là một hằng số quan trọng trong hóa học, cho phép chúng ta chuyển đổi giữa số lượng hạt vi mô và lượng chất vĩ mô có thể cân, đo, đếm được.
Ví dụ:
- 1 mol nguyên tử đồng (Cu) chứa 6,022 x 1023 nguyên tử Cu.
- 1 mol phân tử nước (H2O) chứa 6,022 x 1023 phân tử H2O.
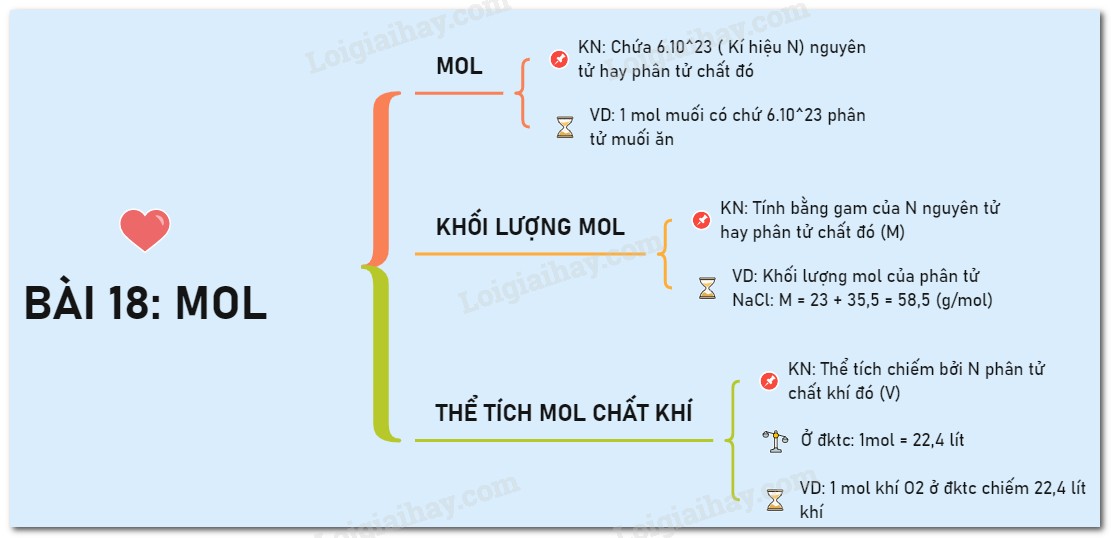 Ảnh sơ đồ tư duy mol
Ảnh sơ đồ tư duy mol
Alt text: Sơ đồ tư duy về mol, bao gồm định nghĩa, khối lượng mol, thể tích mol và các công thức tính toán liên quan.
1.1 Số Avogadro Là Gì?
Số Avogadro (NA), như đã đề cập ở trên, là số lượng hạt (nguyên tử, phân tử, ion,…) có trong một mol chất. Giá trị chính xác của số Avogadro là 6,02214076 x 1023 mol-1.
Số Avogadro được đặt theo tên của nhà khoa học người Ý Amedeo Avogadro, người có những đóng góp quan trọng trong việc phát triển khái niệm về mol và mối quan hệ giữa số lượng hạt và lượng chất.
1.2 Phân Biệt Giữa Mol Nguyên Tử Và Mol Phân Tử Như Thế Nào?
Việc phân biệt giữa mol nguyên tử và mol phân tử là rất quan trọng để tránh nhầm lẫn trong các bài toán hóa học.
- Mol nguyên tử: Là lượng chất chứa 6,022 x 1023 nguyên tử của nguyên tố đó.
- Ví dụ: 1 mol nguyên tử oxy (O) chứa 6,022 x 1023 nguyên tử O.
- Mol phân tử: Là lượng chất chứa 6,022 x 1023 phân tử của hợp chất đó.
- Ví dụ: 1 mol phân tử oxy (O2) chứa 6,022 x 1023 phân tử O2.
Lưu ý: 1 mol phân tử O2 chứa 2 mol nguyên tử O.
Để hiểu rõ hơn, hãy xem xét ví dụ sau:
- 1 mol H (hydro) chỉ 1 mol nguyên tử hydro.
- 1 mol H2 (khí hydro) chỉ 1 mol phân tử hydro.
2. Khối Lượng Mol Là Gì? Cách Tính Khối Lượng Mol?
Khối lượng mol (M) của một chất là khối lượng tính bằng gam của một mol chất đó. Khối lượng mol có cùng giá trị số với khối lượng nguyên tử (đối với nguyên tố) hoặc khối lượng phân tử (đối với hợp chất), nhưng có đơn vị là gam/mol (g/mol).
2.1 Cách Tính Khối Lượng Mol Của Nguyên Tố
Khối lượng mol của một nguyên tố bằng với khối lượng nguyên tử của nguyên tố đó, được tra cứu trong bảng tuần hoàn các nguyên tố hóa học.
Ví dụ:
- Khối lượng mol của natri (Na) là 23 g/mol.
- Khối lượng mol của clo (Cl) là 35,5 g/mol.
2.2 Cách Tính Khối Lượng Mol Của Hợp Chất
Khối lượng mol của một hợp chất bằng tổng khối lượng mol của các nguyên tố tạo nên hợp chất đó, nhân với số lượng nguyên tử của mỗi nguyên tố trong công thức hóa học của hợp chất.
Ví dụ:
Tính khối lượng mol của nước (H2O):
- Khối lượng mol của H là 1 g/mol.
- Khối lượng mol của O là 16 g/mol.
- MH2O = (1 x 2) + 16 = 18 g/mol.
Tính khối lượng mol của axit sunfuric (H2SO4):
- Khối lượng mol của H là 1 g/mol.
- Khối lượng mol của S là 32 g/mol.
- Khối lượng mol của O là 16 g/mol.
- MH2SO4 = (1 x 2) + 32 + (16 x 4) = 98 g/mol.
2.3 Mối Quan Hệ Giữa Khối Lượng (m), Số Mol (n) Và Khối Lượng Mol (M)
Mối quan hệ giữa khối lượng (m), số mol (n) và khối lượng mol (M) được biểu diễn bằng công thức:
n = m / M
Trong đó:
- n là số mol (đơn vị: mol).
- m là khối lượng (đơn vị: gam).
- M là khối lượng mol (đơn vị: g/mol).
Công thức này cho phép chúng ta chuyển đổi giữa khối lượng và số mol của một chất, và ngược lại.
Ví dụ:
Tính số mol của 9 gam nước (H2O):
- m = 9 g.
- MH2O = 18 g/mol.
- n = 9 / 18 = 0,5 mol.
Tính khối lượng của 0,2 mol natri clorua (NaCl):
- n = 0,2 mol.
- MNaCl = 23 + 35,5 = 58,5 g/mol.
- m = 0,2 x 58,5 = 11,7 g.
3. Thể Tích Mol Là Gì? Điều Kiện Tiêu Chuẩn (Đktc) Là Gì?
Thể tích mol (Vm) của một chất khí là thể tích chiếm bởi một mol chất khí đó ở một điều kiện nhiệt độ và áp suất xác định.
3.1 Thể Tích Mol Của Chất Khí Ở Điều Kiện Tiêu Chuẩn (Đktc)
Điều kiện tiêu chuẩn (đktc) là điều kiện nhiệt độ và áp suất được quy định là 0°C (273,15 K) và 1 atm (101,325 kPa).
Ở điều kiện tiêu chuẩn (đktc), thể tích mol của mọi chất khí đều bằng 22,4 lít/mol.
Vm = 22,4 lít/mol (ở đktc)
3.2 Mối Quan Hệ Giữa Thể Tích (V), Số Mol (n) Và Thể Tích Mol (Vm)
Mối quan hệ giữa thể tích (V), số mol (n) và thể tích mol (Vm) của chất khí được biểu diễn bằng công thức:
n = V / Vm
Trong đó:
- n là số mol (đơn vị: mol).
- V là thể tích (đơn vị: lít).
- Vm là thể tích mol (đơn vị: lít/mol).
Công thức này cho phép chúng ta chuyển đổi giữa thể tích và số mol của chất khí ở điều kiện nhất định.
Ví dụ:
Tính số mol của 44,8 lít khí CO2 ở đktc:
- V = 44,8 lít.
- Vm = 22,4 lít/mol.
- n = 44,8 / 22,4 = 2 mol.
Tính thể tích của 0,5 mol khí nitơ (N2) ở đktc:
- n = 0,5 mol.
- Vm = 22,4 lít/mol.
- V = 0,5 x 22,4 = 11,2 lít.
3.3 Lưu Ý Khi Sử Dụng Thể Tích Mol
- Công thức Vm = 22,4 lít/mol chỉ áp dụng cho chất khí ở điều kiện tiêu chuẩn (đktc).
- Ở điều kiện khác đktc, thể tích mol của chất khí sẽ khác 22,4 lít/mol và phải được tính toán bằng các phương trình trạng thái khí (ví dụ: phương trình Clapeyron-Mendeleev).
4. Các Công Thức Tính Mol Thông Dụng Nhất
Để giúp bạn dễ dàng áp dụng khái niệm mol vào giải các bài toán hóa học, Xe Tải Mỹ Đình tổng hợp các công thức tính mol thông dụng nhất:
-
Tính số mol khi biết khối lượng:
n = m / M
Trong đó:
- n là số mol (mol).
- m là khối lượng (gam).
- M là khối lượng mol (g/mol).
-
Tính số mol khi biết thể tích (ở đktc):
n = V / 22,4
Trong đó:
- n là số mol (mol).
- V là thể tích (lít).
-
Tính số mol khi biết số lượng hạt (N):
n = N / NA
Trong đó:
- n là số mol (mol).
- N là số lượng hạt (nguyên tử, phân tử,…).
- NA là số Avogadro (6,022 x 1023).
-
Tính số mol khi biết nồng độ mol (C) và thể tích dung dịch (V):
n = C x V
Trong đó:
- n là số mol (mol).
- C là nồng độ mol (mol/lít).
- V là thể tích dung dịch (lít).
5. Ứng Dụng Của Mol Trong Hóa Học Và Đời Sống
Mol là một khái niệm cơ bản và quan trọng trong hóa học, được sử dụng rộng rãi trong nhiều lĩnh vực khác nhau:
5.1 Trong Tính Toán Hóa Học
- Tính toán lượng chất tham gia và sản phẩm trong phản ứng hóa học: Mol cho phép chúng ta xác định tỷ lệ số mol giữa các chất trong phản ứng, từ đó tính toán được lượng chất cần thiết để phản ứng hoàn toàn hoặc lượng sản phẩm tạo thành.
- Xác định công thức hóa học của hợp chất: Dựa vào thành phần phần trăm về khối lượng của các nguyên tố trong hợp chất, ta có thể tính được tỷ lệ số mol giữa các nguyên tố, từ đó suy ra công thức hóa học đơn giản nhất (công thức thực nghiệm) của hợp chất.
- Tính toán nồng độ dung dịch: Mol được sử dụng để biểu diễn nồng độ của dung dịch (nồng độ mol, nồng độ molan), giúp chúng ta định lượng chính xác lượng chất tan trong dung dịch.
5.2 Trong Nghiên Cứu Khoa Học
- Nghiên cứu về cấu trúc và tính chất của vật chất: Mol là đơn vị cơ bản để đo lượng chất, giúp các nhà khoa học nghiên cứu về cấu trúc và tính chất của vật chất ở cấp độ nguyên tử và phân tử.
- Phát triển vật liệu mới: Mol được sử dụng trong quá trình tổng hợp và chế tạo các vật liệu mới, đảm bảo tỷ lệ chính xác giữa các thành phần để đạt được tính chất mong muốn.
5.3 Trong Đời Sống Hàng Ngày
- Sản xuất hóa chất: Mol được sử dụng trong quá trình sản xuất các hóa chất công nghiệp, dược phẩm, phân bón,… đảm bảo chất lượng và hiệu quả của sản phẩm.
- Kiểm tra chất lượng sản phẩm: Mol được sử dụng để kiểm tra hàm lượng các chất trong thực phẩm, đồ uống, mỹ phẩm,… đảm bảo an toàn cho người tiêu dùng.
- Ứng dụng trong nông nghiệp: Mol được sử dụng để tính toán lượng phân bón cần thiết cho cây trồng, giúp tăng năng suất và chất lượng nông sản.
6. Bài Tập Vận Dụng Về Mol (Có Hướng Dẫn Giải Chi Tiết)
Để củng cố kiến thức về mol, Xe Tải Mỹ Đình xin giới thiệu một số bài tập vận dụng có hướng dẫn giải chi tiết:
Bài 1: Tính số mol của 36 gam glucozơ (C6H12O6).
Hướng dẫn giải:
- Khối lượng mol của glucozơ: MC6H12O6 = (12 x 6) + (1 x 12) + (16 x 6) = 180 g/mol.
- Số mol của glucozơ: n = m / M = 36 / 180 = 0,2 mol.
Bài 2: Tính thể tích của 5,6 gam khí nitơ (N2) ở đktc.
Hướng dẫn giải:
- Số mol của khí nitơ: n = m / M = 5,6 / 28 = 0,2 mol.
- Thể tích của khí nitơ ở đktc: V = n x 22,4 = 0,2 x 22,4 = 4,48 lít.
Bài 3: Có bao nhiêu phân tử nước (H2O) trong 0,1 mol nước?
Hướng dẫn giải:
- Số phân tử nước: N = n x NA = 0,1 x 6,022 x 1023 = 6,022 x 1022 phân tử.
Bài 4: Hòa tan 4 gam NaOH vào nước để được 200 ml dung dịch. Tính nồng độ mol của dung dịch NaOH.
Hướng dẫn giải:
- Số mol của NaOH: n = m / M = 4 / 40 = 0,1 mol.
- Thể tích dung dịch: V = 200 ml = 0,2 lít.
- Nồng độ mol của dung dịch NaOH: C = n / V = 0,1 / 0,2 = 0,5 mol/lít.
Bài 5: Đốt cháy hoàn toàn 6 gam magie (Mg) trong không khí. Tính khối lượng magie oxit (MgO) tạo thành.
Hướng dẫn giải:
- Phương trình hóa học của phản ứng: 2Mg + O2 → 2MgO.
- Số mol của Mg: nMg = m / M = 6 / 24 = 0,25 mol.
- Theo phương trình phản ứng, số mol MgO tạo thành bằng số mol Mg phản ứng: nMgO = nMg = 0,25 mol.
- Khối lượng MgO tạo thành: mMgO = n x M = 0,25 x 40 = 10 gam.
7. FAQ: Các Câu Hỏi Thường Gặp Về Mol
Dưới đây là một số câu hỏi thường gặp về mol, được Xe Tải Mỹ Đình tổng hợp và giải đáp:
7.1 Tại Sao Cần Sử Dụng Mol Thay Vì Khối Lượng Trong Tính Toán Hóa Học?
Mol là đơn vị đo lượng chất dựa trên số lượng hạt vi mô (nguyên tử, phân tử,…), trong khi khối lượng là đại lượng đo lượng vật chất. Trong phản ứng hóa học, các chất phản ứng với nhau theo một tỷ lệ số mol nhất định, không phải theo tỷ lệ khối lượng. Do đó, sử dụng mol giúp chúng ta tính toán chính xác lượng chất tham gia và sản phẩm trong phản ứng.
7.2 Số Avogadro Có Ý Nghĩa Gì Trong Hóa Học?
Số Avogadro (NA) là số lượng hạt (nguyên tử, phân tử, ion,…) có trong một mol chất. Nó là một hằng số quan trọng trong hóa học, cho phép chúng ta chuyển đổi giữa số lượng hạt vi mô và lượng chất vĩ mô có thể cân, đo, đếm được.
7.3 Thể Tích Mol Có Phải Luôn Bằng 22,4 Lít/Mol Không?
Không, thể tích mol chỉ bằng 22,4 lít/mol ở điều kiện tiêu chuẩn (đktc: 0°C và 1 atm). Ở điều kiện khác đktc, thể tích mol của chất khí sẽ khác 22,4 lít/mol và phải được tính toán bằng các phương trình trạng thái khí.
7.4 Làm Thế Nào Để Chuyển Đổi Giữa Khối Lượng, Số Mol Và Thể Tích?
Chúng ta có thể chuyển đổi giữa khối lượng, số mol và thể tích bằng các công thức sau:
- n = m / M (chuyển đổi giữa khối lượng và số mol).
- n = V / 22,4 (chuyển đổi giữa thể tích ở đktc và số mol).
7.5 Mol Có Ứng Dụng Gì Trong Đời Sống Hàng Ngày?
Mol có nhiều ứng dụng trong đời sống hàng ngày, ví dụ như trong sản xuất hóa chất, kiểm tra chất lượng sản phẩm, ứng dụng trong nông nghiệp,…
7.6 Khối Lượng Mol Của Một Chất Có Thay Đổi Không?
Khối lượng mol của một chất là một hằng số, không thay đổi theo điều kiện nhiệt độ, áp suất hay trạng thái của chất.
7.7 Tại Sao Cần Phân Biệt Giữa Mol Nguyên Tử Và Mol Phân Tử?
Việc phân biệt giữa mol nguyên tử và mol phân tử là rất quan trọng để tránh nhầm lẫn trong các bài toán hóa học. Ví dụ, 1 mol phân tử oxy (O2) chứa 2 mol nguyên tử oxy (O).
7.8 Làm Thế Nào Để Tính Khối Lượng Mol Của Một Hợp Chất?
Để tính khối lượng mol của một hợp chất, ta cộng khối lượng mol của các nguyên tố tạo nên hợp chất đó, nhân với số lượng nguyên tử của mỗi nguyên tố trong công thức hóa học của hợp chất.
7.9 Mol Có Phải Là Đơn Vị Đo Lường Quốc Tế (SI) Không?
Có, mol là một trong bảy đơn vị cơ bản của Hệ đo lường quốc tế (SI).
7.10 Có Cách Nào Để Ghi Nhớ Các Công Thức Tính Mol Một Cách Dễ Dàng Hơn Không?
Bạn có thể sử dụng các sơ đồ tư duy hoặc các mẹo nhớ để ghi nhớ các công thức tính mol một cách dễ dàng hơn.
8. Xe Tải Mỹ Đình – Địa Chỉ Tin Cậy Cho Mọi Thông Tin Về Xe Tải
Bạn đang tìm kiếm thông tin chi tiết và đáng tin cậy về các loại xe tải ở Mỹ Đình, Hà Nội? Bạn muốn so sánh giá cả và thông số kỹ thuật giữa các dòng xe? Bạn cần tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách? Hãy đến với Xe Tải Mỹ Đình!
Tại XETAIMYDINH.EDU.VN, chúng tôi cung cấp:
- Thông tin chi tiết và cập nhật về các loại xe tải có sẵn ở Mỹ Đình, Hà Nội.
- So sánh giá cả và thông số kỹ thuật giữa các dòng xe.
- Tư vấn lựa chọn xe phù hợp với nhu cầu và ngân sách.
- Giải đáp các thắc mắc liên quan đến thủ tục mua bán, đăng ký và bảo dưỡng xe tải.
- Thông tin về các dịch vụ sửa chữa xe tải uy tín trong khu vực.
Địa chỉ: Số 18 đường Mỹ Đình, phường Mỹ Đình 2, quận Nam Từ Liêm, Hà Nội.
Hotline: 0247 309 9988.
Trang web: XETAIMYDINH.EDU.VN.
Liên hệ ngay với Xe Tải Mỹ Đình để được tư vấn và giải đáp mọi thắc mắc!
Từ khóa LSI: đơn vị mol, số hạt, lượng chất, công thức hóa học.